Clear Sky Science · sv
Kvantitativ liveavbildning visar att PRICKLE1 styr junctional neural tube-morfogenes oberoende av planär cellpolaritet
Hur tidig nervbildning formar våra hjärnor och ryggmärgar
Innan ett människoembryo ens är lika stort som ett riskorn måste ett platt cellskikt vikas och slutas till ett ihåligt rör som senare blir hjärnan och ryggmärgen. När den här processen går fel kan barn födas med allvarliga ryggmärgsdefekter. I den här studien används toppmodern liveavbildning i små vakteläggsembryon för att i realtid följa denna omvandling, vilket avslöjar ett överraskande cellbeteende och ett nyckelproteins roll som tillsammans hjälper till att förebygga en särskild klass av ryggproblem.
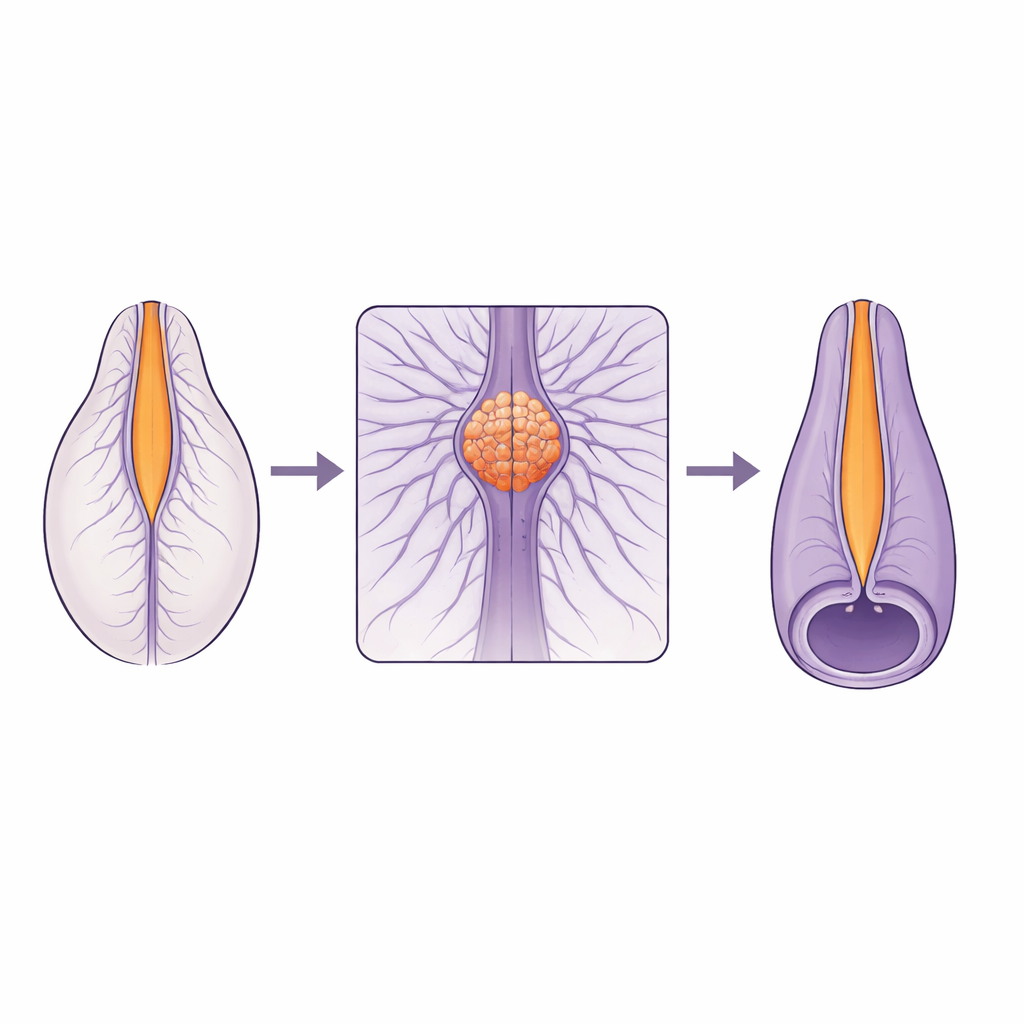
En ömtålig fog i den växande ryggraden
Ryggmärgen bildas inte på ett enda sätt längs hela sin längd. Den övre delen uppstår genom att ett platt vävnadsskikt viks och sluts, medan den nedre delen bildas från en solid stav av celler som inifrån blir ihålig. Dessa två byggprogram måste mötas och smälta samman smidigt i ett litet område som kallas junctionalzonen. Många mänskliga ryggmärgsdefekter samlas nära denna fog, vilket tyder på att den är särskilt sårbar. Fram till nu har forskare dock saknat direkta, högupplösta levande bilder som visar hur celler faktiskt rör sig och ändrar form i denna zon medan röret sluts.
Att se celler röra sig och dyka under ytan
Forskarna använde transgena vakteläggsembryon vars celler lyser under mikroskopet, vilket gjorde det möjligt att följa hundratals enskilda celler över flera timmar. De fann att junctional neural tube bildas genom två samordnade rörelser. Först kryper celler från sidorna mot mittlinjen, en rörelse som kallas mediolateral konvergens och som smalnar av vävnaden. För det andra gör en rand av celler precis i mitten något mer dramatiskt: dessa celler krymper sina övre (apikala) ytor och faller sedan ner under ytan in i djupare vävnad, ett beteende känt som ingression. Denna ingression liknar en epitel-till-mesenkymal övergång, där ordnade skivlika celler blir mer rörliga, men här sker det i celler som behåller sin neurala identitet och som främst bidrar till ryggmärgen snarare än till andra vävnader.
En överraskande roll för ett känt polaritetsprotein
Tidigare arbete hade pekat ut ett protein kallat PRICKLE1 i denna junctionalzon. PRICKLE1 är vanligtvis känt som en del av systemet för planär cellpolaritet, som orienterar celler sidledes och hjälper vävnader att förlängas. Man skulle kunna förvänta sig att borttagning av PRICKLE1 skulle störa denna polaritet. Istället, när teamet minskade PRICKLE1-nivåerna specifikt i junctionalzonen, förblev de vanliga polaritetsmönstren och de långa aktinkablar som styr konvergens i stort sett intakta. Det som förändrades var beteendet hos de mediala cellerna: de lyckades inte dra ihop sina apikala ytor, de ingressade inte korrekt, och den bakre öppningen av neuralröret förblev öppen, vilket ledde till junctionala neuralrörsdefekter i embryona.
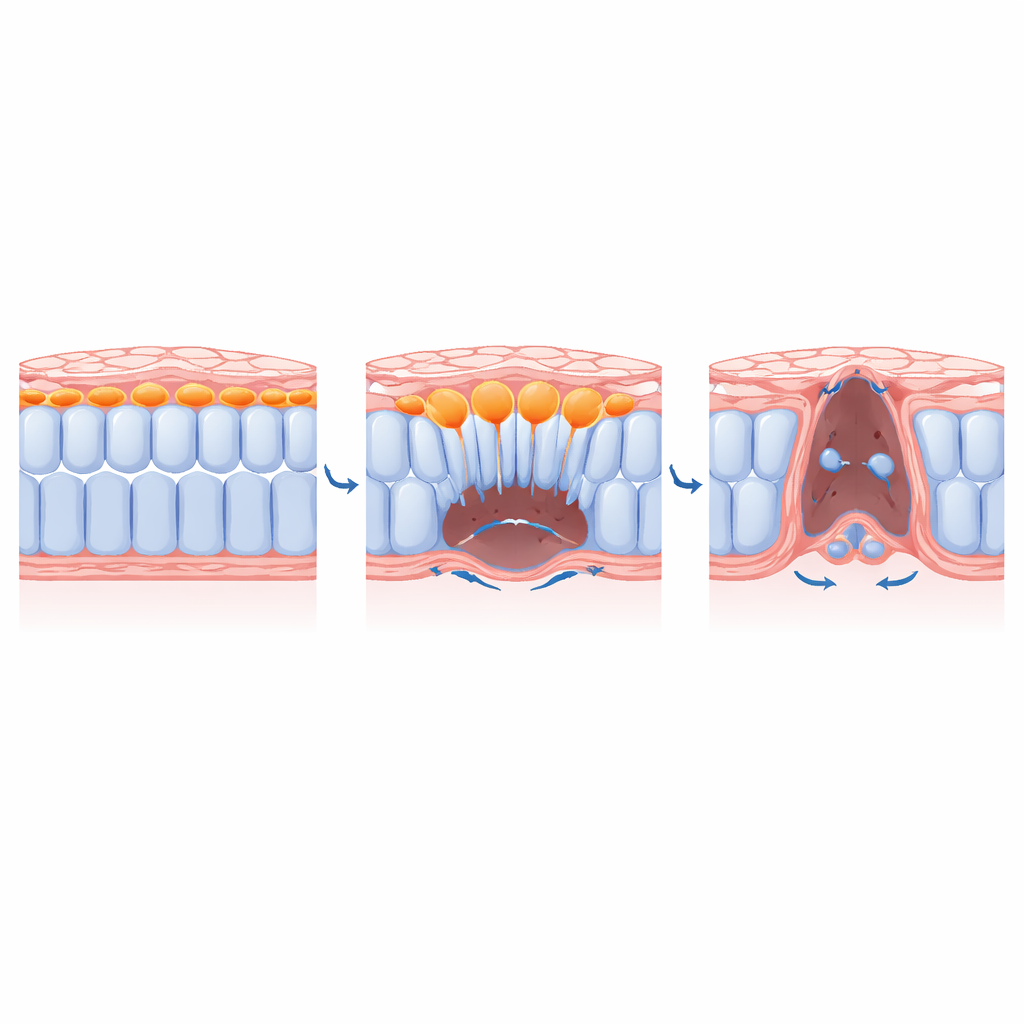
Hur centrala celler skapar plats åt sina grannar
Genom att kombinera genetiska verktyg, läkemedel och till och med ljusaktiverade hämmare av myosin (motorn som driver kontraktion) dissekerade teamet hur ingressionen styrs. De visade att viktiga EMT-regulatorer såsom transkriptionsfaktorn SLUG och signaler från fibroblasttillväxtfaktorer krävs för att mediala celler ska anta en utskjutande, migratorisk form och bryta ner det stödjande matrix under sig. Att blockera dessa signaler fångade mediala celler nära dorsalyten och hindrade dem från att röra sig ventralt. Avgörande var att när forskarna inaktiverade kontraktion endast i de mediala cellerna, ingressade dessa celler inte längre, och laterala grannar kunde inte fullt ut konvergera mot mittlinjen. Med andra ord rensar handlingen att centrala celler dyker in fysiskt utrymme som tillåter att den återstående cellskivan dragits ihop och sluts.
Varför detta är viktigt för mänskliga ryggmärgsdefekter
Arbetet visar att PRICKLE1 har en PCP-oberoende uppgift vid den apikala kortexen hos mediala celler: det främjar uppbyggnaden av kontraktilt aktin och myosin som behövs för apikal sammandragning och ingression. Utan denna funktion, även om sidledes polaritetsflöden kvarstår, stannar den centrala EMT-liknande processen av och neuralröret sluts inte vid junctionen. Eftersom mänskliga mutationer i PRICKLE1 oftast kopplas till lokaliserade spinala dysrafier — junctionala neuralrörsdefekter — erbjuder dessa fynd en konkret cellulär förklaring. För en allmän läsare är huvudpoängen att en liten grupp celler både måste dra ihop sina toppar och dyka under ytan på precis rätt plats och tid, och att proteinet PRICKLE1 är en avgörande växel för denna rörelse. När den växeln sviktar kan inte fogen mellan övre och nedre ryggmärg bildas korrekt, vilket bidrar till att förklara en specifik och allvarlig klass av födelsefel.
Citering: Wang, J.X., Alvarez, Y.D., Tan, S.Z. et al. Quantitative live imaging reveals PRICKLE1 controls junctional neural tube morphogenesis independent of Planar Cell Polarity. Nat Commun 17, 3654 (2026). https://doi.org/10.1038/s41467-026-71242-0
Nyckelord: neuralrörsdefekter, PRICKLE1, epitel-till-mesenkymal övergång, embryonal utveckling, cellmigration