Clear Sky Science · zh
使用人类 iPSC 衍生皮层网络模拟儿童痴呆中的突触功能障碍
这项研究为何与家庭息息相关
儿童痴呆是一类令人心碎的大脑疾病,患儿会逐步丧失记忆、思维能力和独立生活能力。其中一种常见类型——桑菲利普综合征 A 型,目前尚无治愈方法,治疗选择有限。本研究利用先进的干细胞技术在实验室中培育出微型的人类脑网络,让科学家得以观察受影响儿童来源的神经元随时间的行为。通过揭示这些细胞出问题的具体方式,工作指向了新的药物策略,可能在儿童确诊较晚时仍能保护其思维和学习能力。
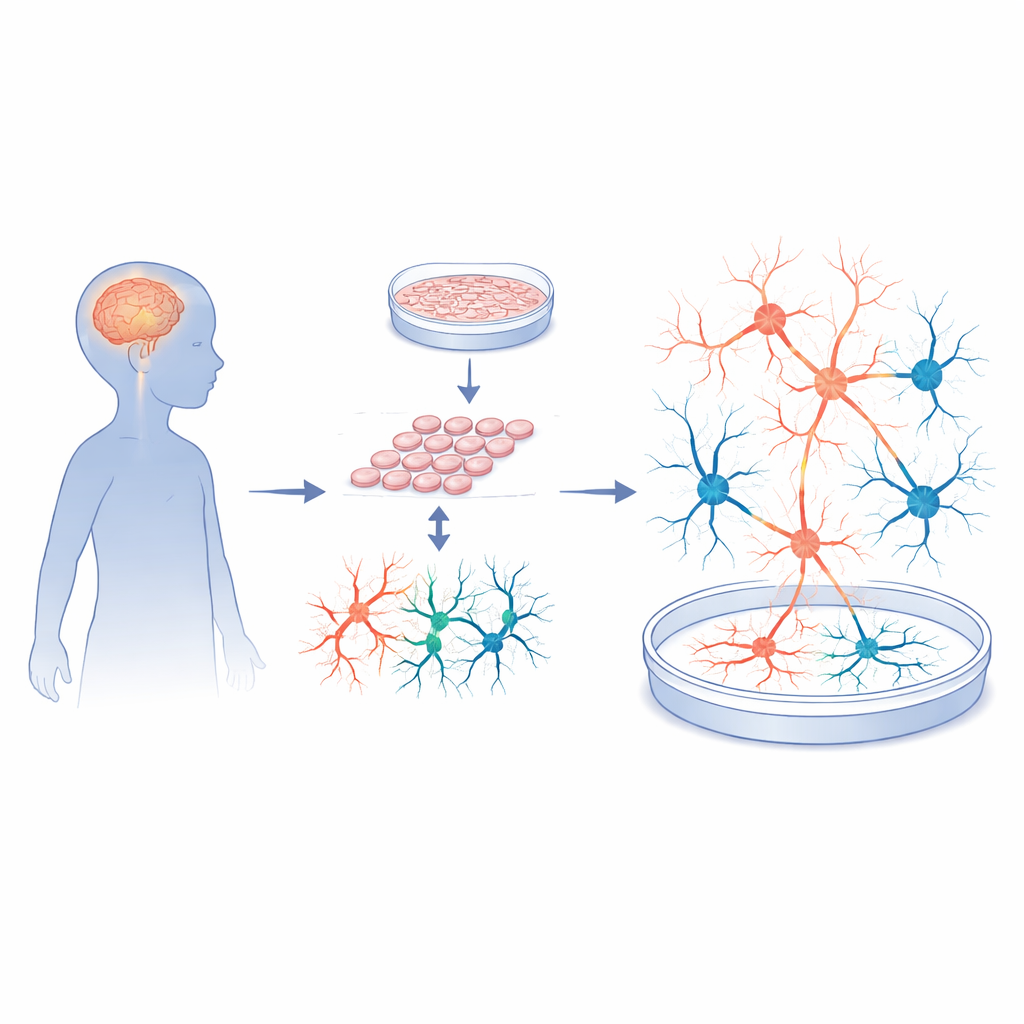
把皮肤细胞变成可工作的脑电路
研究人员从五名桑菲利普 A 型患儿和五名年龄配对的神经典型供者处取皮肤活检,首先将这些皮肤细胞重编程为诱导多能干细胞(iPSC),这种可塑性细胞几乎能分化为任何组织。随后,他们将这些干细胞精细引导为皮层神经元和支持细胞,模拟参与学习、记忆与行为的大脑区域。严格的质量检测显示,患者和对照的干细胞生长良好、染色体正常,且能形成高质量的神经前体细胞。换言之,随后观察到的脑样活动差异不太可能由基本的细胞生成过程缺陷引起。
起初看起来形态与放电都正常的神经元
接下来,团队检查了单个神经元的形态和电活动。通过精细成像,他们重建了数百个单细胞,发现患者与对照神经元具有相似复杂的分支模式——这表明桑菲利普并不阻止这些细胞建立丰富的连接网络。电生理记录显示,两组神经元都能产生强度、速度和阈值相当的动作电位(传递信息的电信号)。产生这些脉冲的关键离子通道也运行正常。因此在发育早期,桑菲利普神经元在外观和放电能力上与典型神经元非常相似。
“加速”与“刹车”信号之间的隐性失衡
问题在实验室培养的网络成熟后显现。团队测量了当相邻细胞释放化学信使时流入神经元的微小电流。数周内,桑菲利普神经元出现了更多兴奋性突触——传递“加速”信号的连接,伴随 PSD95 蛋白簇增多。而提供“停止”信号的抑制性突触相对滞后,导致向兴奋方向的不健康倾斜。患者神经元的兴奋性电流变得更频繁且更强,而抑制性电流基本保持不变。当科学家通过短暂去除生长因子和抗氧化剂来引入轻度细胞应激时,患者培养物中的兴奋性偏向变得更明显,而神经典型网络基本未受影响。
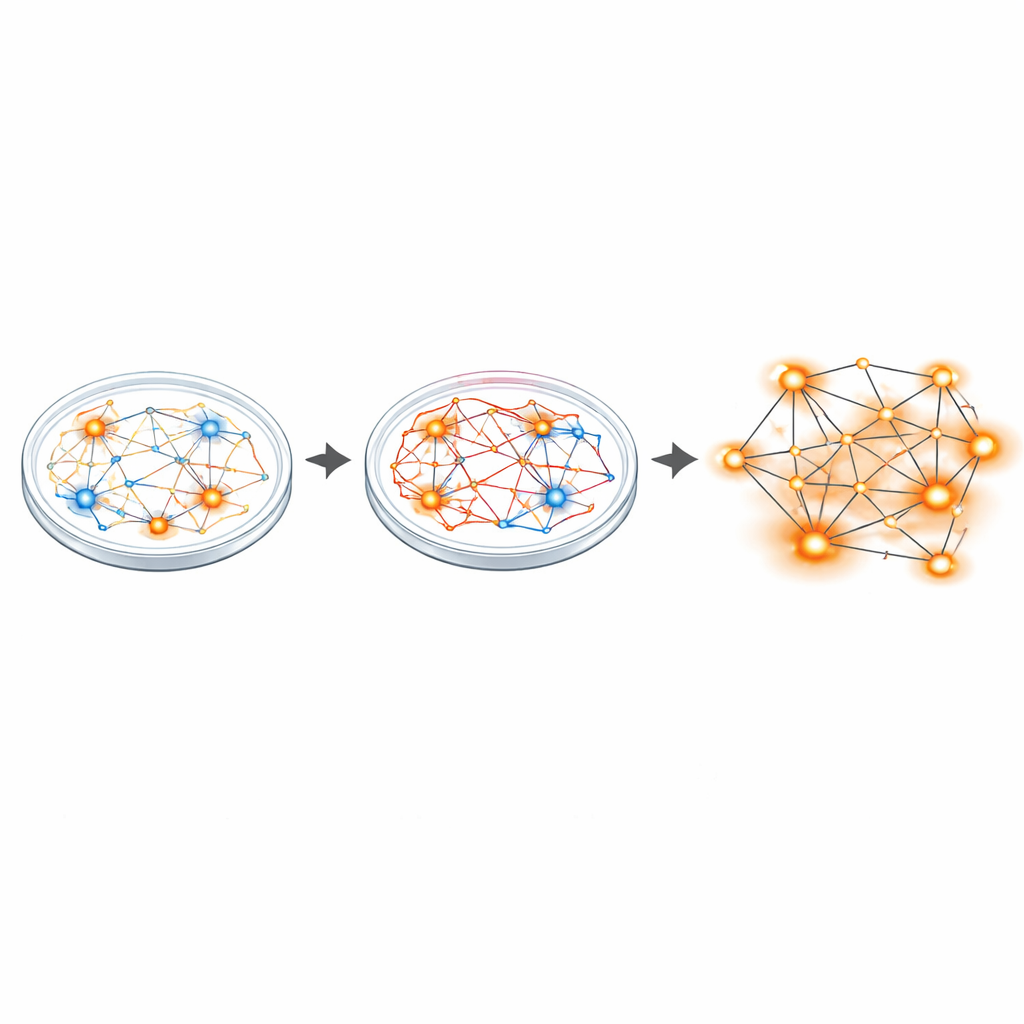
从过度兴奋的突触到过度活跃的网络
为了观察这种失衡在电路层面的表现,研究者使用了多电极阵列——可同时记录多枚神经元的微型网格。虽然患者来源的单个神经元的平均放电率与对照相近,但整体网络呈现不同图景。桑菲利普培养物中更活跃且易爆发的神经元更多,且同步化的网络事件约为对照的两倍,这种协调放电的模式表明电路过度活跃。随后对数千个细胞进行了单核 RNA 测序,揭示出基因表达的广泛改变,尤其是参与构建和增强谷氨酸能(兴奋性)突触的基因。其中若干基因与其他表现为兴奋—抑制失衡的脑疾病有关,如自闭症和精神分裂症。
这对未来治疗的意义
对非专业读者而言,关键结论是:在这种儿童痴呆中,神经元的基础连接结构大体完好,但大脑“油门”和“刹车”之间的平衡会随着时间失调。神经元受到过多兴奋性输入驱动,导致网络过度活跃,这可能为随后发生的退行性变和认知能力丧失奠定基础。由于团队可以在培养皿中使用患者来源的细胞再现这些改变,他们建立的模型为寻找能够恢复兴奋—抑制平衡的药物提供了有力平台。此类治疗并不会替代造成桑菲利普的缺失酶,但可能有助于维持思维与行为功能——从而改善与该毁灭性疾病共处儿童的生活质量。
引用: Mazzachi, P., McDonald, E., Greenberg, Z. et al. Modelling synaptic dysfunction in childhood dementia using human iPSC-derived cortical networks. Nat Commun 17, 3161 (2026). https://doi.org/10.1038/s41467-026-71112-9
关键词: 儿童痴呆, 桑菲利普综合征, 突触失衡, 诱导多能干细胞, 神经网络过度兴奋