Clear Sky Science · pl
Modelowanie dysfunkcji synaptycznej w dziecięcej demencji przy użyciu ludzkich sieci korowych pochodzących z iPSC
Dlaczego te badania mają znaczenie dla rodzin
Dziecięca demencja to wyniszczająca grupa chorób mózgu, w których dzieci stopniowo tracą pamięć, zdolności poznawcze i samodzielność. Jedna z najczęstszych postaci, zespół Sanfilippo typu A, nie ma obecnie lekarstwa i oferuje ograniczone możliwości leczenia. W tym badaniu wykorzystano zaawansowane metody komórek macierzystych, by hodować w laboratorium miniaturowe ludzkie sieci mózgowe, co pozwala naukowcom obserwować, jak neurony pochodzące od chorych dzieci zachowują się w czasie. Dzięki ujawnieniu, w jaki sposób te komórki zawodzą, praca wskazuje nowe strategie lekowe, które mogłyby chronić myślenie i uczenie się, nawet jeśli rozpoznanie choroby nastąpi późno.
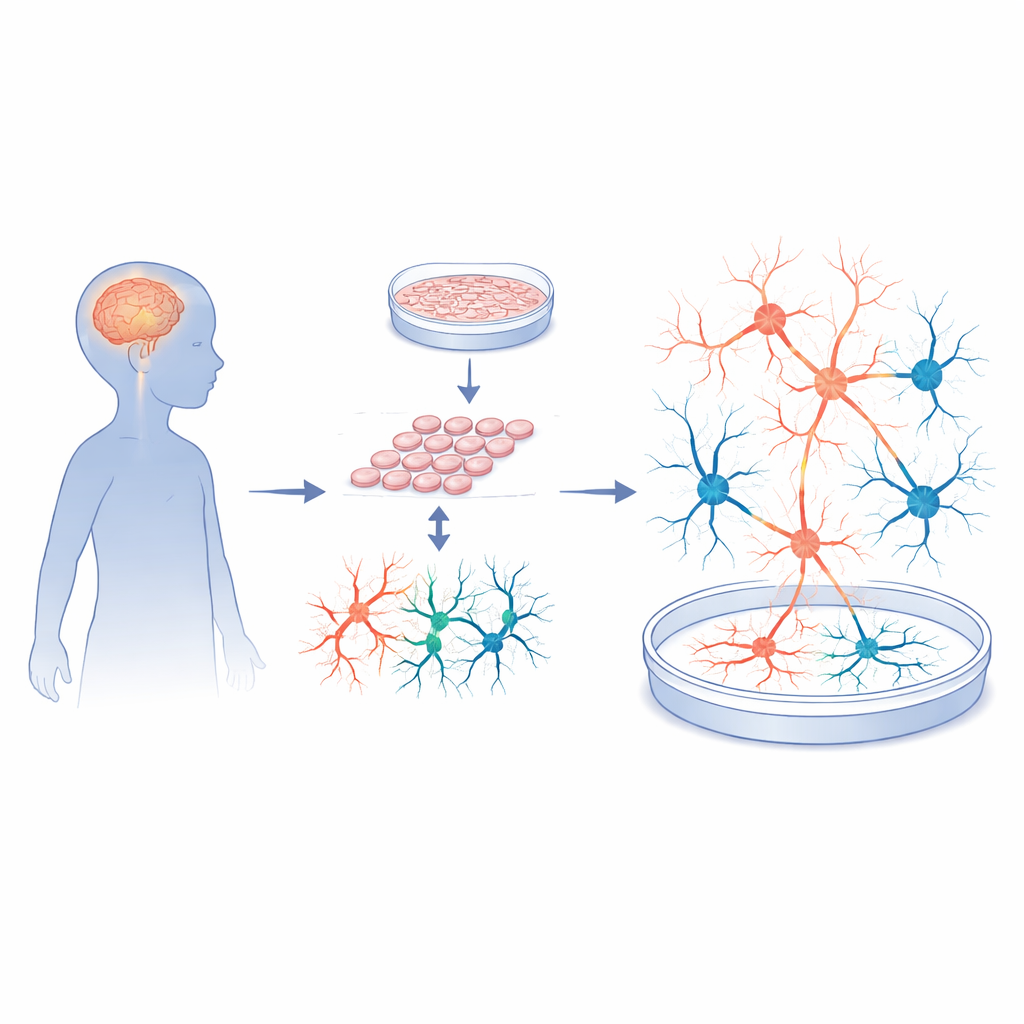
Przekształcanie komórek skóry w funkcjonujące obwody mózgowe
Naukowcy zaczęli od biopsji skóry pobranych od pięciorga dzieci z zespołem Sanfilippo typu A oraz pięciorga neurotypowych dawców dopasowanych wiekowo. Przeprogramowali te komórki skóry do indukowanych pluripotentnych komórek macierzystych — elastycznego typu komórek, który może przekształcić się niemal w każdy rodzaj tkanki. Komórki macierzyste były następnie starannie kierowane do różnicowania w neurony korowe i komórki wspierające, naśladując obszar mózgu zaangażowany w uczenie się, pamięć i zachowanie. Rygorystyczne kontrole jakości wykazały, że zarówno komórki pacjentów, jak i kontroli rosły prawidłowo, miały prawidłowy zestaw chromosomów i potrafiły tworzyć wysokiej jakości progenitory neuronowe. Innymi słowy, późniejsze różnice w aktywności przypominającej mózg raczej nie były spowodowane wadami podstawowego procesu produkcji komórek.
Neurony, które na początku wyglądają i wyładowują się normalnie
Następnie zespół badał morfologię i elektryczne zachowanie pojedynczych neuronów. Dzięki szczegółowemu obrazowaniu odtworzono setki komórek i stwierdzono, że neurony pacjentów i kontrolne miały podobnie złożone rozgałęzienia — co sugeruje, że Sanfilippo nie uniemożliwia tym komórkom budowania bogatej sieci połączeń. Nagrania elektryczne pokazały, że neurony z obu grup generowały potencjały czynnościowe (elektryczne impulsy przenoszące informacje) o porównywalnej sile, szybkości i progach pobudliwości. Kluczowe kanały jonowe odpowiedzialne za generowanie tych impulsów również funkcjonowały prawidłowo. We wczesnym rozwoju neurony z Sanfilippo wyglądały więc podobnie do typowych neuronów i mogły wyładowywać się równie dobrze.
Ukryta nierównowaga między sygnałami „przyspieszającymi” i „hamującymi”
Problemy pojawiły się później, w miarę dojrzewania hodowanych w laboratorium sieci. Zespół mierzył drobne prądy wpływające do neuronów, gdy sąsiednie komórki uwalniały neuroprzekaźniki. W ciągu tygodni neurony z Sanfilippo rozwijały więcej kontaktów pobudzających — synaps wysyłających sygnały „przyspieszające” — co było widoczne jako zwiększone skupiska białka PSD95. Kontakty hamujące, które dostarczają sygnały „stop”, pozostawały w tyle. To spowodowało niezdrowe przechylenie równowagi w stronę pobudzenia. Prądy pobudzające w neuronach pacjentów stały się częstsze i większe, podczas gdy prądy hamujące pozostawały w dużej mierze niezmienione. Gdy naukowcy wprowadzili łagodny stres komórkowy przez krótkotrwałe usunięcie czynników wzrostu i przeciwutleniaczy, ten bias pobudzający w hodowlach pacjentów stał się znacznie bardziej wyraźny, podczas gdy sieci neurotypowe były w dużej mierze niedotknięte.
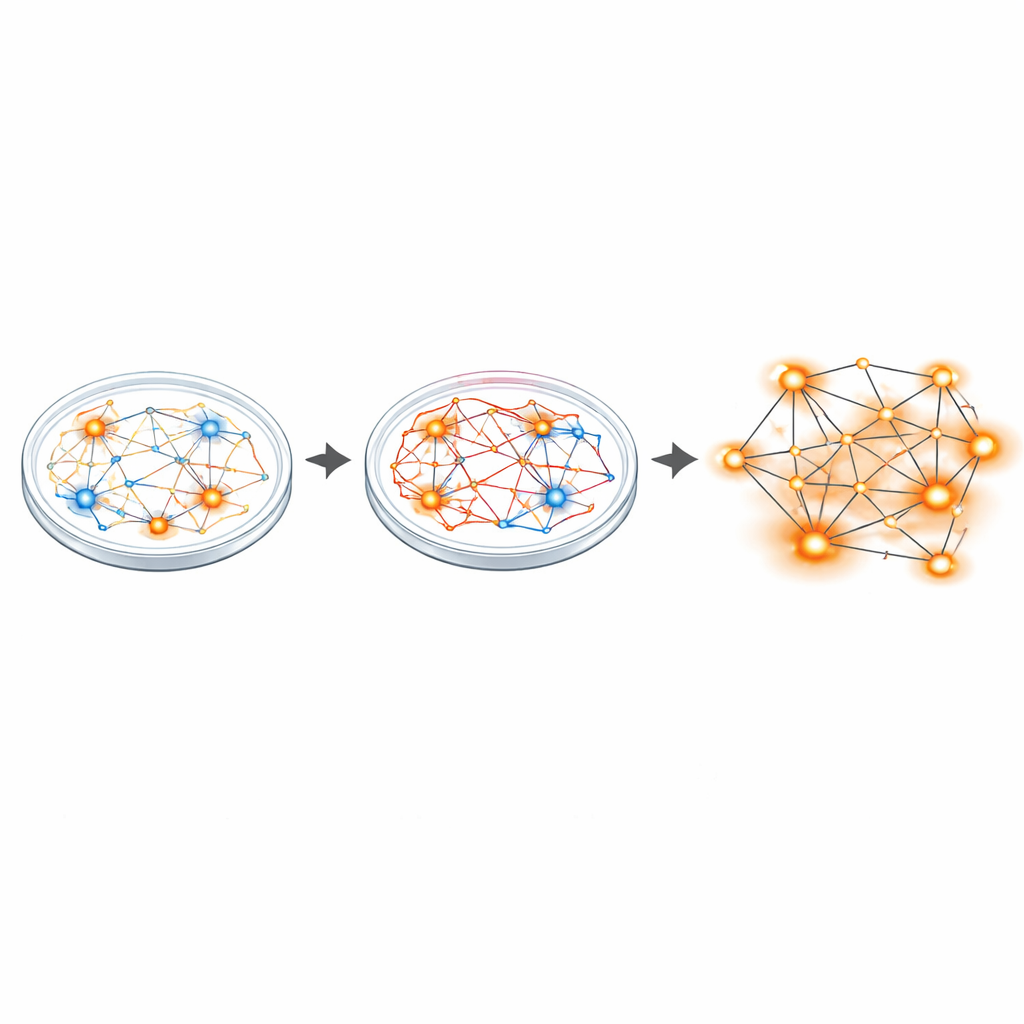
Od nadpobudliwych synaps do hiperaktywnych sieci
Aby zobaczyć, jak ta nierównowaga objawia się na poziomie obwodów, badacze użyli wielielektrodowych matryc — miniaturowych siatek rejestrujących równocześnie wiele neuronów. Podczas gdy pojedyncze neurony pacjentów wystrzeliwały z podobną średnią częstością jak neurony kontrolne, ogólny obraz sieci był inny. Hodowle z Sanfilippo miały więcej aktywnych i pulsujących (burstujących) neuronów oraz wykazywały około dwa razy więcej zsynchronizowanych zdarzeń sieciowych, wzorca skoordynowanego wyładowania wskazującego na hiperaktywne obwody. Sequencing RNA pojedynczych jąder tysięcy komórek ujawnił szerokie przesunięcia w aktywności genów, szczególnie w genach odpowiedzialnych za budowę i wzmacnianie synaps glutamatergicznych (pobudzających). Kilka z tych genów wiązano wcześniej z innymi schorzeniami mózgu charakteryzującymi się nierównowagą między pobudzeniem a hamowaniem, takimi jak autyzm i schizofrenia.
Co to oznacza dla przyszłych terapii
Dla osoby niebędącej specjalistą kluczowy wniosek jest taki, że w tej dziecięcej demencji podstawowe okablowanie neuronów jest w dużej mierze zachowane, lecz z czasem zaburzona zostaje równowaga między „pedałem” a „hamulcem” mózgu. Neurony są nadmiernie napędzane przez sygnały pobudzające, co prowadzi do hiperaktywnych sieci, które mogą stworzyć podłoże dla późniejszej degeneracji i utraty funkcji poznawczych. Ponieważ zespół był w stanie odtworzyć te zmiany in vitro używając komórek pochodzących od pacjentów, ich model stanowi potężną platformę do poszukiwania leków przywracających równowagę między sygnałami pobudzającymi i hamującymi. Takie leczenie nie zastąpi brakującego enzymu powodującego Sanfilippo, ale mogłoby pomóc zachować funkcje poznawcze i zachowanie — potencjalnie poprawiając jakość życia dzieci żyjących z tą wyniszczającą chorobą.
Cytowanie: Mazzachi, P., McDonald, E., Greenberg, Z. et al. Modelling synaptic dysfunction in childhood dementia using human iPSC-derived cortical networks. Nat Commun 17, 3161 (2026). https://doi.org/10.1038/s41467-026-71112-9
Słowa kluczowe: dzicięca demencja, zespół Sanfilippo, nierównowaga synaptyczna, indukowane komórki pluripotentne, nadmierna pobudliwość sieci nerwowych