Clear Sky Science · de
Modellierung synaptischer Funktionsstörungen bei kindlicher Demenz mithilfe humaner iPSC-abgeleiteter kortikaler Netzwerke
Warum diese Forschung für Familien wichtig ist
Kindliche Demenz ist eine verheerende Gruppe von Hirnerkrankungen, bei der Kinder nach und nach Gedächtnis, Denkfähigkeiten und Selbstständigkeit verlieren. Eine der häufigsten Formen, das Sanfilippo-Syndrom Typ A, ist derzeit nicht heilbar und die Behandlungsmöglichkeiten sind begrenzt. Diese Studie nutzt fortgeschrittene Stammzellmethoden, um winzige menschliche Gehirnnetzwerke im Labor zu züchten, sodass Forschende beobachten können, wie Neurone von betroffenen Kindern sich über die Zeit verhalten. Indem gezeigt wird, wie diese Zellen genau fehlgehen, weist die Arbeit auf neue Medikamentenansätze hin, die Denken und Lernen schützen könnten – sogar wenn ein Kind spät diagnostiziert wird.
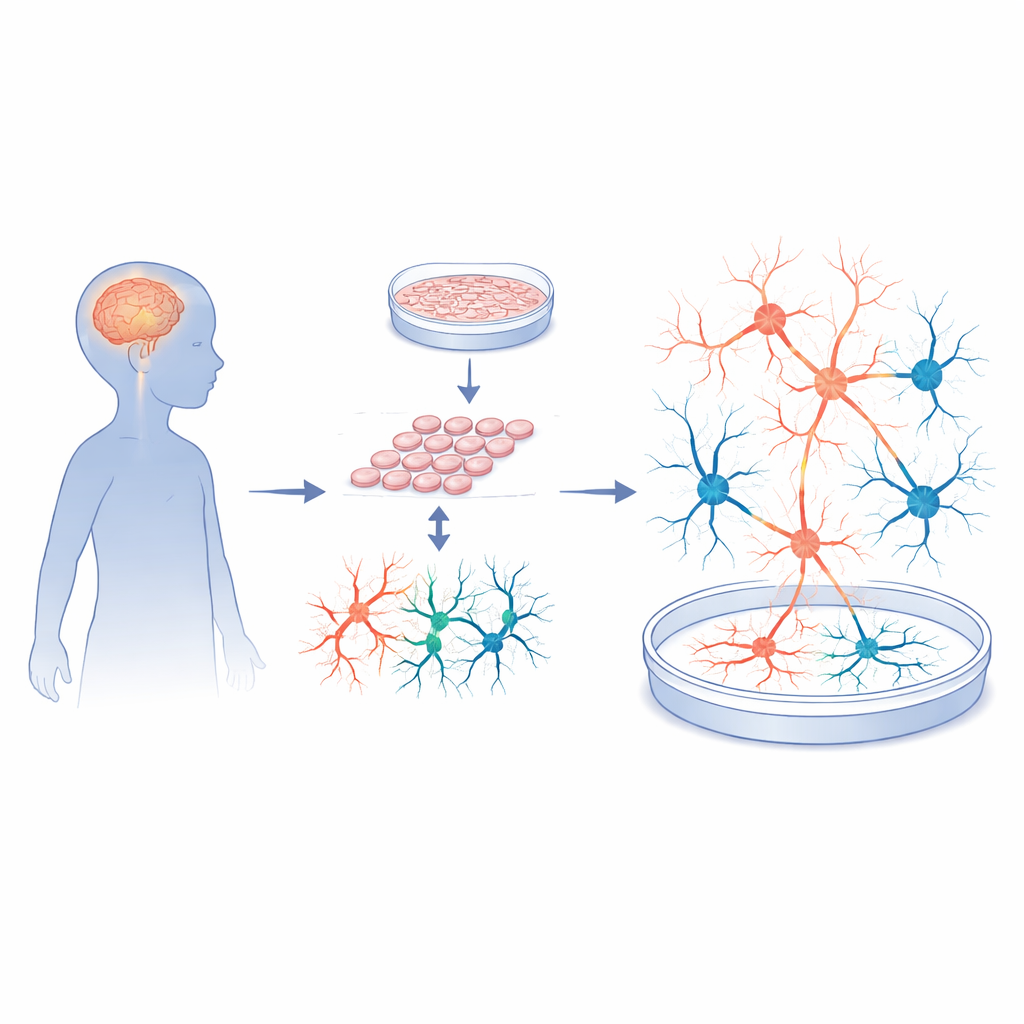
Hautzellen zu funktionierenden Hirnschaltkreisen machen
Die Forschenden begannen mit Hautbiopsien von fünf Kindern mit Sanfilippo Typ A und fünf neurotypischen, altersentsprechenden Spendern. Sie reprogrammierten diese Hautzellen zu induzierten pluripotenten Stammzellen, einem flexiblen Zelltyp, der sich zu fast jedem Gewebe entwickeln kann. Diese Stammzellen wurden dann gezielt zu kortikalen Neuronen und Stützzellen geleitet, um die Gehirnregion nachzubilden, die an Lernen, Gedächtnis und Verhalten beteiligt ist. Gründliche Qualitätskontrollen zeigten, dass sowohl Patienten- als auch Kontrollstammzellen gut wuchsen, normale Chromosomen aufwiesen und hochwertige neuronale Vorläuferzellen bilden konnten. Mit anderen Worten: Etwaige spätere Unterschiede in gehirnähnlicher Aktivität ließen sich kaum auf Fehler im grundlegenden Zellbildungsprozess zurückführen.
Neurone, die anfangs normal aussehen und feuern
Als Nächstes untersuchte das Team Form und elektrische Eigenschaften einzelner Neurone. Mittels detaillierter Bildgebung rekonstruierten sie Hunderte einzelner Zellen und fanden heraus, dass Patienten- und Kontrollneurone ähnlich komplex verzweigte Muster aufwiesen – was darauf hindeutet, dass Sanfilippo diese Zellen nicht daran hindert, ein dichtes Netzwerk von Verbindungen aufzubauen. Elektrische Aufzeichnungen zeigten, dass die Neurone beider Gruppen Aktionspotenziale (die elektrischen Impulse zur Informationsübertragung) mit vergleichbarer Stärke, Geschwindigkeit und Schwelle erzeugten. Wichtige Ionenkanäle, die diese Impulse erzeugen, funktionierten ebenfalls normal. Zu frühen Entwicklungsphasen wirkten Sanfilippo-Neurone demnach weitgehend wie typische Neurone und konnten ebenso gut feuern.
Verborgenes Ungleichgewicht zwischen „Gas“- und „Bremse“-Signalen
Die Probleme traten später auf, als die im Labor gewachsenen Netzwerke reiften. Das Team maß winzige Ströme, die in Neurone fließen, wenn benachbarte Zellen chemische Botenstoffe freisetzen. Im Verlauf von Wochen entwickelten Sanfilippo-Neurone mehr exzitatorische Kontakte – Synapsen, die „Go“-Signale senden – erkennbar an vermehrten Clustern des Proteins PSD95. Inhibitorische Kontakte, die „Stop“-Signale liefern, hinkten dahinter her. Das erzeugte eine ungünstige Verschiebung hin zur Erregung. Die exzitatorischen Ströme in Patientenneuronen wurden häufiger und größer, während die inhibitorischen Ströme weitgehend unverändert blieben. Als die Forschenden milden zellulären Stress einführten, indem sie vorübergehend Wachstumsfaktoren und Antioxidantien entfernten, wurde diese exzitatorische Verzerrung in den Patientenkulturen deutlich stärker ausgeprägt, während neurotypische Netzwerke größtenteils unbeeindruckt blieben.
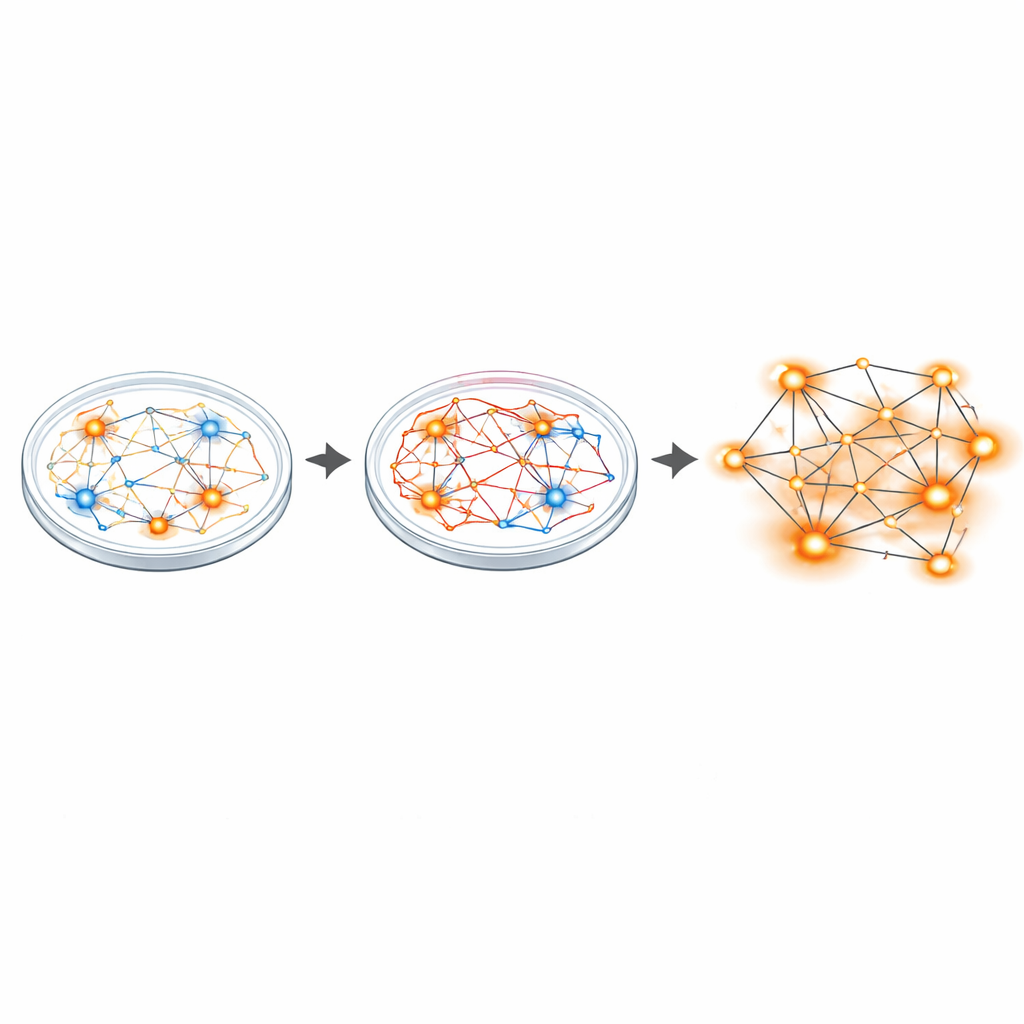
Von übererregten Synapsen zu hyperaktiven Netzwerken
Um zu sehen, wie sich dieses Ungleichgewicht auf Schaltkreisebene auswirkt, nutzten die Forschenden Multielektrodenarrays – winzige Gitter, die von vielen Neuronen gleichzeitig aufzeichnen. Während einzelne Neurone von Patienten mit etwa gleicher mittlerer Rate feuerten wie die Kontrollen, erzählten die Gesamtnetzwerke eine andere Geschichte. Sanfilippo-Kulturen hatten mehr aktive und burstende Neurone und zeigten ungefähr doppelt so viele synchronisierte Netzwerkevents, ein Muster koordinierter Aktivität, das auf hyperaktive Schaltkreise hinweist. Einzelkern-RNA-Sequenzierung von Tausenden Zellen zeigte dann breite Verschiebungen in der Genaktivität, besonders in Genen, die glutamaterge (exzitatorische) Synapsen aufbauen und stärken. Einige dieser Gene wurden bereits mit anderen Gehirnerkrankungen in Verbindung gebracht, die ein Ungleichgewicht von Erregung und Hemmung zeigen, etwa Autismus und Schizophrenie.
Was das für künftige Behandlungen bedeutet
Für Nichtfachleute ist die Kernbotschaft, dass bei dieser kindlichen Demenz die grundlegende Verschaltung von Neuronen weitgehend intakt bleibt, aber das Gleichgewicht zwischen den Beschleunigern und Bremsen des Gehirns sich im Laufe der Zeit verschiebt. Neurone werden durch exzitatorische Eingänge zu stark angetrieben, was zu hyperaktiven Netzwerken führt, die den Boden für spätere Degeneration und den Verlust kognitiver Fähigkeiten bereiten können. Da das Team diese Veränderungen in einer Zellkultur mit patientenabgeleiteten Zellen reproduzieren konnte, bietet ihr Modell eine starke Plattform, um nach Wirkstoffen zu suchen, die das Gleichgewicht zwischen exzitatorischen und inhibitorischen Signalen wiederherstellen. Solche Behandlungen würden nicht das fehlende Enzym ersetzen, das Sanfilippo verursacht, könnten aber Denken und Verhalten schützen – und potenziell die Lebensqualität von Kindern mit dieser verheerenden Krankheit verbessern.
Zitation: Mazzachi, P., McDonald, E., Greenberg, Z. et al. Modelling synaptic dysfunction in childhood dementia using human iPSC-derived cortical networks. Nat Commun 17, 3161 (2026). https://doi.org/10.1038/s41467-026-71112-9
Schlüsselwörter: kindliche Demenz, Sanfilippo-Syndrom, synaptische Dysbalance, induzierte pluripotente Stammzellen, neuronale Netzwerkhyperexzitabilität