Clear Sky Science · pt
Modelando a disfunção sináptica na demência infantil usando redes corticais humanas derivadas de iPSC
Por que esta pesquisa importa para famílias
A demência infantil é um conjunto devastador de doenças cerebrais em que crianças perdem gradualmente memória, habilidades de pensamento e independência. Uma das formas mais comuns, a síndrome de Sanfilippo do tipo A, atualmente não tem cura e oferece opções terapêuticas limitadas. Este estudo utiliza métodos avançados com células-tronco para cultivar pequenas redes cerebrais humanas em laboratório, permitindo aos cientistas observar como os neurônios de crianças afetadas se comportam ao longo do tempo. Ao revelar exatamente como essas células falham, o trabalho aponta para novas estratégias medicamentosas que podem proteger as funções de pensamento e aprendizagem, mesmo quando a criança é diagnosticada tardiamente.
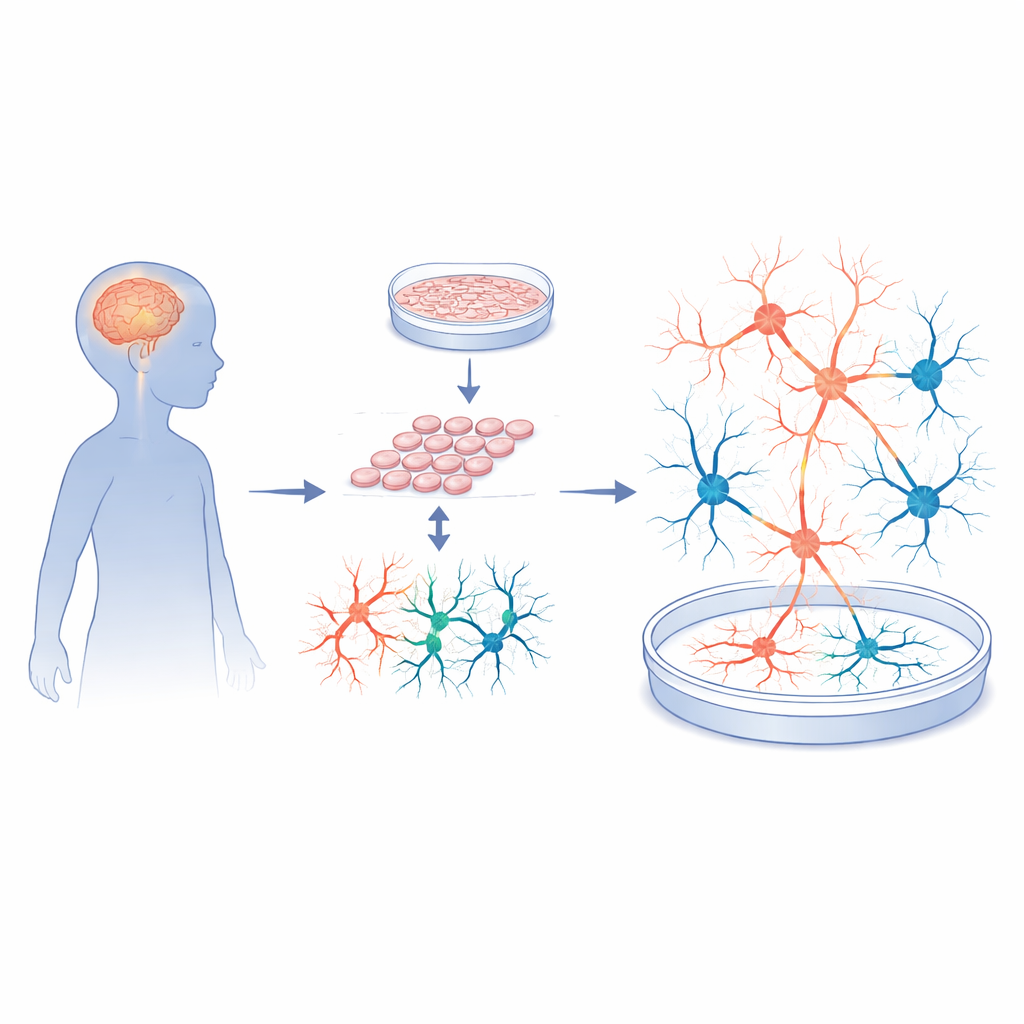
Transformando células da pele em circuitos cerebrais funcionais
Os pesquisadores começaram com biópsias de pele de cinco crianças com Sanfilippo tipo A e cinco doadores neurotípicos pareados por idade. Eles reprogramaram essas células da pele em células-tronco pluripotentes induzidas, um tipo celular flexível que pode se transformar em quase qualquer tecido. Essas células-tronco foram então cuidadosamente dirigidas a se tornarem neurônios corticais e células de suporte, imitando a região do cérebro envolvida em aprendizagem, memória e comportamento. Verificações rigorosas de qualidade mostraram que tanto as células-tronco de pacientes quanto as de controles cresceram bem, apresentaram cromossomos normais e puderam formar progenitores neurais de alta qualidade. Em outras palavras, quaisquer diferenças posteriores na atividade semelhante à cerebral eram pouco prováveis de serem causadas por falhas no processo básico de formação celular.
Neurônios que, a princípio, parecem e disparam normalmente
Em seguida, a equipe examinou a forma e o comportamento elétrico de neurônios individuais. Usando imagens detalhadas, eles reconstruíram centenas de células únicas e descobriram que neurônios de pacientes e controles tinham padrões de ramificação igualmente complexos — sugerindo que Sanfilippo não impede essas células de construir uma rede rica de conexões. Registros elétricos mostraram que os neurônios de ambos os grupos produziram potenciais de ação (os picos elétricos que transmitem informação) com força, velocidade e limiares comparáveis. Canais iônicos-chave que geram esses picos também funcionaram normalmente. No início do desenvolvimento, portanto, os neurônios com Sanfilippo se pareciam muito com neurônios típicos e podiam disparar da mesma forma.
Desequilíbrio oculto entre sinais de “vai” e “pare”
Os problemas surgiram mais tarde, à medida que as redes cultivadas em laboratório amadureceram. A equipe mediu correntes diminutas que fluíam para os neurônios quando células vizinhas liberavam mensageiros químicos. Ao longo de semanas, os neurônios com Sanfilippo desenvolveram mais contatos excitatórios — sinapses que enviam sinais de “vai” — marcados por um aumento nos aglomerados da proteína PSD95. Os contatos inibitórios, que fornecem sinais de “pare”, ficaram para trás. Isso criou uma inclinação prejudicial em direção à excitação. As correntes excitatórias nos neurônios de pacientes tornaram-se mais frequentes e maiores, enquanto as correntes inibitórias permaneceram amplamente inalteradas. Quando os cientistas introduziram um estresse celular leve, removendo brevemente fatores de crescimento e antioxidantes, esse viés excitatório nas culturas de pacientes tornou-se muito mais pronunciado, enquanto as redes neurotípicas foram em grande parte pouco afetadas.
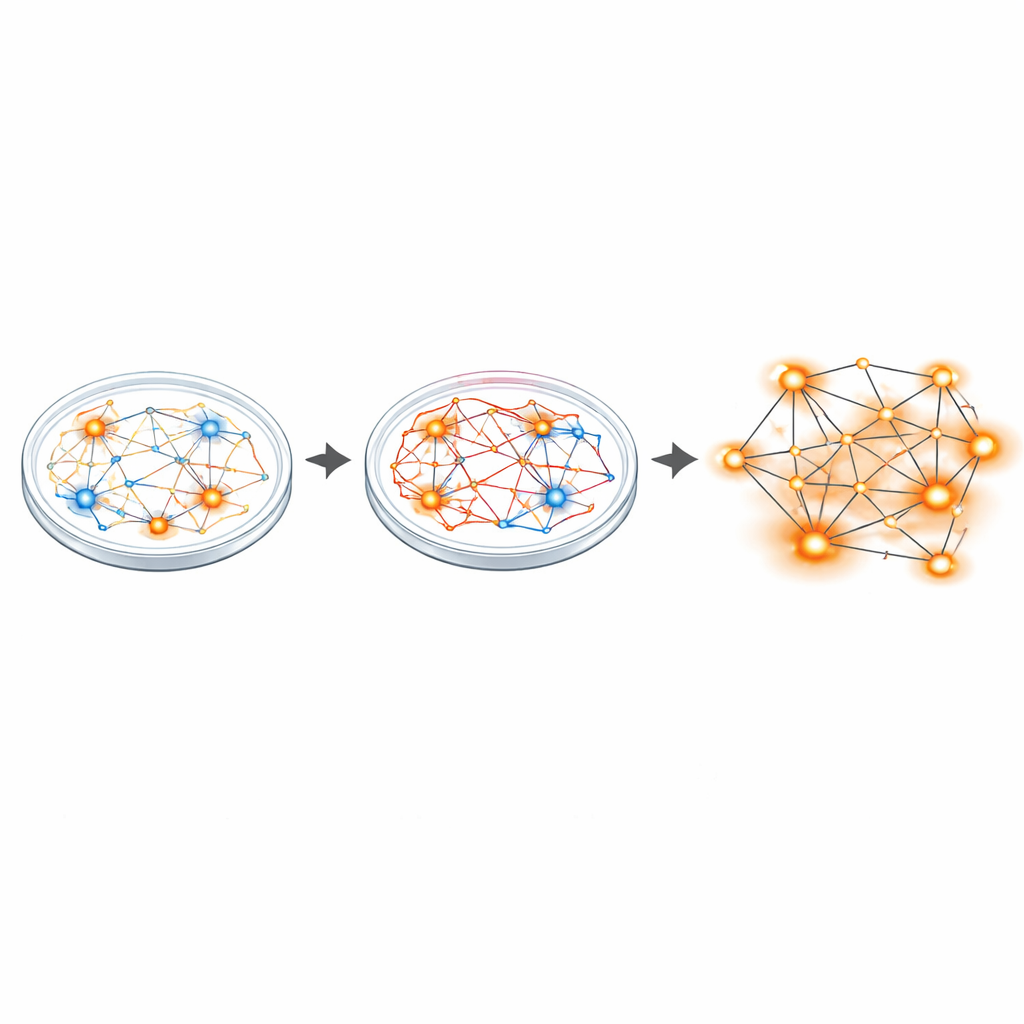
De sinapses hiperexcitadas a redes hiperativas
Para ver como esse desequilíbrio se manifesta ao nível do circuito, os pesquisadores usaram matrizes de multieletrodos — pequenas grades que registram muitos neurônios ao mesmo tempo. Embora neurônios individuais de pacientes disparassem a uma taxa média semelhante à dos controles, as redes como um todo contaram uma história diferente. As culturas de Sanfilippo apresentaram mais neurônios ativos e em rajadas e mostraram aproximadamente o dobro de eventos de rede sincronizados, um padrão de disparo coordenado que sinaliza circuitos hiperativos. O sequenciamento de RNA de núcleo único de milhares de células revelou então mudanças amplas na atividade gênica, especialmente em genes que constroem e fortalecem sinapses glutamatérgicas (excitadoras). Vários desses genes foram ligados a outras condições cerebrais que exibem desequilíbrios entre excitação e inibição, como autismo e esquizofrenia.
O que isso significa para tratamentos futuros
Para um público não especialista, a mensagem principal é que, nessa demência infantil, a fiação básica dos neurônios está em grande parte preservada, mas o equilíbrio entre os aceleradores e freios do cérebro se altera com o tempo. Os neurônios passam a ser excessivamente estimulados por entradas excitatórias, levando a redes hiperativas que podem preparar o terreno para degeneração posterior e perda de capacidades cognitivas. Porque a equipe pôde reproduzir essas alterações em uma placa usando células derivadas de pacientes, seu modelo oferece uma plataforma poderosa para buscar drogas que restaurem o equilíbrio entre sinais excitatórios e inibitórios. Esses tratamentos não substituiriam a enzima faltante que causa Sanfilippo, mas poderiam ajudar a preservar o pensamento e o comportamento — potencialmente melhorando a qualidade de vida de crianças que vivem com essa doença devastadora.
Citação: Mazzachi, P., McDonald, E., Greenberg, Z. et al. Modelling synaptic dysfunction in childhood dementia using human iPSC-derived cortical networks. Nat Commun 17, 3161 (2026). https://doi.org/10.1038/s41467-026-71112-9
Palavras-chave: demência infantil, síndrome de Sanfilippo, desequilíbrio sináptico, células-tronco pluripotentes induzidas, hiperexcitabilidade de redes neurais