Clear Sky Science · fr
Modélisation des dysfonctionnements synaptiques dans la démence infantile à l’aide de réseaux corticaux dérivés de cellules iPSC humaines
Pourquoi cette recherche compte pour les familles
La démence infantile regroupe des maladies cérébrales dévastatrices dans lesquelles les enfants perdent progressivement la mémoire, les capacités cognitives et leur autonomie. L’une des formes les plus fréquentes, le syndrome de Sanfilippo de type A, n’a actuellement ni remède ni options thérapeutiques étendues. Cette étude utilise des techniques avancées de cellules souches pour faire croître en laboratoire de petits réseaux cérébraux humains, permettant aux scientifiques d’observer le comportement des neurones issus d’enfants atteints au fil du temps. En révélant précisément comment ces cellules dysfonctionnent, le travail ouvre la voie à de nouvelles stratégies médicamenteuses susceptibles de protéger la pensée et l’apprentissage, même lorsqu’un enfant est diagnostiqué tardivement.
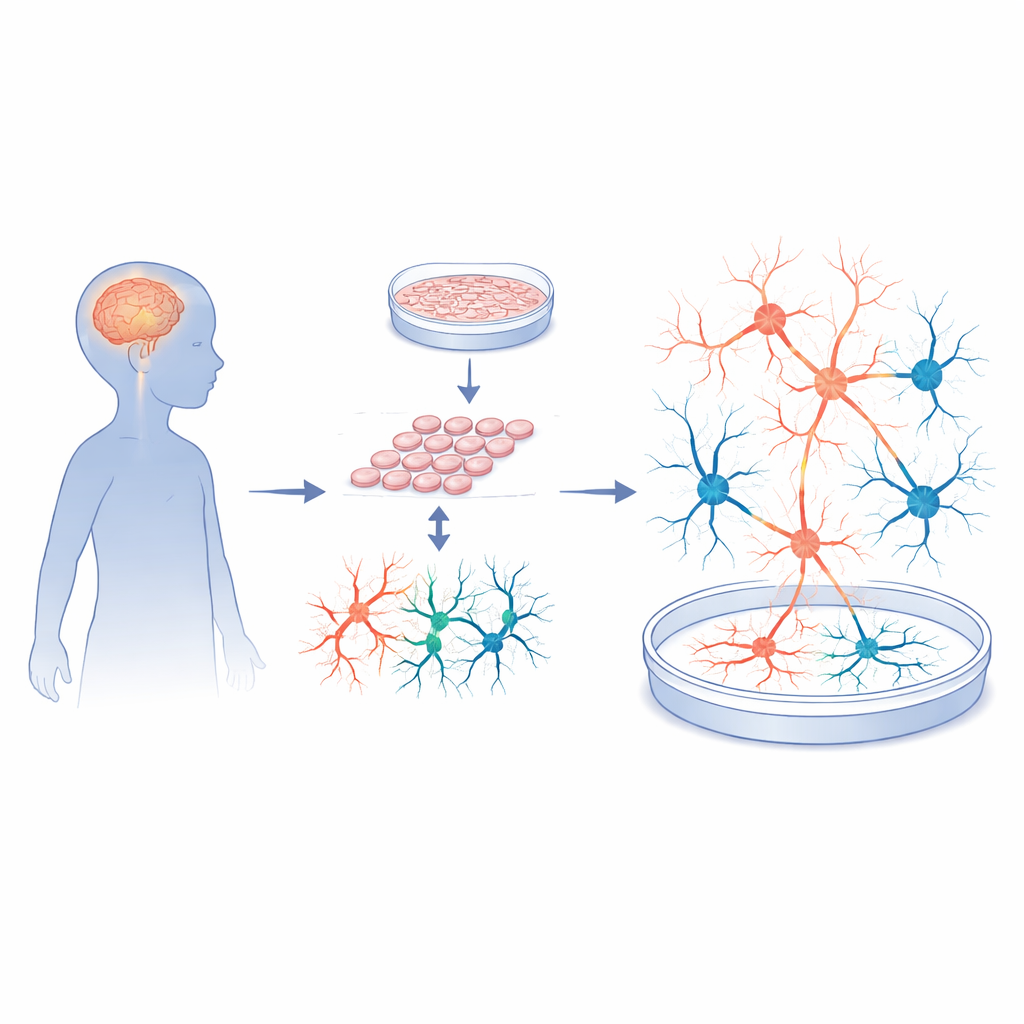
Transformer des cellules de peau en circuits cérébraux fonctionnels
Les chercheurs ont commencé par des biopsies cutanées de cinq enfants atteints du syndrome de Sanfilippo de type A et de cinq donneurs neurotypiques appariés sur l’âge. Ils ont reprogrammés ces cellules de peau en cellules souches pluripotentes induites, un type cellulaire flexible pouvant devenir presque n’importe quel tissu. Ces cellules souches ont ensuite été guidées avec soin pour devenir des neurones corticaux et des cellules de soutien, imitant la région du cerveau impliquée dans l’apprentissage, la mémoire et le comportement. Des contrôles qualité rigoureux ont montré que les cellules souches des patients et des témoins se développaient bien, présentaient des chromosomes normaux et pouvaient former des progéniteurs neuronaux de haute qualité. En d’autres termes, les différences ultérieures dans l’activité de type cérébral étaient peu susceptibles d’être causées par des défauts dans le processus de création cellulaire de base.
Des neurones qui paraissent et tirent normalement au départ
Ensuite, l’équipe a examiné la morphologie et le comportement électrique de neurones individuels. À l’aide d’imagerie détaillée, ils ont reconstruit des centaines de cellules uniques et constaté que les neurones des patients et des témoins présentaient des motifs de branchement d’égale complexité—ce qui suggère que le Sanfilippo n’empêche pas ces cellules de construire un réseau riche de connexions. Les enregistrements électriques ont montré que les neurones des deux groupes produisaient des potentiels d’action (les pointes électriques qui véhiculent l’information) avec une intensité, une vitesse et des seuils comparables. Les canaux ioniques clés générant ces pointes fonctionnaient également normalement. Au début du développement, donc, les neurones Sanfilippo ressemblaient beaucoup à des neurones typiques et pouvaient tirer tout aussi bien.
Déséquilibre caché entre signaux « aller » et « arrêt »
Les problèmes sont apparus plus tard, à mesure que les réseaux cultivés en laboratoire mûrissaient. L’équipe a mesuré de faibles courants entrant dans les neurones lorsque les cellules voisines libéraient des messagers chimiques. Au fil des semaines, les neurones Sanfilippo ont développé davantage de contacts excitateurs—des synapses qui envoient des signaux « aller »—marqués par une augmentation des agrégats de la protéine PSD95. Les contacts inhibiteurs, qui fournissent des signaux « arrêt », ont pris du retard. Cela a créé une inclinaison malsaine en faveur de l’excitation. Les courants excitateurs dans les neurones des patients sont devenus plus fréquents et plus importants, tandis que les courants inhibiteurs sont restés en grande partie inchangés. Lorsque les scientifiques ont introduit un stress cellulaire léger en retirant brièvement facteurs de croissance et antioxydants, ce biais exciteur dans les cultures de patients s’est considérablement accentué, alors que les réseaux neurotypiques ont été largement épargnés.
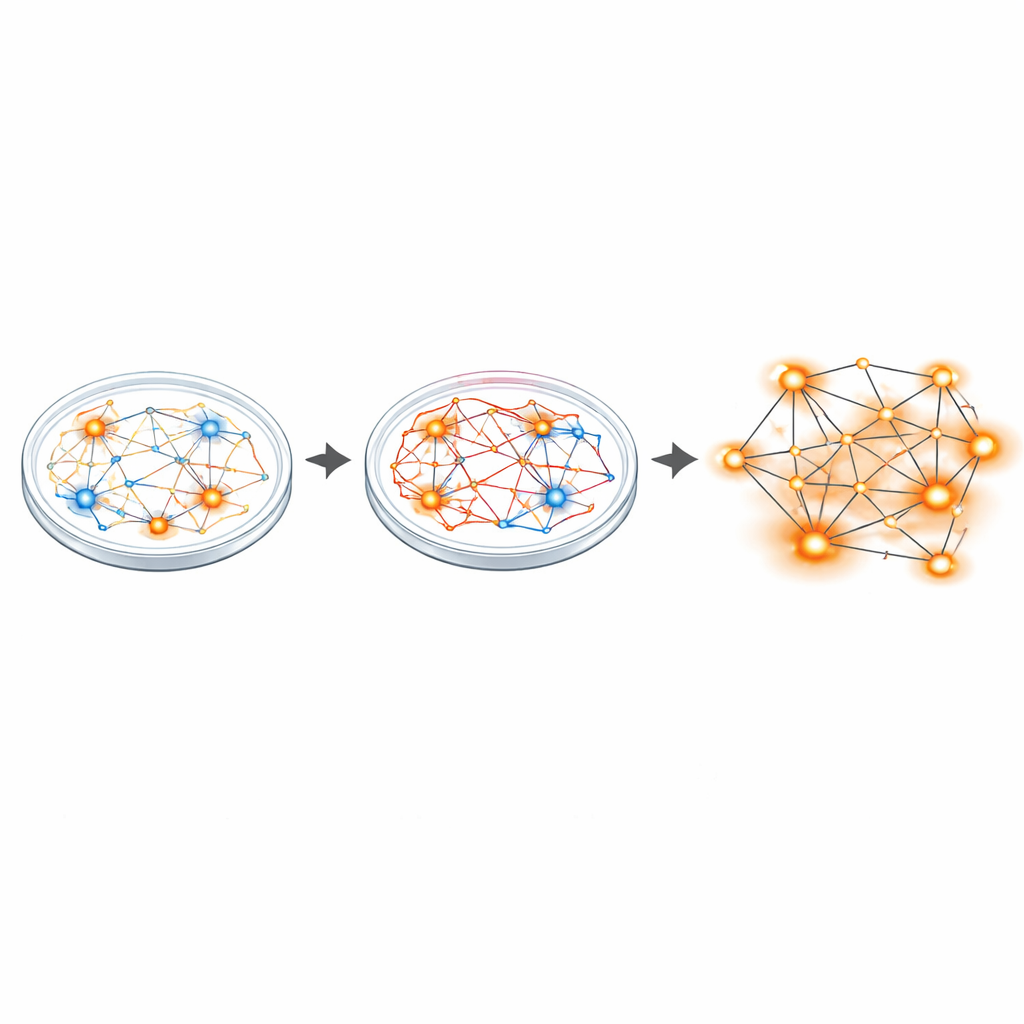
Dés de synapses suractivées à réseaux hyperactifs
Pour voir comment ce déséquilibre se manifeste au niveau du circuit, les chercheurs ont utilisé des réseaux multielectrodes—de minuscules grilles enregistrant de nombreux neurones simultanément. Alors que les neurones isolés des patients tiraient à peu près au même rythme moyen que ceux des témoins, les réseaux dans leur ensemble racontaient une histoire différente. Les cultures Sanfilippo comportaient davantage de neurones actifs et à bouffées d’activité et présentaient environ deux fois plus d’événements synchronisés au niveau du réseau, un schéma de décharge coordonnée qui signale des circuits hyperactifs. Le séquençage ARN d’un seul noyau de milliers de cellules a ensuite révélé de larges changements dans l’activité génique, en particulier dans des gènes qui construisent et renforcent les synapses glutamatergiques (excitatrices). Plusieurs de ces gènes ont été associés à d’autres troubles cérébraux caractérisés par des déséquilibres entre excitation et inhibition, tels que l’autisme et la schizophrénie.
Ce que cela signifie pour les traitements futurs
Pour un non-spécialiste, le message clé est que dans cette démence infantile, le câblage de base des neurones reste en grande partie intact, mais l’équilibre entre les accélérateurs et les freins du cerveau se dérègle avec le temps. Les neurones sont trop stimulés par des entrées excitatrices, conduisant à des réseaux hyperactifs qui peuvent préparer le terrain pour une dégénérescence ultérieure et une perte des capacités cognitives. Parce que l’équipe a pu reproduire ces changements en culture à partir de cellules de patients, leur modèle offre une plateforme puissante pour rechercher des médicaments visant à rétablir l’équilibre entre signaux excitateurs et inhibiteurs. De tels traitements ne remplaceraient pas l’enzyme manquante à l’origine du Sanfilippo, mais ils pourraient aider à préserver la pensée et le comportement—améliorant potentiellement la qualité de vie des enfants concernés par cette maladie dévastatrice.
Citation: Mazzachi, P., McDonald, E., Greenberg, Z. et al. Modelling synaptic dysfunction in childhood dementia using human iPSC-derived cortical networks. Nat Commun 17, 3161 (2026). https://doi.org/10.1038/s41467-026-71112-9
Mots-clés: démence infantile, syndrome de Sanfilippo, déséquilibre synaptique, cellules souches pluripotentes induites, hyperexcitabilité des réseaux neuronaux