Clear Sky Science · it
Modellare la disfunzione sinaptica nella demenza infantile usando reti corticali umane derivate da iPSC
Perché questa ricerca conta per le famiglie
La demenza infantile è un gruppo devastante di malattie cerebrali in cui i bambini perdono gradualmente memoria, capacità di pensiero e autonomia. Una delle forme più comuni, la sindrome di Sanfilippo di tipo A, attualmente non ha cura e offre opzioni terapeutiche limitate. Questo studio utilizza avanzate tecniche con cellule staminali per coltivare in laboratorio piccole reti cerebrali umane, permettendo agli scienziati di osservare come i neuroni provenienti da bambini affetti si comportano nel tempo. Rivelando esattamente come queste cellule si alterano, il lavoro indica nuove strategie farmacologiche che potrebbero proteggere il pensiero e l’apprendimento, anche se la diagnosi avviene in fase avanzata.
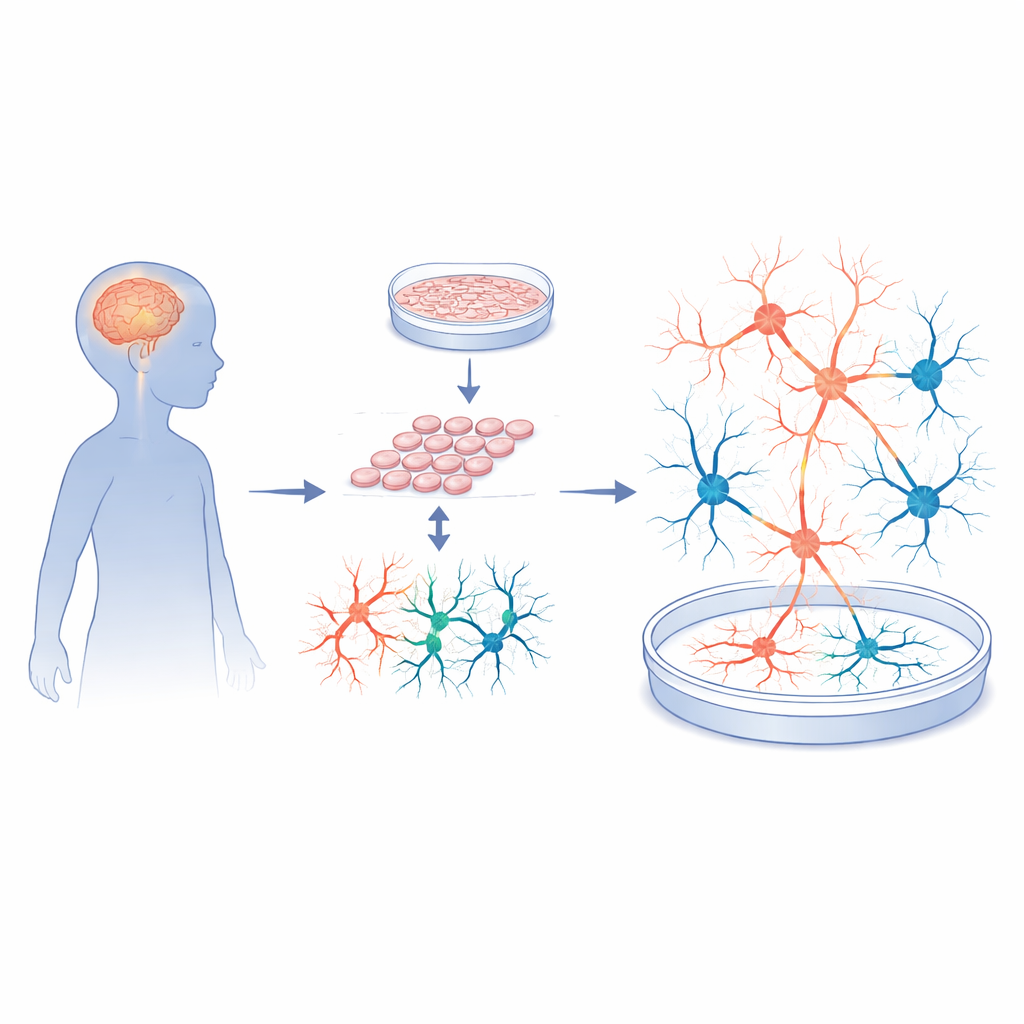
Trasformare cellule della pelle in circuiti cerebrali funzionanti
I ricercatori hanno iniziato con biopsie cutanee di cinque bambini con Sanfilippo di tipo A e cinque donatori neurotipici di età corrispondente. Hanno riprogrammato queste cellule della pelle in cellule staminali pluripotenti indotte, un tipo cellulare flessibile che può diventare quasi qualsiasi tessuto. Queste cellule staminali sono state poi guidate con cura a differenziarsi in neuroni corticali e cellule di supporto, imitando la regione del cervello coinvolta nell’apprendimento, nella memoria e nel comportamento. Controlli di qualità rigorosi hanno mostrato che sia le cellule staminali dei pazienti sia quelle dei controlli crescevano bene, avevano cromosomi normali e potevano formare progenitori neurali di alta qualità. In altre parole, eventuali differenze successive nell’attività simile a quella cerebrale erano improbabili da attribuire a errori nel processo di generazione cellulare di base.
Neuroni che all’inizio sembrano morfologicamente ed elettricamente normali
Successivamente il team ha esaminato la forma e il comportamento elettrico di singoli neuroni. Utilizzando immagini dettagliate, hanno ricostruito centinaia di singole cellule e hanno rilevato che neuroni di pazienti e controlli avevano pattern di ramificazione altrettanto complessi—suggerendo che la sindrome di Sanfilippo non impedisce a queste cellule di costruire una rete ricca di connessioni. Registrazioni elettriche hanno mostrato che i neuroni di entrambi i gruppi generavano potenziali d’azione (le scariche elettriche che trasmettono informazioni) con forza, velocità e soglie comparabili. I canali ionici chiave che generano queste scariche funzionavano anch’essi normalmente. Nelle fasi iniziali dello sviluppo, dunque, i neuroni di Sanfilippo assomigliavano molto a neuroni tipici e potevano scaricare altrettanto bene.
Uno squilibrio nascosto tra segnali “vai” e “fermati”
I problemi sono emersi più tardi, con la maturazione delle reti coltivate in laboratorio. Il team ha misurato piccole correnti che entravano nei neuroni quando le cellule vicine rilasciavano messaggeri chimici. Nel corso delle settimane, i neuroni di Sanfilippo hanno sviluppato più contatti eccitatori—sinapsi che inviano segnali “vai”—contrassegnati da un aumento degli ammassi della proteina PSD95. I contatti inibitori, che forniscono segnali “fermati”, sono rimasti indietro. Questo ha creato un’inclinazione malsana verso l’eccitazione. Le correnti eccitatorie nei neuroni dei pazienti sono diventate più frequenti e più grandi, mentre le correnti inibitorie sono rimaste in gran parte invariate. Quando gli scienziati hanno introdotto un lieve stress cellulare rimuovendo brevemente fattori di crescita e antiossidanti, questo bias eccitatorio nelle colture dei pazienti è diventato molto più pronunciato, mentre le reti neurotipiche sono rimaste per lo più invariate.
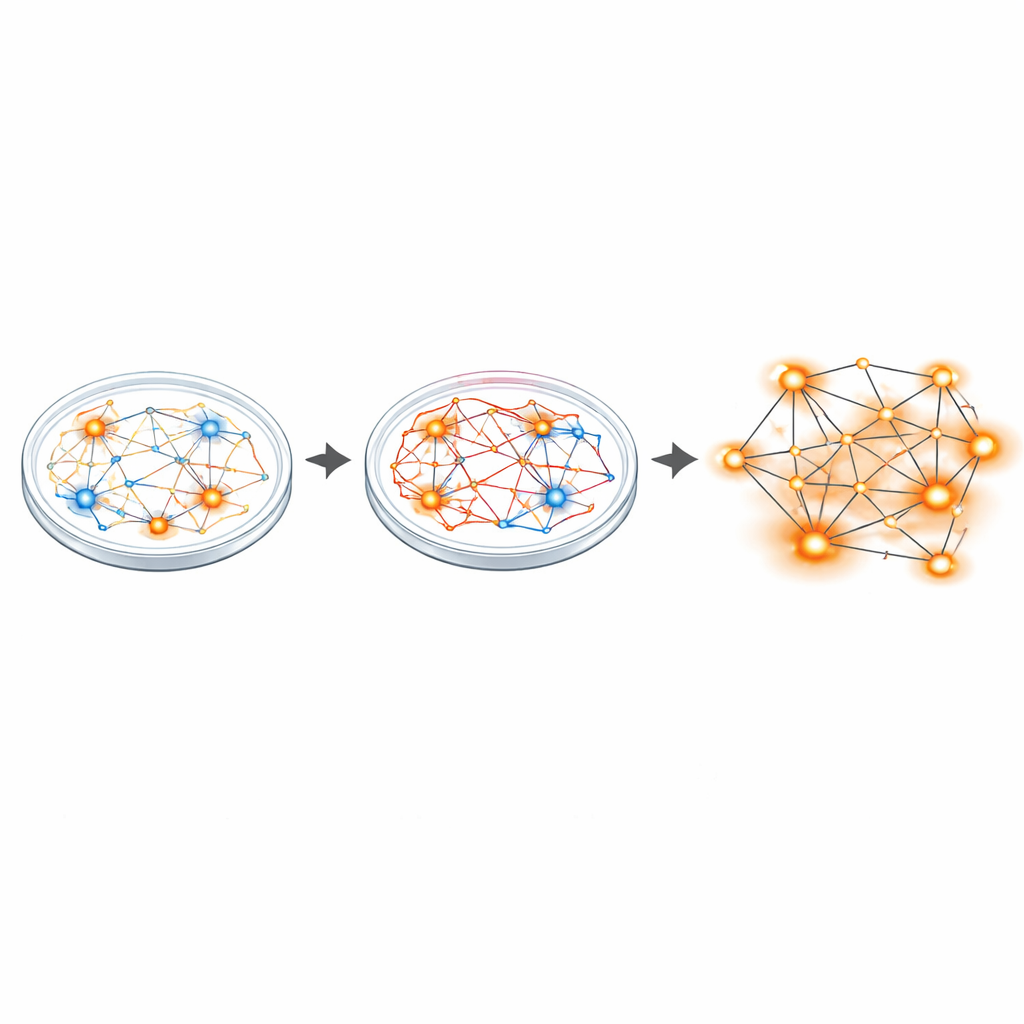
Dalle sinapsi ipereccitate a reti iperattive
Per osservare come questo squilibrio si manifesta a livello di circuito, i ricercatori hanno usato array a multielettrodo—piccole griglie che registrano molti neuroni contemporaneamente. Pur essendo i singoli neuroni dei pazienti scaricati a un tasso medio simile a quello dei controlli, la storia delle reti complessive era diversa. Le colture di Sanfilippo avevano più neuroni attivi e in bursting e mostravano all’incirca il doppio degli eventi di rete sincronizzati, un pattern di scariche coordinate che segnala circuiti iperattivi. L’analisi di RNA a singolo nucleo su migliaia di cellule ha poi rivelato ampi spostamenti nell’attività genica, specialmente nei geni che costruiscono e rafforzano le sinapsi glutamatergiche (eccitatorie). Diversi di questi geni sono stati collegati ad altre condizioni cerebrali caratterizzate da squilibri tra eccitazione e inibizione, come l’autismo e la schizofrenia.
Cosa significa per i trattamenti futuri
Per un non specialista, il messaggio chiave è che in questa demenza infantile il cablaggio di base dei neuroni è in gran parte intatto, ma l’equilibrio tra acceleratori e freni del cervello si altera nel tempo. I neuroni diventano sovraffollati dall’input eccitatorio, provocando reti iperattive che possono predisporre a successiva degenerazione e perdita delle capacità cognitive. Poiché il team è riuscito a riprodurre questi cambiamenti in coltura usando cellule derivate dai pazienti, il loro modello offre una piattaforma potente per cercare farmaci che ripristinino l’equilibrio tra segnali eccitatori e inibitori. Tali terapie non sostituirebbero l’enzima mancante che causa la sindrome di Sanfilippo, ma potrebbero aiutare a preservare il pensiero e il comportamento—migliorando potenzialmente la qualità della vita dei bambini che vivono con questa malattia devastante.
Citazione: Mazzachi, P., McDonald, E., Greenberg, Z. et al. Modelling synaptic dysfunction in childhood dementia using human iPSC-derived cortical networks. Nat Commun 17, 3161 (2026). https://doi.org/10.1038/s41467-026-71112-9
Parole chiave: demenza infantile, sindrome di Sanfilippo, squilibrio sinaptico, cellule staminali pluripotenti indotte, iper-eccitabilità delle reti neurali