Clear Sky Science · sv
Modellering av synaptisk dysfunktion vid barndomsdemens med humana iPSC-deriverade kortikala nätverk
Varför denna forskning är viktig för familjer
Barndomsdemens är en förödande grupp hjärnsjukdomar där barn gradvis förlorar minne, tänkande och självständighet. En av de vanligaste formerna, Sanfilippo‑syndrom typ A, har i nuläget ingen bot och få behandlingsalternativ. Denna studie använder avancerade stamcellsmetoder för att odla små mänskliga hjärnnätverk i labb, vilket gör det möjligt för forskare att följa hur neuroner från drabbade barn beter sig över tid. Genom att visa exakt hur dessa celler går fel pekar arbetet på nya läkemedelsstrategier som kan skydda tanke- och inlärningsförmåga, även om ett barn diagnostiseras sent.
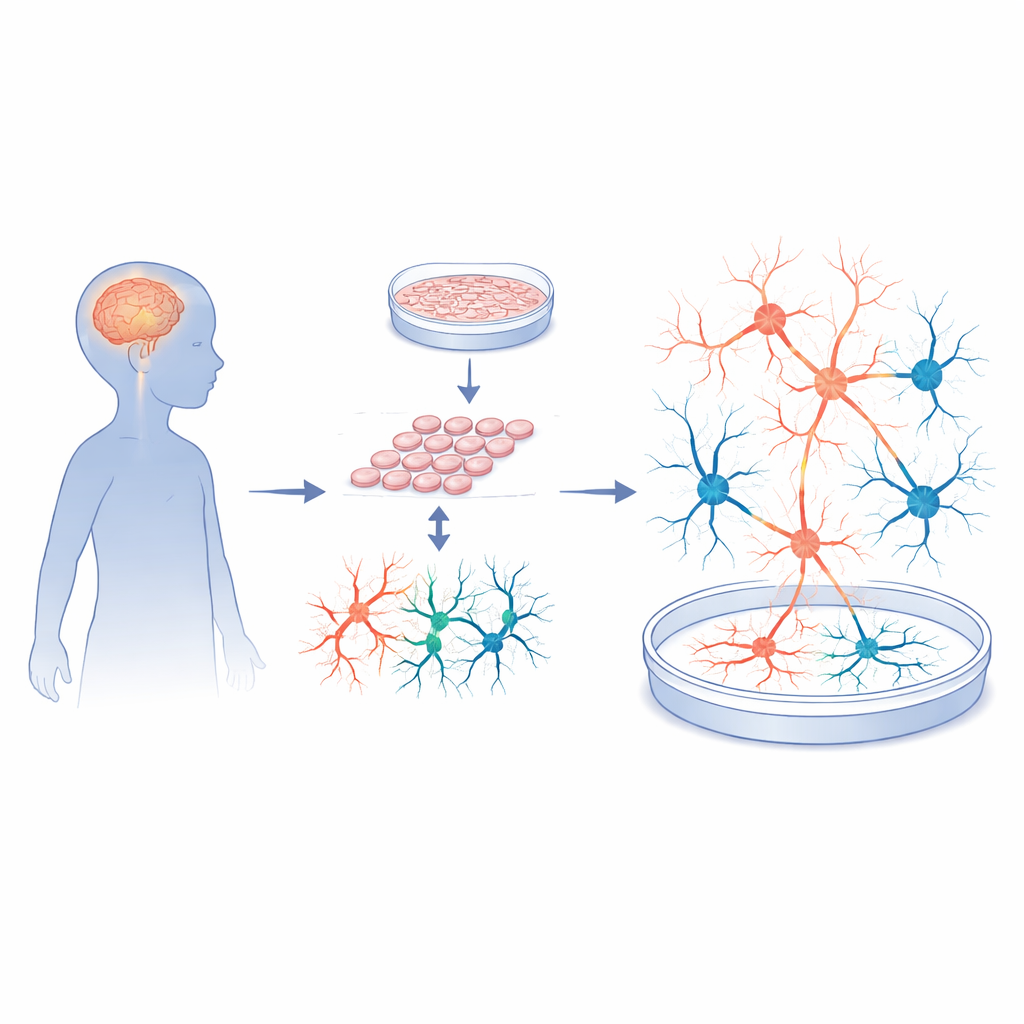
Att förvandla hudceller till fungerande hjärnkretsar
Forskarna började med hudbiopsier från fem barn med Sanfilippo typ A och fem neurotypiska, åldersmatchade givare. De omprogrammerade dessa hudceller till inducerade pluripotenta stamceller, en flexibel celltyp som kan bli nästan vilken vävnad som helst. Dessa stamceller vägleddes sedan noggrant att bli kortikala neuroner och stödjeceller, vilket efterliknar den del av hjärnan som är involverad i lärande, minne och beteende. Strikta kvalitetskontroller visade att både patient- och kontrollstamceller växte väl, hade normala kromosomer och kunde bilda högkvalitativa neurala progenitorceller. Med andra ord var senare skillnader i hjärnlik aktivitet osannolika att bero på brister i den grundläggande cellbildningsprocessen.
Neuroner som först ser normala ut och avfyrar som vanligt
Nästa steg var att undersöka formen och den elektriska beteendet hos enskilda neuroner. Med detaljerad avbildning rekonstruerade de hundratals enskilda celler och fann att patient- och kontrollneuroner hade liknande komplexa förgreningsmönster — vilket tyder på att Sanfilippo inte hindrar dessa celler från att bygga ett rikt nätverk av kontakter. Elektriska inspelningar visade att neuroner från båda grupperna genererade aktionspotentialer (de elektriska spikarna som förmedlar information) med jämförbar styrka, hastighet och tröskelvärden. Nyckeljonkanaler som skapar dessa spikar fungerade också normalt. Tidigt i utvecklingen såg Sanfilippo‑neuroner alltså mycket ut som typiska neuroner och kunde avfyra lika väl.
En dold obalans mellan "gasa"- och "bromsa"-signaler
Problemen visade sig senare, när de labbodlade nätverken mognade. Teamet mätte mycket små strömmar in i neuroner när grannceller släppte ut kemiska budbärare. Över veckor utvecklade Sanfilippo‑neuroner fler excitatoriska kontakter — synapser som skickar "gasa"-signaler — markerade av ökade kluster av proteinet PSD95. Inhibitoriska kontakter, som ger "bromsa"-signaler, kom efter. Detta skapade en ohälsosam lutning mot excitation. De excitatoriska strömmarna i patientneuroner blev både oftare förekommande och större, medan de inhibitoriska strömmarna förblev i stort sett oförändrade. När forskarna introducerade mild cellulär stress genom att kort ta bort tillväxtfaktorer och antioxidanter förvärrades denna excitatoriska snedvridning i patientkulturerna kraftigt, medan de neurotypiska nätsverken till stor del var opåverkade.
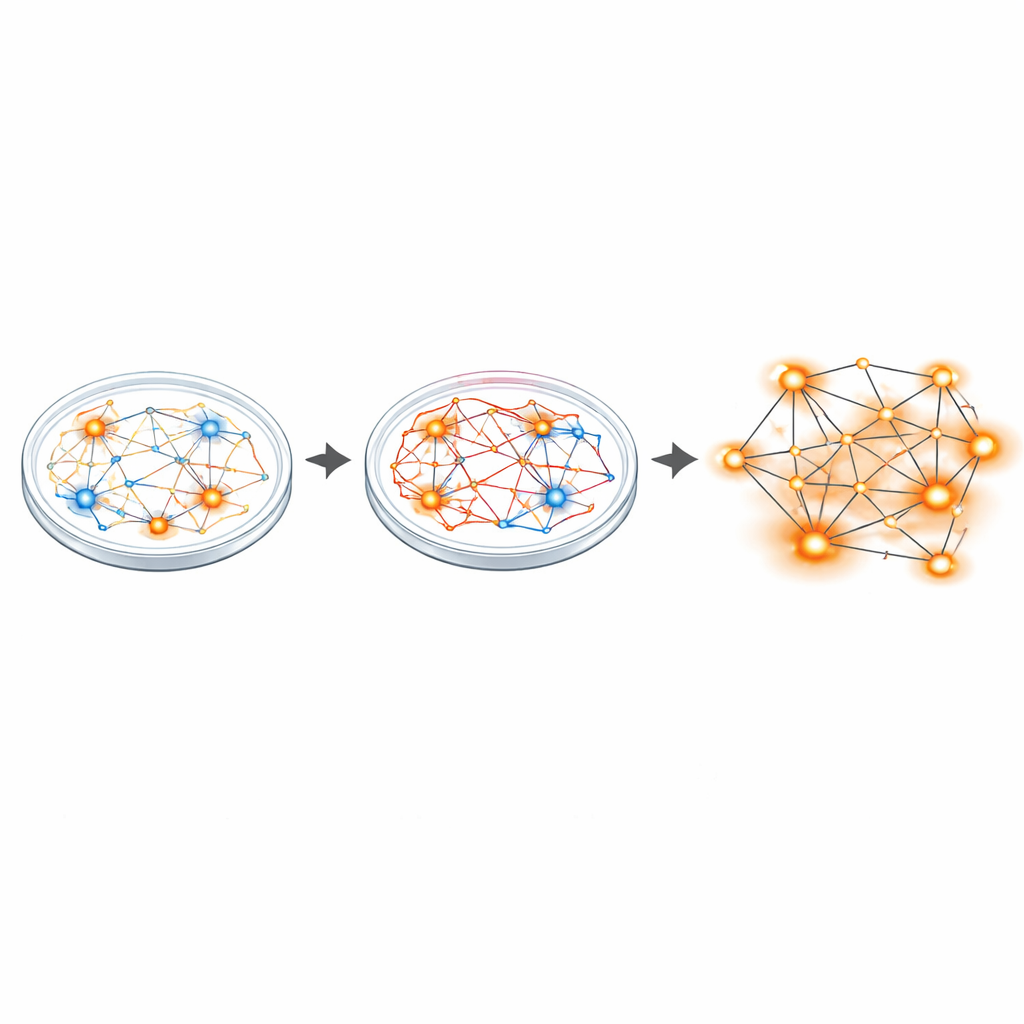
Från överexciterade synapser till hyperaktiva nätverk
För att se hur denna obalans yttrade sig på kretsnivå använde forskarna multielektrodarrays — små gitter som spelar in från många neuroner samtidigt. Medan enskilda neuroner från patienter avfyrade i ungefär samma genomsnittliga takt som kontrollerna, berättade nätverken en annan historia. Sanfilippo‑kulturer hade fler aktiva och burstande neuroner och visade ungefär dubbelt så många synkroniserade nätverkshändelser, ett mönster av koordinerad avfyrning som indikerar hyperaktiva kretsar. Single‑nucleus RNA‑sekvensering av tusentals celler avslöjade sedan breda skift i genaktivitet, särskilt i gener som bygger och stärker glutamatergiska (excitatoriska) synapser. Flera av dessa gener har kopplats till andra hjärntillstånd som kännetecknas av obalanser mellan excitation och inhibition, såsom autism och schizofreni.
Vad detta betyder för framtida behandlingar
För den icke‑specialistiska läsaren är huvudbudskapet att vid denna barndomsdemens är den grundläggande kopplingsarkitekturen hos neuroner till stor del intakt, men balansen mellan hjärnans gaspedal och broms går fel över tid. Neuroner drivs för hårt av excitatorisk input, vilket leder till hyperaktiva nätverk som kan bana väg för senare degeneration och förlust av kognitiva förmågor. Eftersom teamet kunde återskapa dessa förändringar i en skål med patient‑deriverade celler erbjuder deras modell en kraftfull plattform för att söka läkemedel som återställer balansen mellan excitatoriska och inhibitoriska signaler. Sådana behandlingar skulle inte ersätta det saknade enzymet som orsakar Sanfilippo, men de skulle kunna hjälpa till att bevara tänkande och beteende — potentiellt förbättra livskvaliteten för barn som lever med denna förödande sjukdom.
Citering: Mazzachi, P., McDonald, E., Greenberg, Z. et al. Modelling synaptic dysfunction in childhood dementia using human iPSC-derived cortical networks. Nat Commun 17, 3161 (2026). https://doi.org/10.1038/s41467-026-71112-9
Nyckelord: barndomsdemens, Sanfilippo‑syndrom, synaptisk obalans, inducerade pluripotenta stamceller, neuralt nätverks hyperexcitabilitet