Clear Sky Science · ru
Моделирование синаптической дисфункции при детской деменции с использованием кортикальных сетей, полученных из человеческих iPSC
Почему это исследование важно для семей
Детская деменция — сокрушительная группа заболеваний мозга, при которых дети постепенно теряют память, мыслительные способности и самостоятельность. Одна из самых распространённых форм, синдром Санфилиппо типа A, в настоящее время не имеет лечения и ограничена в терапевтических опциях. В этом исследовании применяются передовые методы со стволовыми клетками для выращивания крошечных человеческих мозговых сетей в лаборатории, что позволяет учёным наблюдать за поведением нейронов, полученных от больных детей, с течением времени. Точная реконструкция способов, которыми эти клетки дают сбой, указывает на новые лекарственные стратегии, которые могли бы защитить мышление и обучение, даже если ребёнок был диагностирован поздно.
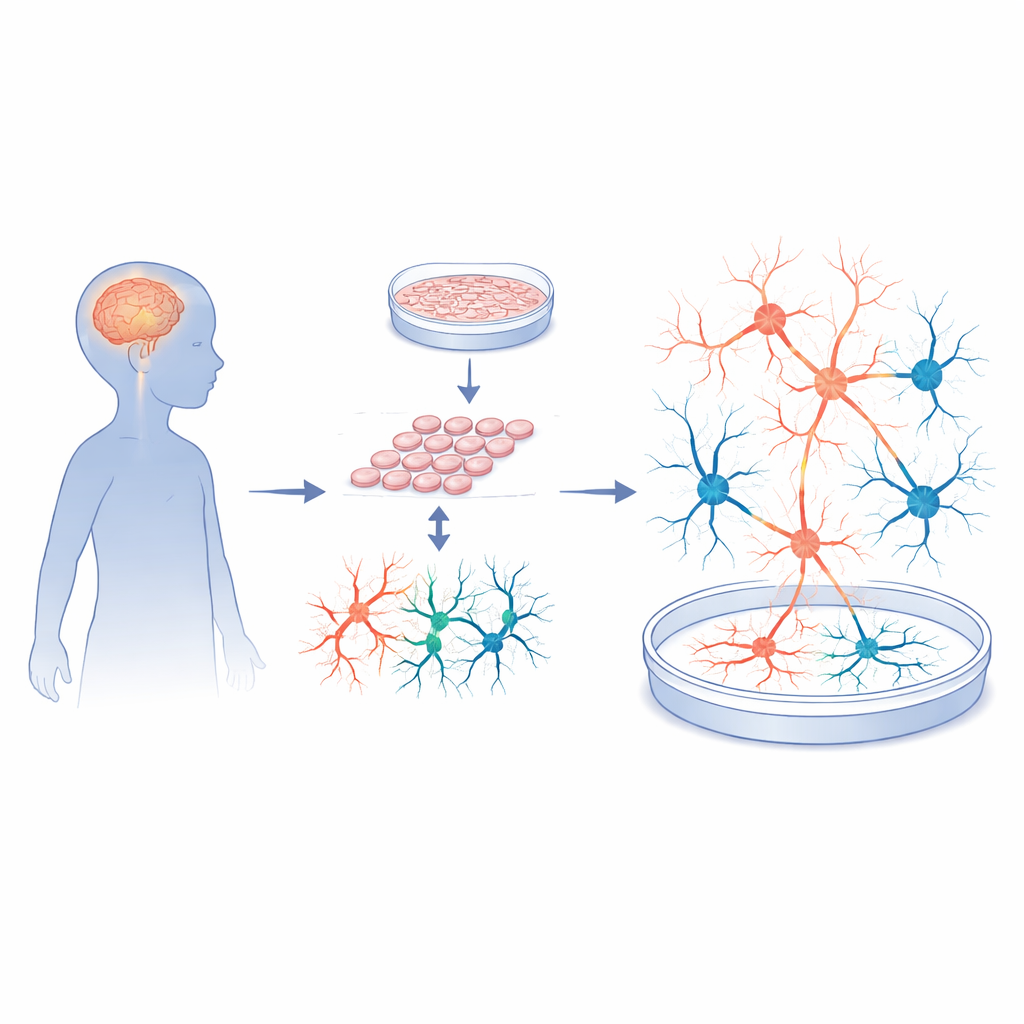
Преобразование клеток кожи в рабочие мозговые цепи
Исследователи начали с кожных биопсий пятерых детей с синдромом Санфилиппо типа A и пятерых нейротипичных доноров сопоставимого возраста. Они перепрограммировали эти клетки кожи в индуцированные плюрипотентные стволовые клетки — гибкий тип клеток, способный превращаться практически в любую ткань. Затем эти стволовые клетки целенаправленно направляли в корковые нейроны и поддерживающие клетки, имитируя участок мозга, ответственный за обучение, память и поведение. Строгие проверки качества показали, что и клетки пациентов, и контрольные клетки хорошо размножались, имели нормальные хромосомы и могли формировать высококачественные нейральные прогениторы. Иными словами, последующие различия в активности, похожей на мозговую, вряд ли были обусловлены дефектами в базовом процессе получения клеток.
Нейроны, которые сначала выглядят и «стреляют» нормально
Далее команда изучила форму и электрическое поведение отдельных нейронов. С помощью детальной визуализации они реконструировали сотни одиночных клеток и обнаружили, что у пациентов и в контроле нейроны имели сопоставимо сложные ветвящиеся структуры — что говорит о том, что при Санфилиппо эти клетки способны строить богатую сеть связей. Электрические записи показали, что нейроны обеих групп генерировали потенциалы действия (электрические импульсы, передающие информацию) со схожей амплитудой, скоростью и порогами. Ключевые ионные каналы, создающие эти импульсы, также функционировали нормально. На ранних этапах развития нейроны при Санфилиппо были по внешним характеристикам похожи на типичные нейроны и могли «выстреливать» так же хорошо.
Скрытый дисбаланс между сигналами «вперёд» и «стоп»
Проблемы проявились позже, по мере созревания выращенных в лаборатории сетей. Команда измеряла крошечные токи, втекающие в нейроны при высвобождении соседними клетками химических посредников. В течение нескольких недель у нейронов пациентов сформировалось больше возбуждающих контактов — синапсов, посылающих «вперёд»-сигналы — что отмечалось увеличением кластеров белка PSD95. Ингибирующие контакты, обеспечивающие «стоп»-сигналы, отставали. Это создавало нездоровое смещение в сторону возбуждения. Возбуждающие токи в нейронах пациентов становились более частыми и крупными, тогда как ингибирующие токи оставались в основном без изменений. Когда учёные ввели лёгкий клеточный стресс, временно удалив факторы роста и антиоксиданты, этот сдвиг в сторону возбуждения в культурах пациентов стал гораздо более выраженным, тогда как нейротипичные сети в основном не подверглись изменениям.
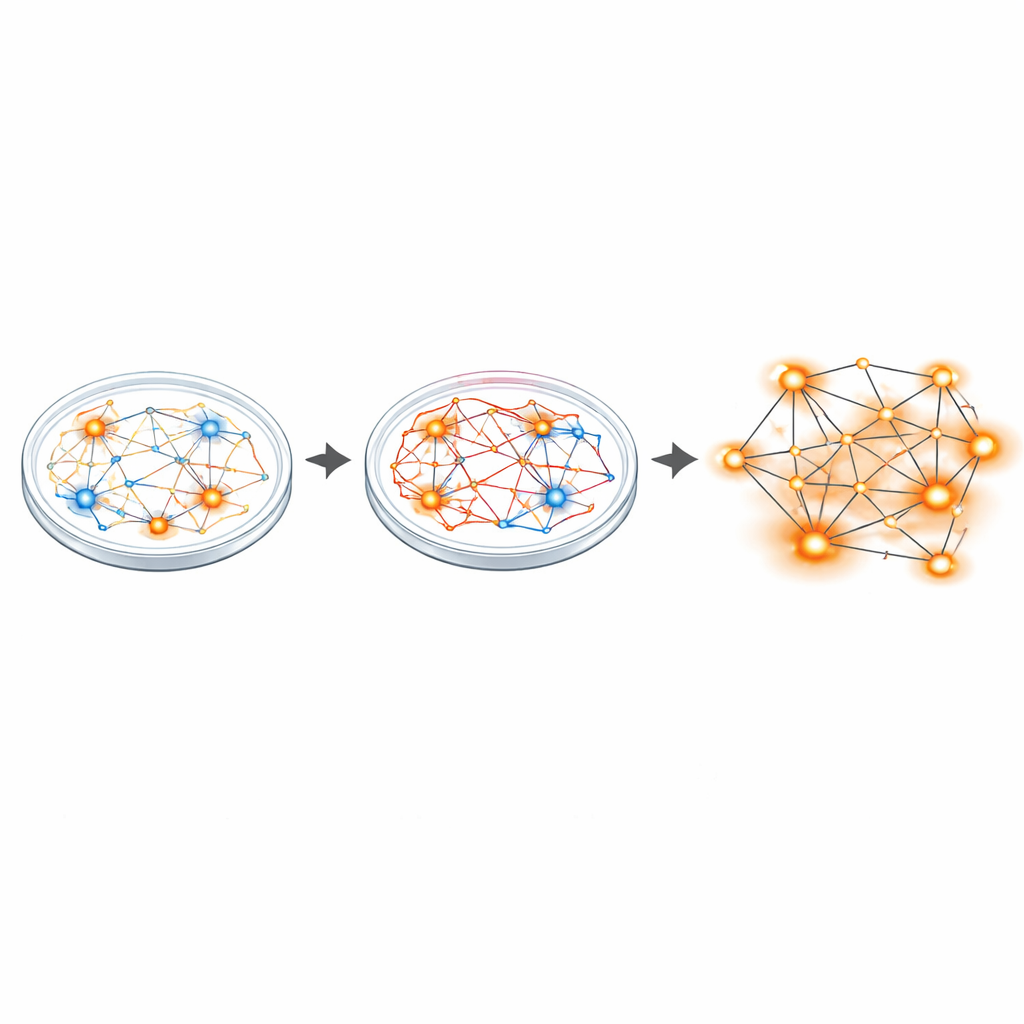
От чрезмерно возбужденных синапсов к гиперактивным сетям
Чтобы увидеть, как этот дисбаланс проявляется на уровне цепей, исследователи использовали мультиэлектродные матрицы — крошечные сетки, регистрирующие активность многих нейронов одновременно. Хотя отдельные нейроны пациентов в среднем имели примерно такую же частоту спайков, как и контрольные, картина на уровне сетей была иной. Культуры Санфилиппо содержали больше активных и «всплескивающих» нейронов и демонстрировали примерно вдвое больше синхронизированных сетевых событий — паттернов координированного «стрелянья», сигнализирующих о гиперактивных цепях. Секвенирование РНК из отдельных ядер тысяч клеток затем выявило широкие сдвиги в активности генов, особенно в генах, которые строят и укрепляют глутаматергические (возбуждающие) синапсы. Ряд этих генов ранее связывали с другими заболеваниями мозга, характеризующимися дисбалансом возбуждения и торможения, такими как аутизм и шизофрения.
Что это означает для будущих лечебных подходов
Для неспециалиста главный вывод таков: при этой форме детской деменции базовая проводка нейронов в целом сохранна, но со временем нарушается баланс между «газом» и «тормозом» мозга. Нейроны чрезмерно стимулируются возбуждающими входами, что ведёт к гиперактивным сетям, способным создавать фон для последующей дегенерации и утраты когнитивных функций. Поскольку команда смогла воспроизвести эти изменения in vitro, используя клетки пациентов, их модель представляет мощную платформу для поиска препаратов, восстанавливающих баланс между возбуждающими и ингибирующими сигналами. Такие терапии не заменят отсутствующий фермент, вызывающий Санфилиппо, но могут помочь сохранить мышление и поведение — потенциально улучшив качество жизни детей, живущих с этим разрушительным заболеванием.
Цитирование: Mazzachi, P., McDonald, E., Greenberg, Z. et al. Modelling synaptic dysfunction in childhood dementia using human iPSC-derived cortical networks. Nat Commun 17, 3161 (2026). https://doi.org/10.1038/s41467-026-71112-9
Ключевые слова: детская деменция, синдром Санфилиппо, синаптический дисбаланс, индуцированные плюрипотентные стволовые клетки, гиперактивность нервных сетей