Clear Sky Science · es
Modelado de la disfunción sináptica en la demencia infantil usando redes corticales humanas derivadas de iPSC
Por qué esta investigación importa a las familias
La demencia infantil es un conjunto devastador de enfermedades cerebrales en las que los niños pierden progresivamente la memoria, las habilidades cognitivas y la independencia. Una de las formas más comunes, el síndrome de Sanfilippo tipo A, actualmente no tiene cura y ofrece opciones de tratamiento limitadas. Este estudio emplea métodos avanzados con células madre para cultivar pequeñas redes cerebrales humanas en el laboratorio, lo que permite a los científicos observar cómo se comportan con el tiempo las neuronas procedentes de niños afectados. Al revelar con precisión cómo fallan estas células, el trabajo apunta a nuevas estrategias farmacológicas que podrían proteger el pensamiento y el aprendizaje, incluso si el diagnóstico del niño se realiza de forma tardía.
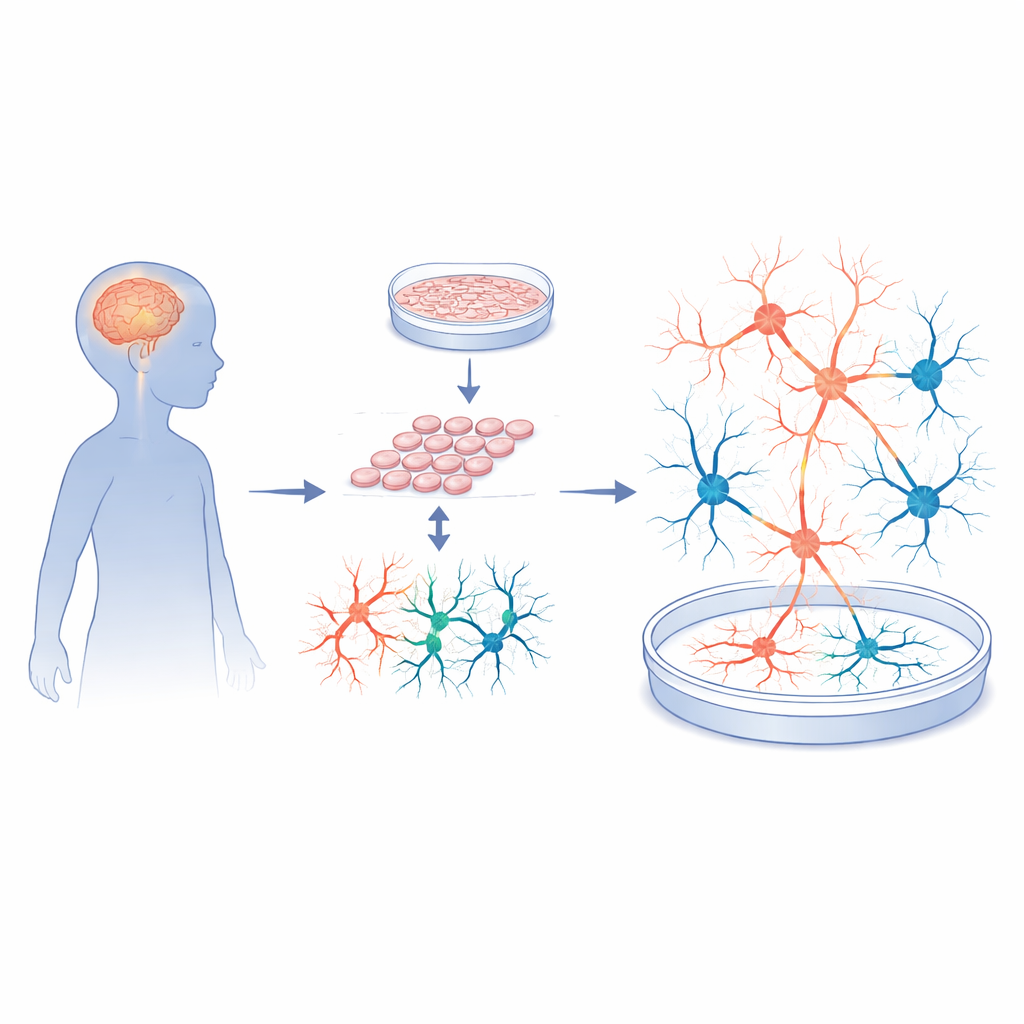
Convertir células de la piel en circuitos cerebrales funcionales
Los investigadores comenzaron con biopsias de piel de cinco niños con Sanfilippo tipo A y cinco donantes neurotípicos emparejados por edad. Reprogramaron estas células cutáneas en células madre pluripotentes inducidas, un tipo celular flexible que puede convertirse en casi cualquier tejido. A estas células madre se les guió cuidadosamente para transformarse en neuronas corticales y células de soporte, imitando la región del cerebro implicada en el aprendizaje, la memoria y el comportamiento. Controles de calidad rigurosos mostraron que tanto las células madre de pacientes como las de controles crecieron bien, tenían cromosomas normales y podían generar células progenitoras neurales de alta calidad. En otras palabras, es poco probable que cualquier diferencia posterior en la actividad tipo cerebral se deba a fallos en el proceso básico de generación celular.
Neuronas que al principio lucen y disparan de forma normal
A continuación, el equipo examinó la forma y el comportamiento eléctrico de neuronas individuales. Mediante imágenes detalladas, reconstruyeron cientos de células y encontraron que las neuronas de pacientes y controles tenían patrones de ramificación igualmente complejos, lo que sugiere que Sanfilippo no impide que estas células construyan una red rica de conexiones. Registros eléctricos mostraron que las neuronas de ambos grupos producían potenciales de acción (los picos eléctricos que transmiten información) con una fuerza, velocidad y umbrales comparables. Los canales iónicos clave que generan estos picos también funcionaban con normalidad. Por tanto, en las primeras etapas del desarrollo, las neuronas con Sanfilippo se parecían mucho a las típicas y podían disparar igual de bien.
Desequilibrio oculto entre señales de "adelante" y "freno"
Los problemas aparecieron más tarde, a medida que las redes cultivadas en el laboratorio maduraban. El equipo midió corrientes diminutas que entran en las neuronas cuando las células vecinas liberan mensajeros químicos. Con el paso de las semanas, las neuronas de Sanfilippo desarrollaron más contactos excitatorios —sinapsis que envían señales de "adelante"— marcados por un aumento de agrupamientos de la proteína PSD95. Los contactos inhibitorios, que proporcionan señales de "freno", se quedaron rezagados. Esto creó una inclinación poco saludable hacia la excitación. Las corrientes excitatorias en las neuronas de pacientes se volvieron más frecuentes y mayores, mientras que las corrientes inhibitorias permanecieron en gran medida sin cambios. Cuando los científicos introdujeron un estrés celular leve mediante la eliminación breve de factores de crecimiento y antioxidantes, este sesgo excitatorio en los cultivos de pacientes se hizo mucho más pronunciado, mientras que las redes neurotípicas resultaron mayormente afectadas en menor medida.
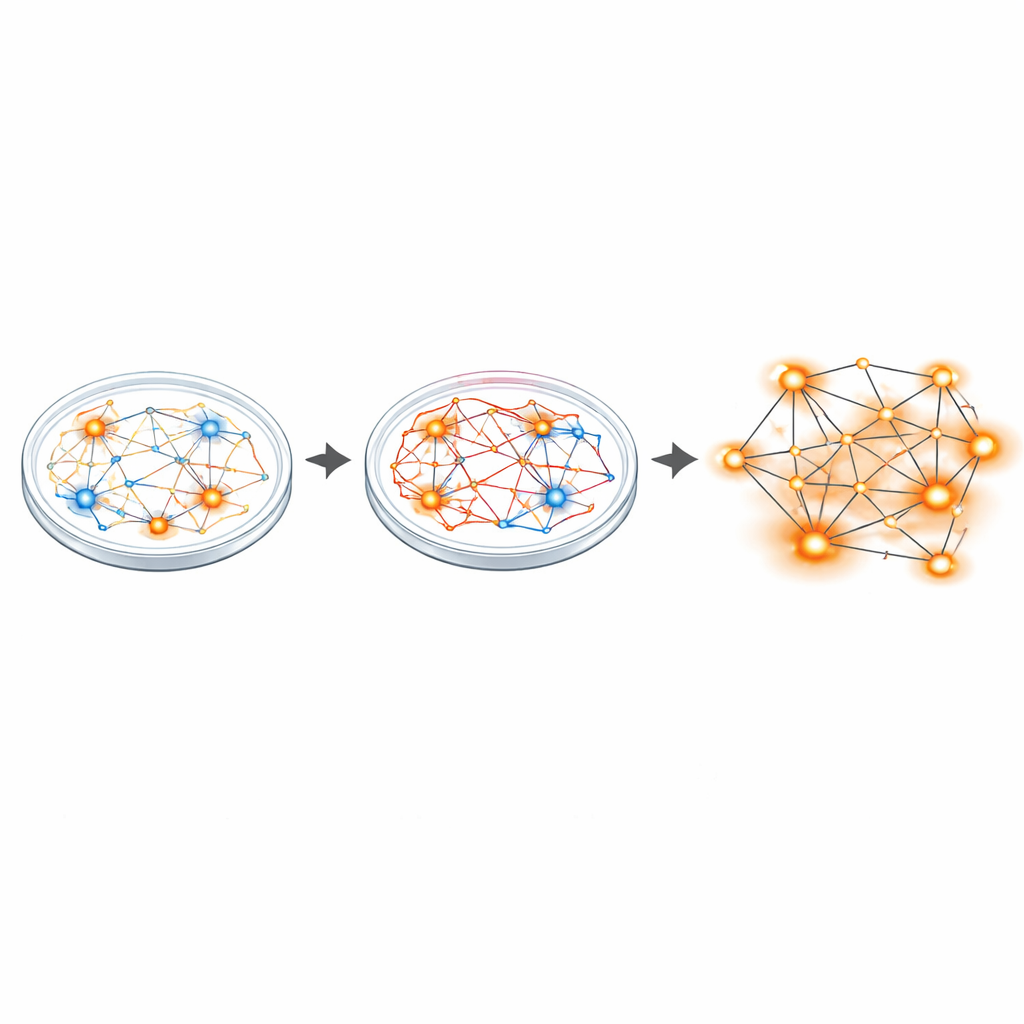
De sinapsis sobreexcitas a redes hiperactivas
Para ver cómo se manifiesta este desequilibrio a nivel de circuito, los investigadores usaron matrices de multielectrodos —pequeñas cuadrículas que registran desde muchas neuronas a la vez. Mientras que las neuronas individuales de los pacientes disparaban a una tasa media similar a la de los controles, las redes en conjunto contaron otra historia. Los cultivos de Sanfilippo presentaron más neuronas activas y con estallidos y mostraron aproximadamente el doble de eventos sincronizados en la red, un patrón de disparo coordinado que señala circuitos hiperactivos. La secuenciación de ARN de núcleo único de miles de células reveló entonces cambios amplios en la actividad génica, especialmente en genes que construyen y fortalecen las sinapsis glutamatérgicas (excitatorias). Varios de estos genes se han relacionado con otras condiciones cerebrales que presentan desequilibrios entre excitación e inhibición, como el autismo y la esquizofrenia.
Qué implica esto para futuros tratamientos
Para un público no especialista, el mensaje clave es que en esta demencia infantil la arquitectura básica de las neuronas está en gran medida intacta, pero con el tiempo se altera el equilibrio entre los aceleradores y los frenos del cerebro. Las neuronas quedan sobreexcitadas por la entrada excitatoria, provocando redes hiperactivas que pueden preparar el terreno para una degeneración posterior y la pérdida de capacidades cognitivas. Dado que el equipo pudo reproducir estos cambios en una placa usando células derivadas de pacientes, su modelo ofrece una plataforma potente para buscar fármacos que restauren el equilibrio entre señales excitatorias e inhibitorias. Tales tratamientos no reemplazarían la enzima faltante que causa Sanfilippo, pero podrían ayudar a preservar el pensamiento y el comportamiento —potencialmente mejorando la calidad de vida de los niños que viven con esta enfermedad devastadora.
Cita: Mazzachi, P., McDonald, E., Greenberg, Z. et al. Modelling synaptic dysfunction in childhood dementia using human iPSC-derived cortical networks. Nat Commun 17, 3161 (2026). https://doi.org/10.1038/s41467-026-71112-9
Palabras clave: demencia infantil, síndrome de Sanfilippo, desequilibrio sináptico, células madre pluripotentes inducidas, hiperexcitabilidad de redes neuronales