Clear Sky Science · nl
Modelleren van synaptische disfunctie bij kinder-dementie met behulp van menselijke iPSC-afgeleide corticale netwerken
Waarom dit onderzoek belangrijk is voor gezinnen
Kinder-dementie is een verwoestende groep hersenaandoeningen waarbij kinderen geleidelijk geheugen, denkvaardigheden en zelfstandigheid kwijtraken. Een van de meest voorkomende vormen, Sanfilippo-syndroom type A, heeft op dit moment geen geneesmiddel en weinig behandelopties. Deze studie gebruikt geavanceerde stamcelmethoden om kleine menselijke hersennetwerken in het laboratorium te kweken, waardoor wetenschappers kunnen volgen hoe neuronen van getroffen kinderen zich in de loop van de tijd gedragen. Door precies te onthullen hoe deze cellen fout gaan, wijst het werk op nieuwe medicijnstrategieën die denken en leren mogelijk kunnen beschermen, zelfs als een kind laat wordt gediagnosticeerd.
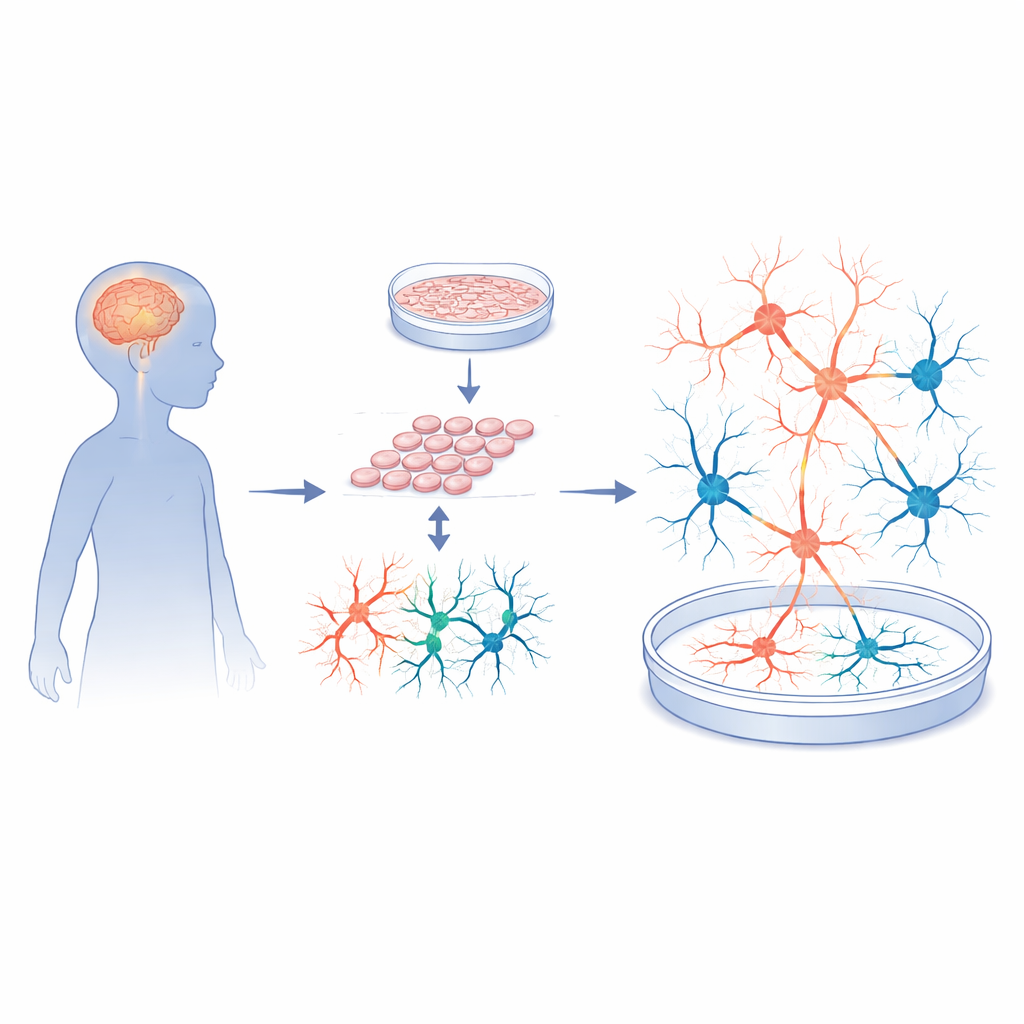
Huidcellen omzetten in werkende hersencircuits
De onderzoekers begonnen met huidbiopten van vijf kinderen met Sanfilippo type A en vijf neurotypische, leeftijdsgematchte donoren. Ze programmeerden deze huidcellen om tot geïnduceerde pluripotente stamcellen, een flexibele celsoort die vrijwel elk weefsel kan worden. Deze stamcellen werden vervolgens zorgvuldig gestuurd om corticale neuronen en ondersteunende cellen te worden, waarmee het hersengebied wordt nagebootst dat betrokken is bij leren, geheugen en gedrag. Strenge kwaliteitscontroles toonden aan dat zowel patiënt- als controlemateriaal goed groeiden, normale chromosomen hadden en hoogwaardige neurale voorlopercellen konden vormen. Met andere woorden: eventuele latere verschillen in hersenachtige activiteit waren onwaarschijnlijk toe te schrijven aan fouten in het basale celvormingsproces.
Neuronen die er aanvankelijk normaal uitzien en vuren
Vervolgens onderzocht het team de vorm en het elektrische gedrag van individuele neuronen. Met behulp van gedetailleerde beeldvorming reconstrueerden ze honderden enkele cellen en ontdekten dat patiënt- en controeneuronen vergelijkbaar complexe vertakkingspatronen hadden—wat suggereert dat Sanfilippo deze cellen niet tegenhoudt in het opbouwen van een rijk netwerk van verbindingen. Elektrische opnamen lieten zien dat neuronen uit beide groepen actiepotentialen produceerden (de elektrische pieken die informatie dragen) met vergelijkbare sterkte, snelheid en drempels. Belangrijke ionkanalen die deze pieken genereren werkten eveneens normaal. Vroeg in de ontwikkeling leken Sanfilippo-neuronen dus veel op typische neuronen en konden ze even goed vuren.
Verborgen onbalans tussen “gas”- en “rem”-signalen
De problemen werden later zichtbaar, naarmate de in het lab gekweekte netwerken rijpten. Het team mat kleine stromen die in neuronen liepen wanneer naburige cellen chemische boodschappers vrijgaven. In de loop van weken ontwikkelden Sanfilippo-neuronen meer exciterende contactpunten—synapsen die “gas”-signalen sturen—gekenmerkt door toegenomen clusters van het eiwit PSD95. Inhiberende contacten, die “rem”-signalen leveren, bleven achter. Dit creëerde een ongezonde helling richting excitatie. De exciterende stromen in patiëntencellen werden frequenter en groter, terwijl de remmende stromen grotendeels ongewijzigd bleven. Wanneer de wetenschappers milde cellulaire stress inbrachten door tijdelijk groeifactoren en antioxidanten te verwijderen, werd deze exciterende bias in patiëntenculturen veel duidelijker, terwijl neurotypische netwerken grotendeels ongevoelig bleven.
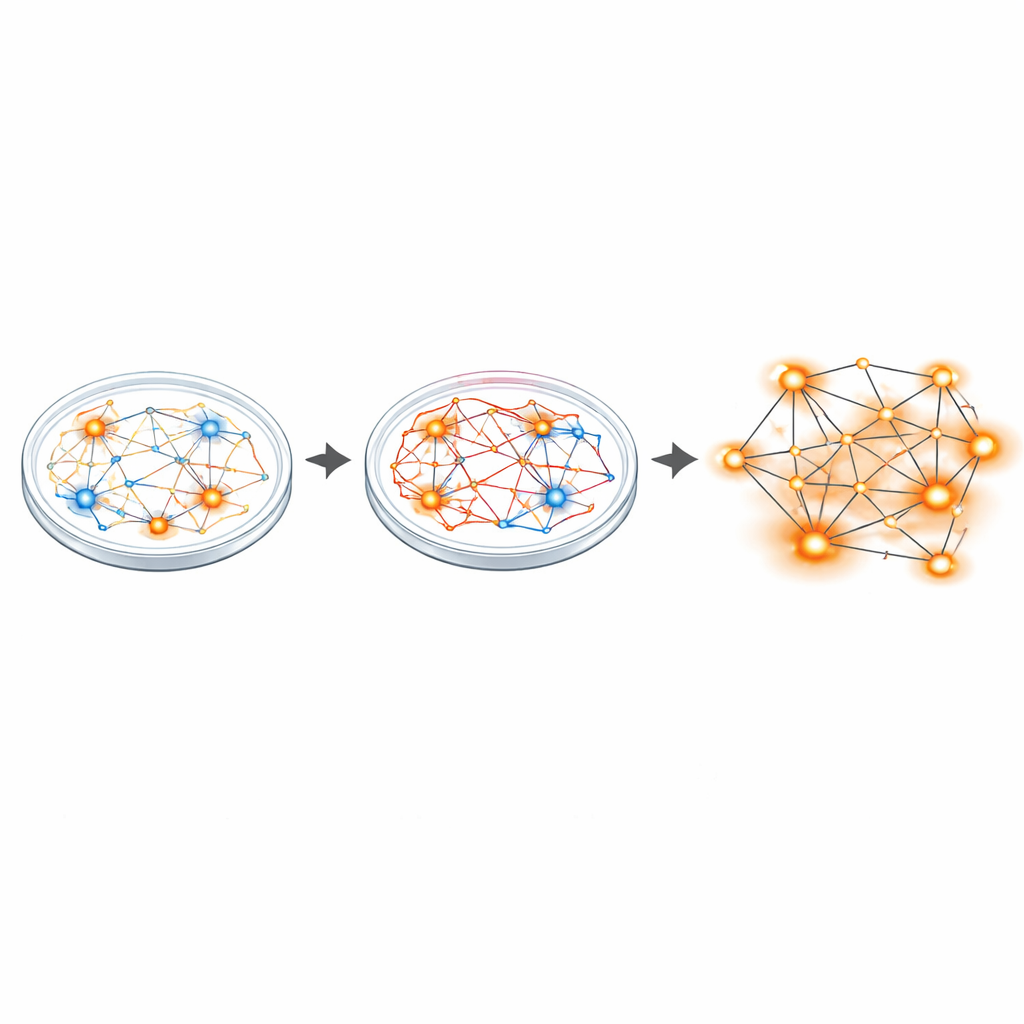
Van overgeprikkelde synapsen naar hyperactieve netwerken
Om te zien hoe deze onbalans zich op circuitschaal uitwerkt, gebruikten de onderzoekers multielektrode-arrays—kleine rasterjes die van veel neuronen tegelijk kunnen opnemen. Terwijl individuele neuronen van patiënten ongeveer hetzelfde gemiddelde vuurtempo hadden als die van controles, vertelde het netwerk als geheel een ander verhaal. Sanfilippo-culturen hadden meer actieve en burstende neuronen en vertoonden ruwweg twee keer zoveel gesynchroniseerde netwerkevenementen, een patroon van gecoördineerd vuren dat wijst op hyperactieve circuits. Single-nucleus RNA-sequencing van duizenden cellen onthulde vervolgens brede verschuivingen in genactiviteit, vooral in genen die glutamaterge (exciterende) synapsen bouwen en versterken. Verscheidene van deze genen zijn gelinkt aan andere hersenaandoeningen met onbalans tussen excitatie en inhibitie, zoals autisme en schizofrenie.
Wat dit betekent voor toekomstige behandelingen
Voor niet-specialisten is de kernboodschap dat bij deze kinder-dementie de basisbedrading van neuronen grotendeels intact blijft, maar dat de balans tussen de hersenacceleratoren en -remmen na verloop van tijd verstoord raakt. Neuronen worden te sterk aangedreven door exciterende input, wat leidt tot hyperactieve netwerken die mogelijk de voedingsbodem vormen voor latere degeneratie en verlies van cognitieve functies. Omdat het team deze veranderingen in een schaaltje met patiënt-afgeleide cellen kon reproduceren, biedt hun model een krachtig platform om naar medicijnen te zoeken die de balans tussen excitatoire en inhibitoire signalen herstellen. Zulke behandelingen zouden het ontbrekende enzym dat Sanfilippo veroorzaakt niet vervangen, maar ze zouden kunnen helpen denken en gedrag te behouden—mogelijk de kwaliteit van leven verbeteren voor kinderen die met deze verwoestende ziekte leven.
Bronvermelding: Mazzachi, P., McDonald, E., Greenberg, Z. et al. Modelling synaptic dysfunction in childhood dementia using human iPSC-derived cortical networks. Nat Commun 17, 3161 (2026). https://doi.org/10.1038/s41467-026-71112-9
Trefwoorden: kinder-dementie, Sanfilippo-syndroom, synaptische onbalans, geïnduceerde pluripotente stamcellen, hyperexcitabiliteit van neurale netwerken