Clear Sky Science · zh
IVNS1ABP 突变在新发现的早衰性神经病中驱动细胞衰老
当神经过早衰老
一些儿童在很小的年纪就出现类似衰老的体征——白发、皮肤脆弱、上学期间就出现行走困难。本文研究一种新近识别的此类疾病,从单一有缺陷的基因追溯到脑细胞的早衰,为我们理解整个神经系统如何变老提供了线索。
一种新型的早发衰老疾病
研究者描述了一个家系,几位青少年出现了罕见的“早衰性神经病变”。这些年轻人皮肤斑驳、早发白发、行走困难并伴有智力障碍,同时关键脑结构出现萎缩。通过全基因组扫描,科学家发现受影响的兄弟姐妹都携带 IVNS1ABP 基因的一种罕见变异的两个拷贝。此基因此前主要与细胞应对流感病毒有关,并未与衰老或神经疾病直接关联。研究团队于是着手揭示这一突变如何使细胞和神经系统表现出过早老化的特征。 
在培养皿中重建疾病
为安全且精细地研究这一疾病,团队将患者与健康亲属的皮肤细胞重编程为诱导多能干细胞,然后将其定向分化为神经祖细胞,即脑细胞的前体。他们还用基因编辑创建了“同基因”对——除 IVNS1ABP 突变外基因组相同的细胞对,甚至制作了完全的基因敲除。在患者细胞、编辑后的干细胞及其神经后代中都出现了相同的模式:细胞分裂更慢、在细胞周期的各个阶段停留更久,且常常无法顺利分裂成两个子细胞。
细胞呈现衰老的迹象
有缺陷的细胞表现出细胞衰老的经典特征。它们累积了 DNA 损伤,可通过标记断裂或受压染色体的分子标志物观察到。维持 DNA 组织性的保护性染色质标记减少,细胞核本身常常变大。许多细胞对一种常用的衰老染色呈阳性,并启动 p16 及相关基因,强制进入永久性生长停滞。在三维“微脑”——大脑类器官中,突变的神经祖细胞过早退出细胞周期并提前分化为神经元。此类类器官体积更小、分裂前体细胞层更薄,但更成熟神经元层更厚,表明应当用于构建大脑的“种子”细胞库被过快耗尽。
细胞骨架辅助因子如何失常
进一步探究时,科学家们询问 IVNS1ABP 正常情况下与哪些蛋白互作。通过拉下实验和质谱分析,他们发现健康的 IVNS1ABP 蛋白与肌动蛋白及一组与肌动蛋白相关的蛋白紧密相互作用,这些蛋白帮助构建和重塑细胞的内部支架。相比之下,突变体与这些结合伙伴结合较差。在体外实验中,正常的 IVNS1ABP 能有效促进肌动蛋白丝的组装,而突变形式显著弱化,即便在更高浓度下也结合不佳。在突变的神经祖细胞内,稳固的肌动蛋白丝向松散的单体形式倾斜,且分裂时用于收紧并把细胞掐成两份的肌动蛋白环变得稀薄且不均匀。 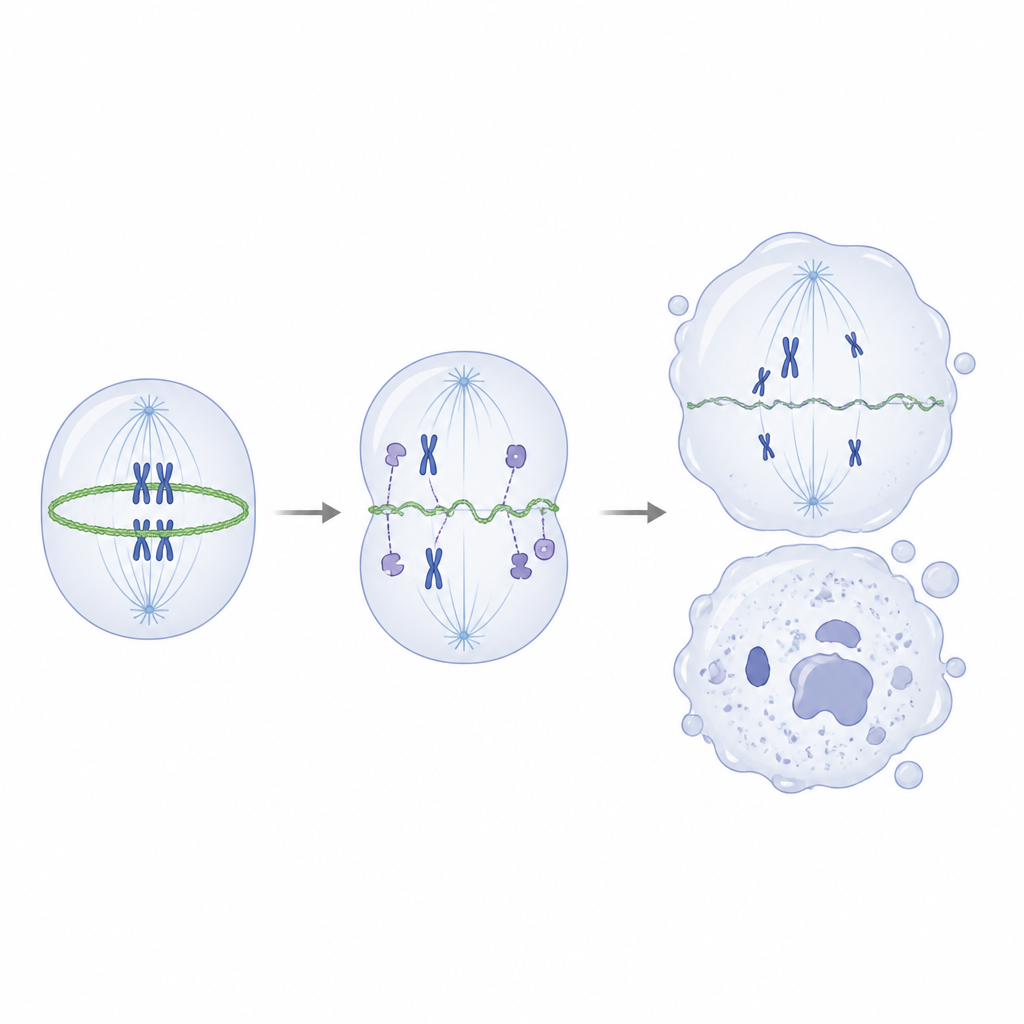
从分裂失败到神经过早老化
分裂过程中受损的内部支架导致染色体错位、梭形体异常和不均匀的细胞分裂,这反过来产生 DNA 损伤并将细胞推向衰老的、不可分裂状态。重要的是,当研究者使用低剂量促进肌动蛋白组装的药物时,能够部分恢复肌动蛋白平衡、改善收缩环形态、减少分裂错误,并降低 DNA 损伤和细胞衰老标志,尽管基因突变仍在。在大脑类器官中,同样的处理部分挽救了生长和神经祖细胞库。对普通读者而言,结论是这种罕见的儿童疾病源于单个基因,该基因在细胞分裂时帮助管理细胞内部支架。当该辅助因子失效时,发育中的神经细胞分裂不良、过早耗竭并提前老化,导致神经元数量和功能减少,最终出现早发衰老特征以及运动和认知问题。
引用: Yuan, F., Tan, Y.S., Wang, H. et al. IVNS1ABP mutation drives cellular senescence in newly identified progeroid neuropathy. Nat Commun 17, 4159 (2026). https://doi.org/10.1038/s41467-026-70756-x
关键词: 细胞衰老, 早衰性神经病变, IVNS1ABP, 肌动蛋白动力学, 神经祖细胞