Clear Sky Science · fr
La mutation IVNS1ABP provoque la sénescence cellulaire dans une neuropathie progeroïde nouvellement identifiée
Quand les nerfs vieillissent trop tôt
Certaines enfants présentent des signes de vieillissement bien avant l’âge, développant des cheveux gris, une peau fragile et des difficultés à marcher alors qu’ils sont encore à l’école. Cette étude examine l’un de ces états nouvellement identifiés, le retraçant d’un seul gène défectueux jusqu’aux cellules cérébrales vieillissantes, et offrant une fenêtre sur la manière dont notre système nerveux peut vieillir chez tous.
Un nouveau type de trouble du vieillissement précoce
Les chercheurs décrivent une famille dans laquelle plusieurs adolescents ont développé une rare « neuropathie progeroïde ». Ces jeunes présentaient une peau marbrée, un grisonnement prématuré des cheveux, des troubles de la marche et une déficience intellectuelle, ainsi qu’un amincissement de structures cérébrales clés. En explorant leur ADN, les scientifiques ont découvert que les frères et sœurs affectés portaient tous deux copies d’une variation rare du gène appelé IVNS1ABP. Ce gène était jusque-là surtout connu pour son rôle dans la réponse cellulaire au virus de la grippe, et non pour le vieillissement ou les maladies nerveuses. L’équipe s’est donc attelée à comprendre comment cette mutation pouvait vieillir prématurément les cellules et le système nerveux. 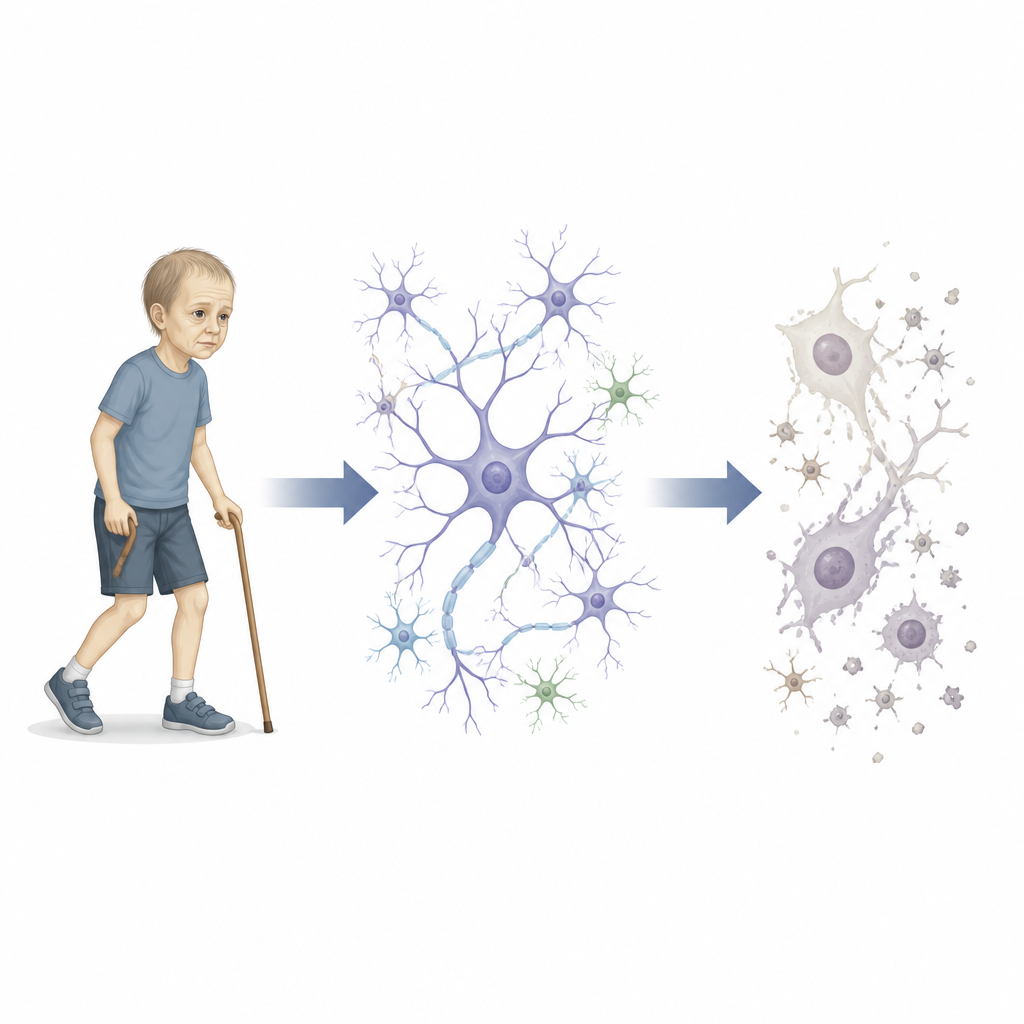
Recréer la maladie en culture
Pour étudier le trouble en toute sécurité et en détail, l’équipe a reprogrammés des cellules cutanées de patients et de proches non affectés en cellules souches pluripotentes induites, puis les a dirigées vers des cellules progénitrices neurales, les précurseurs des cellules cérébrales. Ils ont également utilisé l’édition génomique pour créer des paires « isogéniques » de cellules génétiquement identiques à l’exception de la seule mutation IVNS1ABP, et ont même réalisé des extinctions complètes du gène. Dans les cellules des patients, les cellules souches éditées et leurs descendantes neuronales, le même schéma est apparu : les cellules se divisaient plus lentement, restaient plus longtemps dans chaque phase du cycle cellulaire et échouaient fréquemment à se séparer proprement en deux filles.
Des cellules montrant des signes de vieillissement
Les cellules défectueuses présentaient des signes classiques du vieillissement cellulaire. Elles accumulaient des dommages à l’ADN, visibles par des marqueurs moléculaires indiquant des chromosomes cassés ou stressés. Les marques de chromatine protectrices qui aident à organiser l’ADN étaient réduites, tandis que le noyau lui‑même devenait souvent plus volumineux. De nombreuses cellules étaient positives au colorant couramment utilisé pour la sénescence et activaient p16 et des gènes associés qui imposent un arrêt permanent de la croissance. Lorsqu’on les cultivait en « mini‑cerveaux » tridimensionnels appelés organoïdes cérébraux, les progéniteurs neuraux mutants quittaient le cycle cellulaire précocement et se différenciaient en neurones plus tôt que prévu. Ces organoïdes étaient plus petits, avec des zones de précurseurs en division plus minces mais des couches de neurones plus matures plus épaisses, suggérant que la réserve de cellules « semences » destinée à construire le cerveau s’épuisait trop vite.
Comment un auxiliaire du cytosquelette déraille
En creusant davantage, les scientifiques ont cherché quels protéines s’associent normalement à IVNS1ABP. Par des expériences d’extraction et de spectrométrie de masse, ils ont constaté que la protéine saine interagit fortement avec l’actine et un groupe de protéines associées à l’actine qui aident à construire et remodeler l’échafaudage interne de la cellule. En revanche, la forme mutante se liait mal à ces partenaires. Dans des essais in vitro, IVNS1ABP normal favorisait efficacement l’assemblage des filaments d’actine, tandis que la version mutante était beaucoup plus faible et ne se liant pas bien même à des concentrations plus élevées. À l’intérieur des progéniteurs neuraux mutants, l’équilibre bascula de l’actine filamentaire robuste vers sa forme monomérique lâche, et l’anneau d’actine qui se contracte normalement pour cliver une cellule en division devint fin et irrégulier. 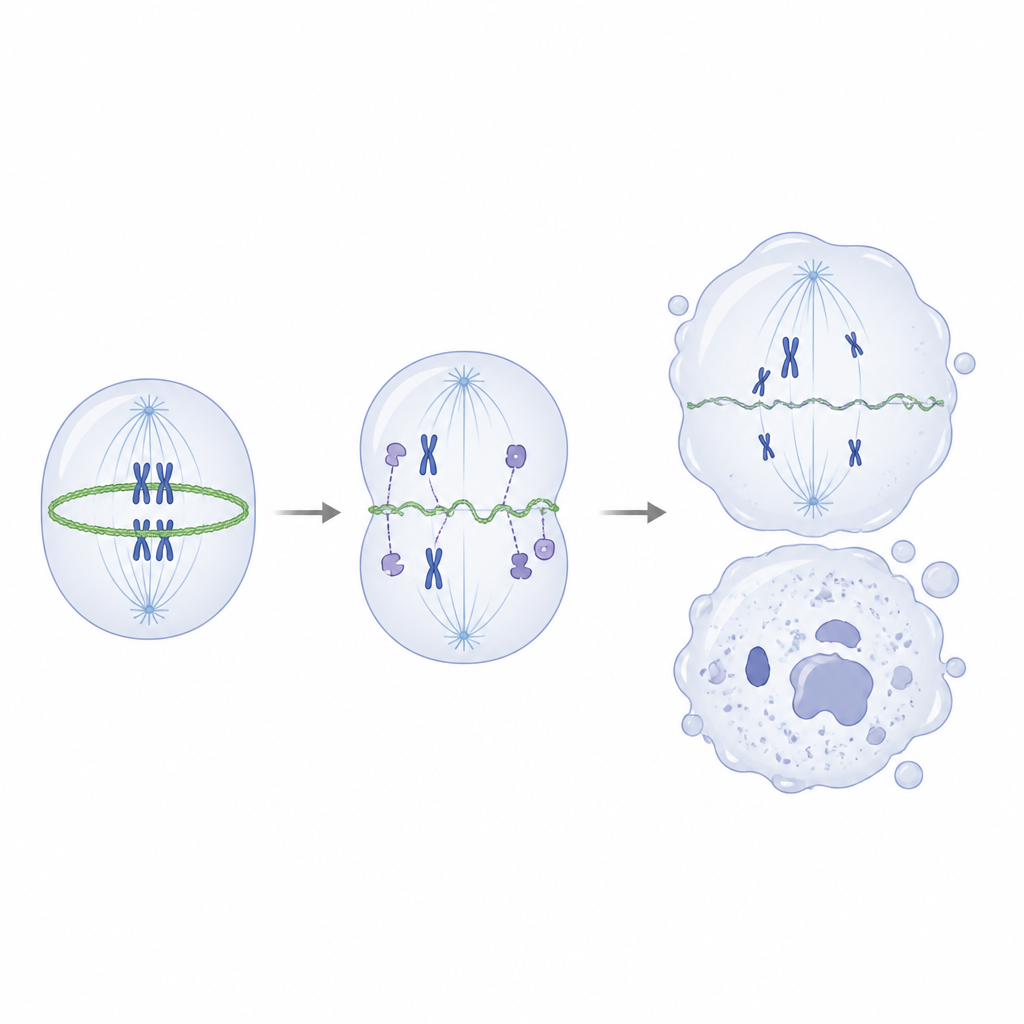
De la division cellulaire défaillante au vieillissement précoce des nerfs
Ce défaut de l’échafaudage lors de la division entraînait des chromosomes mal alignés, des fuseaux anormaux et des divisions inégales, ce qui produisait à son tour des dommages à l’ADN et poussait les cellules dans un état sénescent et non diviseur. Fait important, lorsque les chercheurs utilisèrent une faible dose d’un médicament qui favorise l’assemblage de l’actine, ils purent partiellement rétablir l’équilibre de l’actine, améliorer la forme de l’anneau contractile, réduire les erreurs de division et diminuer les marqueurs de dommages à l’ADN et de vieillissement cellulaire, bien que la mutation génétique demeure. Dans les organoïdes cérébraux, le même traitement permit en partie de restaurer la croissance et la réserve de progéniteurs neuraux. Pour un non‑spécialiste, la conclusion est que cette rare maladie infantile provient d’un seul gène qui aide normalement à gérer l’échafaudage interne de la cellule pendant la division. Lorsque cet auxiliaire fait défaut, les cellules nerveuses en développement se divisent mal, s’épuisent prématurément et vieillissent trop tôt, entraînant moins de neurones, moins robustes, et finalement des signes précoces de vieillissement ainsi que des troubles moteurs et cognitifs.
Citation: Yuan, F., Tan, Y.S., Wang, H. et al. IVNS1ABP mutation drives cellular senescence in newly identified progeroid neuropathy. Nat Commun 17, 4159 (2026). https://doi.org/10.1038/s41467-026-70756-x
Mots-clés: sénescence cellulaire, neuropathie progeroïde, IVNS1ABP, dynamique de l’actine, cellules progénitrices neurales