Clear Sky Science · nl
IVNS1ABP-mutatie veroorzaakt celveroudering bij nieuw geïdentificeerde progeroïde neuropathie
Wanneer zenuwen te snel verouderen
Sommige kinderen tonen verschijnselen van ouderdom lang voordat dat normaal is: ze krijgen grijs haar, broze huid en moeite met lopen terwijl ze nog op school zitten. Deze studie onderzoekt zo’n nieuw geïdentificeerde aandoening, volgt deze terug tot één foutief gen en biedt daarmee inzicht in hoe onze zenuwstelsel bij iedereen voortijdig ouder zou kunnen worden.
Een nieuw type vroegtijdige verouderingsstoornis
De onderzoekers beschrijven een familie waarin meerdere adolescenten een zeldzame «progeroïde neuropathie» ontwikkelden. Deze jonge mensen hadden gevlekt huidbeeld, voortijdig grijs worden van het haar, loopproblemen en verstandelijke beperking, samen met verdunning van belangrijke hersenstructuren. Door hun DNA te scannen ontdekten de wetenschappers dat de aangedane broers en zussen beide kopieën droegen van een zeldzame wijziging in een gen genaamd IVNS1ABP. Dit gen was voorheen vooral bekend vanwege een rol in hoe cellen omgaan met het griepvirus, niet voor veroudering of zenuwziekten. Het team ging na hoe deze mutatie ervoor kan zorgen dat cellen en het zenuwstelsel er te vroeg oud uitzien. 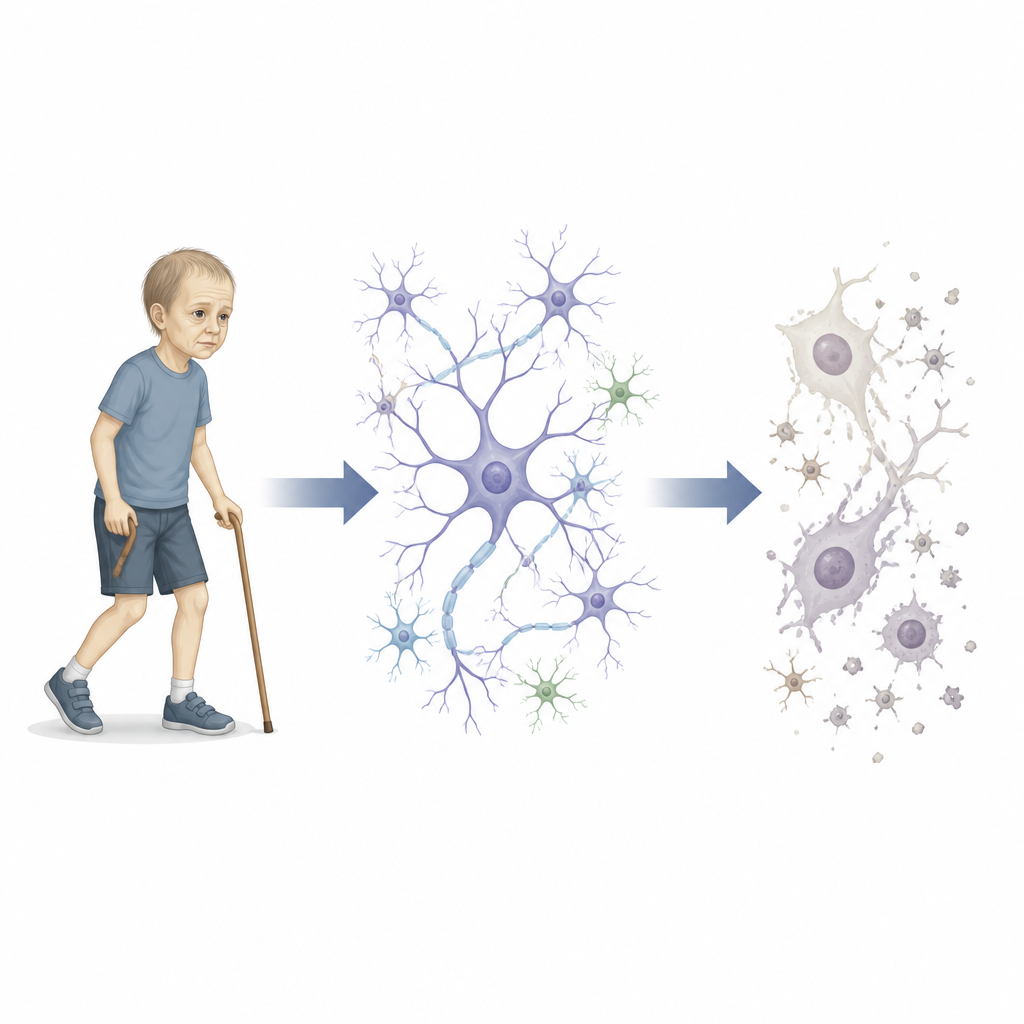
De ziekte in een schaaltje nabootsen
Om de aandoening veilig en gedetailleerd te bestuderen, herprogrammeerde het team huidcellen van patiënten en niet-aangedane familieleden naar geïnduceerde pluripotente stamcellen, en leidde deze vervolgens naar neurale progenitorcellen, de voorlopers van hersencellen. Ze gebruikten ook genbewerking om «isogene» celparen te maken die genetisch identiek waren behalve voor de enkele IVNS1ABP-mutatie, en maakten zelfs volledige gen-uitzettingen. In patiëntencellen, bewerkte stamcellen en hun neurale nazaten trad hetzelfde patroon op: cellen deelden langzamer, verbleven langer in elke fase van de celcyclus en slaagden vaak niet in om netjes in twee dochters te splitsen.
Cellen met tekenen van veroudering
De defecte cellen vertoonden klassieke kenmerken van cellulaire veroudering. Ze stapelden DNA-schade op, zichtbaar via moleculaire markeringen die gebroken of gestreste chromosomen aangeven. Beschermende chromatinemarkeringen die helpen DNA georganiseerd te houden waren verminderd, terwijl de kern zelf vaak groter werd. Veel cellen werden positief voor een veelgebruikte verouderingskleuring en zetten p16 en verwante genen aan die permanente groeistilstand afdwingen. In driedimensionale «mini-hersenen» genaamd cerebrale organoïden stopten mutant neurale progenitoren vroegtijdig met delen en differentieerden ze eerder dan verwacht naar neuronen. Deze organoïden waren kleiner en hadden dunnere zones van delende voorlopercellen maar dikkere lagen meer rijpe neuronen, wat suggereert dat de voorraad van «zaad»-cellen die de hersenen zouden moeten opbouwen te snel werd opgebruikt.
Hoe een cytoskelet-hulp verkeerd gaat
Dieper graven vroeg welke eiwitten normaal met IVNS1ABP samenwerken. Met pull-downexperimenten en massaspectrometrie vonden ze dat het gezonde eiwit sterk interacteert met actine en een groep actine-geassocieerde eiwitten die helpen het interne steigerwerk van de cel op te bouwen en te herschikken. De mutantvorm bond daarentegen slecht met deze partners. In proefbuisassays bevorderde normale IVNS1ABP efficiënt de assemblage van actinefilamenten, terwijl de muteerede versie veel zwakker was en zelfs bij hogere concentraties slecht bond. Binnen mutant neurale progenitoren sloeg de balans om van stevig filamentair actine naar de losse, enkel-eenheidvorm, en de actinering die normaal samentrekt om een delende cel in tweeën te knijpen werd dun en ongelijkmatig. 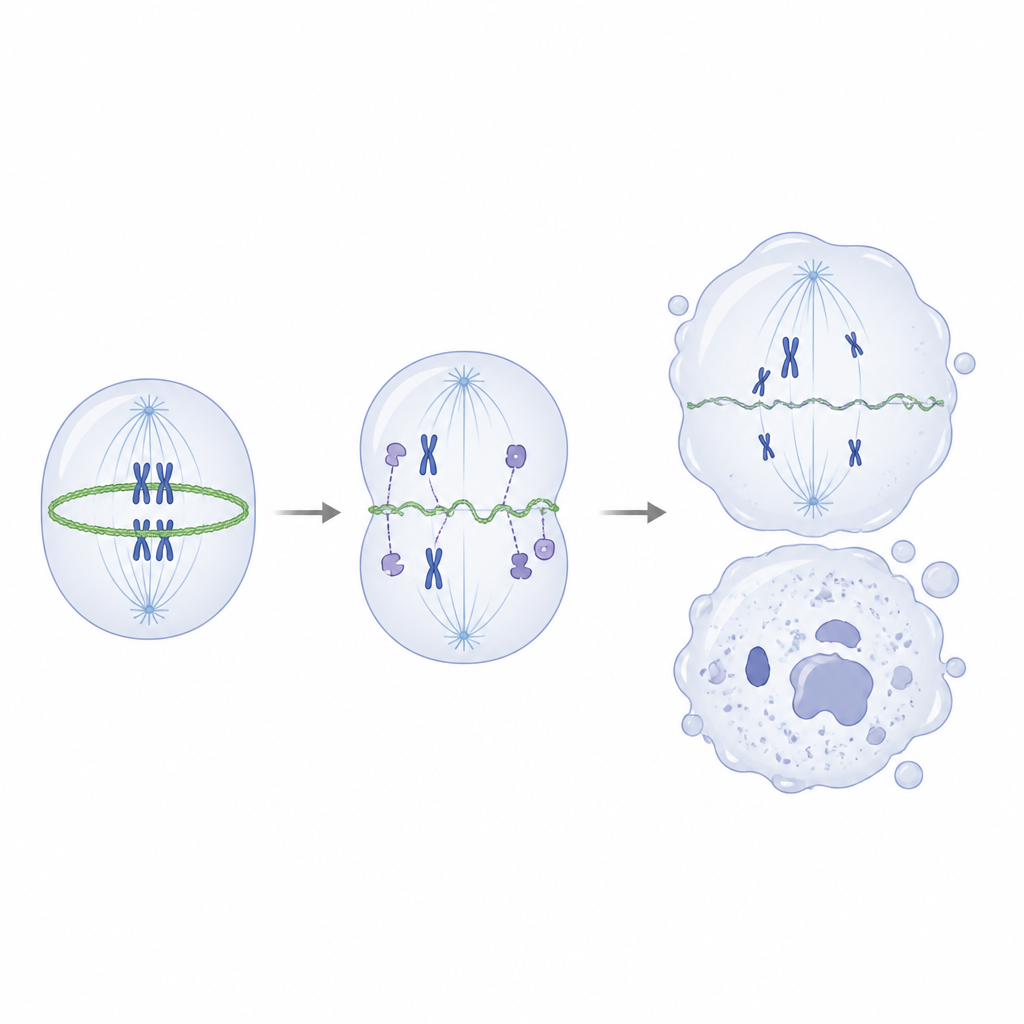
Van gebroken celdelingen naar vroegtijdige zenuwveroudering
Dit kapotte steigerwerk tijdens deling leidde tot verkeerd uitgelijnde chromosomen, abnormale spoelfiguren en ongelijkmatige celdelingen, wat op zijn beurt DNA-schade veroorzaakte en cellen in een senescent, niet-delend stadium duwde. Belangrijk is dat toen de onderzoekers een lage dosis van een middel gebruikten dat actine-assemblage bevordert, ze het actine-evenwicht deels konden herstellen, de vorm van de contractiele ring verbeterden, delingsfouten verminderden en merkers van DNA-schade en cellulaire veroudering lichter zagen, ook al bleef de genmutatie aanwezig. In cerebrale organoïden herstelde dezelfde behandeling gedeeltelijk de groei en de voorraad neurale progenitoren. Voor een leek is de conclusie dat deze zeldzame kinderziekte voortkomt uit één gen dat normaal helpt het interne steigerwerk van de cel tijdens deling te beheren. Als die helper faalt, delen zich ontwikkelende zenuwcellen slecht, raken ze voortijdig uitgeput en verouderen ze te snel, wat leidt tot minder en zwakkere neuronen en uiteindelijk tot zowel vroegtijdige verouderingskenmerken als problemen met bewegen en denken.
Bronvermelding: Yuan, F., Tan, Y.S., Wang, H. et al. IVNS1ABP mutation drives cellular senescence in newly identified progeroid neuropathy. Nat Commun 17, 4159 (2026). https://doi.org/10.1038/s41467-026-70756-x
Trefwoorden: cellulaire senescentie, progeroïde neuropathie, IVNS1ABP, actinedynamiek, neurale progenitorcellen