Clear Sky Science · it
La mutazione IVNS1ABP induce senescenza cellulare in una nuova neuropatia progeroide
Quando i nervi invecchiano troppo presto
Alcuni bambini mostrano segni di invecchiamento molto prima del tempo, sviluppando capelli grigi, pelle fragile e difficoltà a camminare già durante gli anni scolastici. Questo studio indaga una di queste condizioni di recente identificazione, tracciandone il percorso da un singolo gene difettoso alle cellule cerebrali invecchiate, offrendo uno sguardo su come il nostro sistema nervoso potrebbe invecchiare anche in tutti noi.
Un nuovo tipo di disturbo da invecchiamento precoce
I ricercatori descrivono una famiglia in cui diversi adolescenti hanno sviluppato una rara “neuropatia progeroide”. Questi giovani presentavano cute macchiata, ingrigimento precoce dei capelli, problemi di deambulazione e disabilità intellettiva, insieme a un assottigliamento di strutture cerebrali chiave. Analizzando il loro DNA, gli scienziati hanno scoperto che i fratelli colpiti portavano entrambi le copie di una rara variante nel gene chiamato IVNS1ABP. Questo gene era noto principalmente per il suo ruolo nella risposta cellulare al virus dell’influenza, non per l’invecchiamento o le malattie nervose. Il team ha quindi cercato di capire come questa mutazione potesse far apparire le cellule e il sistema nervoso vecchi prima del tempo. 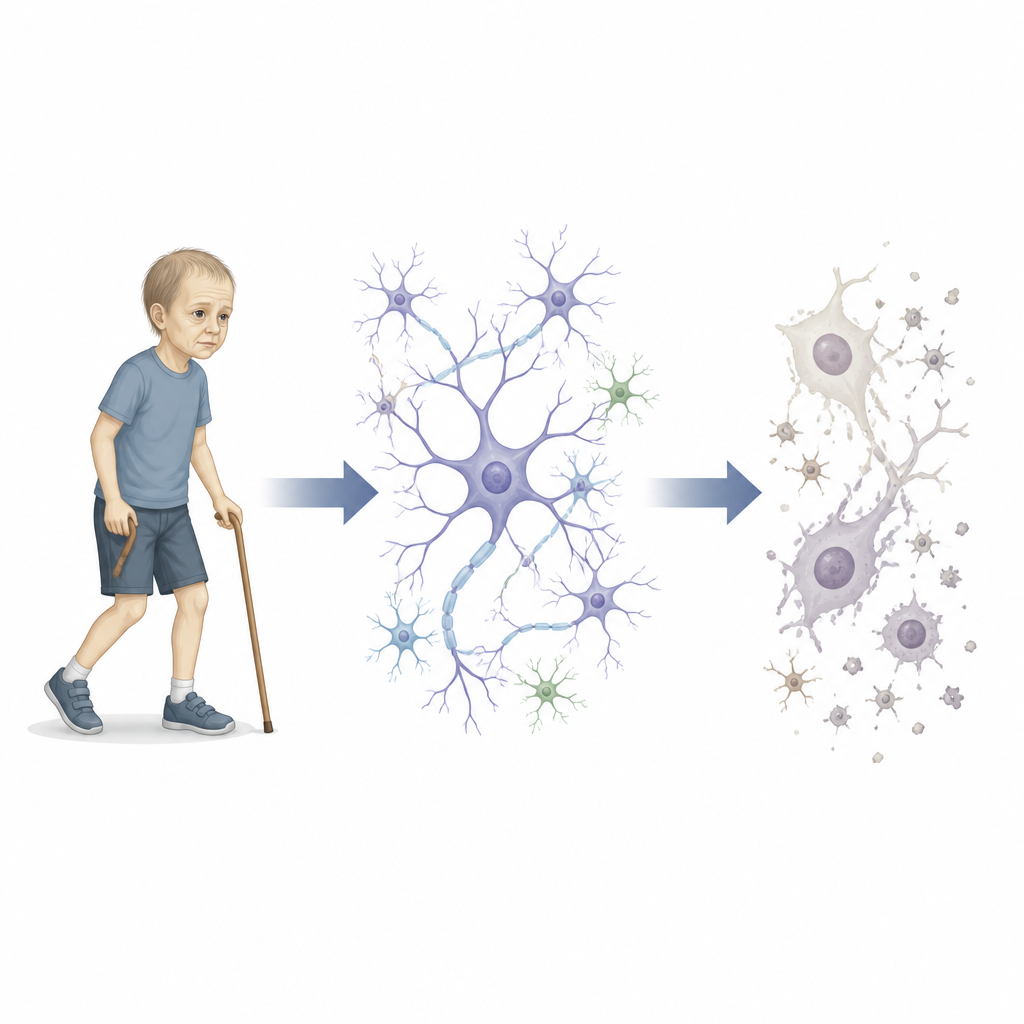
Ricreare la malattia in coltura
Per studiare il disturbo in modo sicuro e dettagliato, il gruppo ha riprogrammato cellule della pelle di pazienti e parenti non affetti in cellule staminali pluripotenti indotte, poi le ha differenziate in cellule progenitrici neurali, i precursori delle cellule cerebrali. Hanno inoltre usato l’editing genetico per creare coppie isogeniche di cellule identiche dal punto di vista genetico eccetto per la singola mutazione IVNS1ABP, e persino knockout completi del gene. In cellule dei pazienti, staminali editate e nei loro discendenti neurali è apparso lo stesso schema: le cellule si dividevano più lentamente, trascorrevano più tempo in ciascuna fase del ciclo cellulare e spesso fallivano nello scindersi nettamente in due cellule figlie.
Cellule che mostrano segni di vecchiaia
Le cellule difettose portavano marcatori classici dell’invecchiamento cellulare. Accumularono danni al DNA, evidenziati da segnali molecolari che segnano cromosomi rotti o sotto stress. I marchi di cromatina protettivi che aiutano a mantenere il DNA organizzato risultarono ridotti, mentre il nucleo spesso aumentava di volume. Molte cellule risultarono positive a una colorazione comunemente usata per l’invecchiamento e attivarono p16 e geni correlati che impongono l’arresto permanente della crescita. Coltivate come “mini-cervelli” tridimensionali chiamati organoidi cerebrali, le progenitrici neurali mutanti uscirono precocemente dal ciclo cellulare e si trasformarono in neuroni prima del previsto. Questi organoidi erano più piccoli e presentavano zone di precursori in divisione più sottili ma strati di neuroni più maturi e spessi, suggerendo che la riserva di cellule “seme” destinata a costruire il cervello si stava esaurendo troppo rapidamente.
Come un aiuto del citoscheletro va in crisi
Approfondendo, gli scienziati hanno indagato quali proteine normalmente interagiscono con IVNS1ABP. Usando esperimenti di pull-down e spettrometria di massa, hanno trovato che la proteina sana interagisce fortemente con l’actina e con un gruppo di proteine associate all’actina che aiutano a costruire e rimodellare l’impalcatura interna della cellula. Al contrario, la forma mutata legava male questi partner. In saggi in provetta, IVNS1ABP normale favoriva efficacemente l’assemblaggio dei filamenti di actina, mentre la versione mutata era molto più debole e non si legava bene nemmeno a dosi maggiori. Nelle progenitrici neurali mutanti, l’equilibrio si spostò lontano dall’actina filamentosa robusta verso la sua forma monomerica libera, e l’anello di actina che normalmente si contrae per separare una cellula in divisione divenne sottile e irregolare. 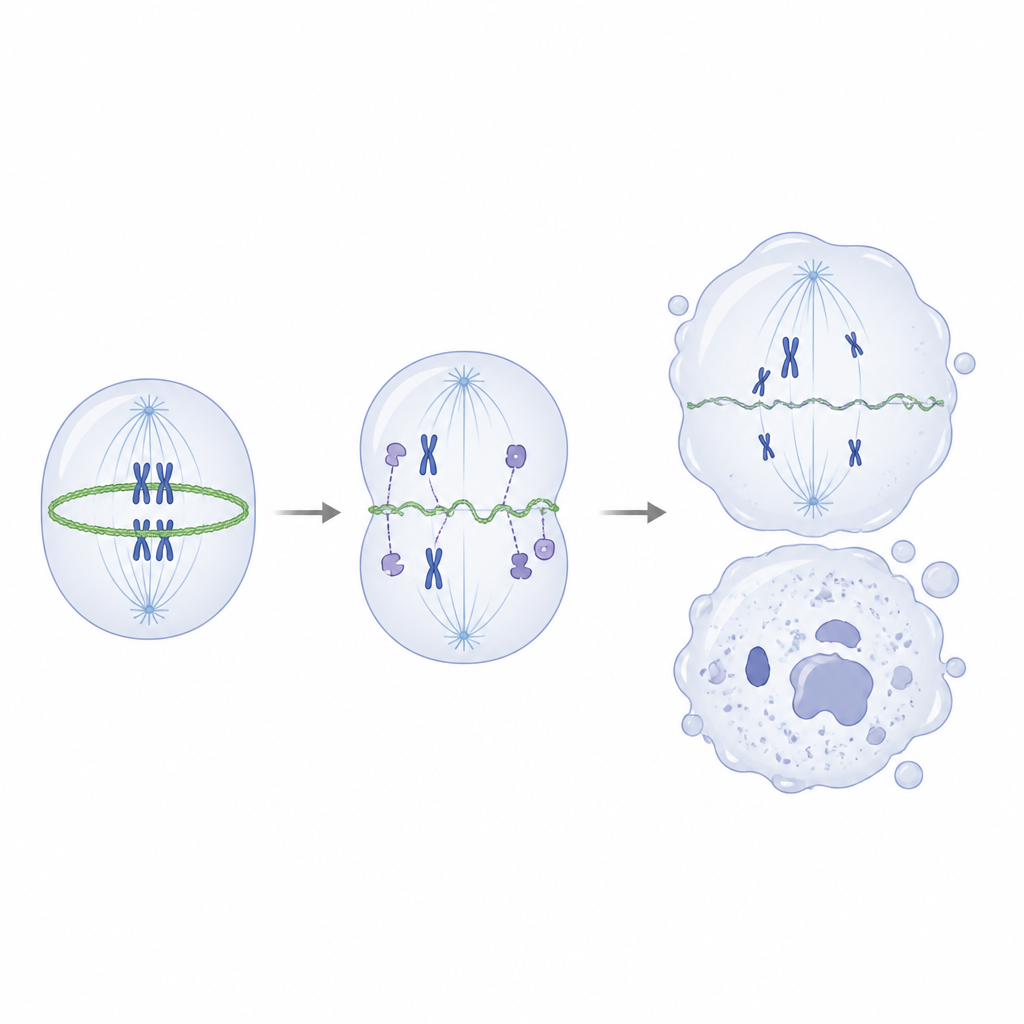
Da divisioni cellulari difettose a invecchiamento nervoso precoce
Questa impalcatura difettosa durante la divisione portò a cromosomi disallineati, fusi anomali e divisioni cellulari diseguali, che a loro volta produssero danni al DNA e spinsero le cellule in uno stato senescente e non-dividente. Importante, quando i ricercatori usarono una bassa dose di un farmaco che promuove l’assemblaggio dell’actina, riuscirono a ripristinare parzialmente l’equilibrio dell’actina, migliorare la forma dell’anello contrattile, ridurre gli errori di divisione e attenuare i marcatori di danno al DNA e di invecchiamento cellulare, anche se la mutazione genica rimaneva presente. Negli organoidi cerebrali lo stesso trattamento recuperò in parte la crescita e la riserva di progenitori neurali. In termini semplici, la conclusione è che questa rara condizione infantile deriva da un singolo gene che normalmente aiuta a gestire l’impalcatura interna della cellula durante la divisione. Quando quel fattore viene meno, le cellule nervose in sviluppo si dividono male, si esauriscono precocemente e invecchiano troppo presto, con conseguente riduzione e indebolimento dei neuroni e, in ultima analisi, comparsa sia di caratteristiche di invecchiamento precoce sia di problemi di movimento e cognizione.
Citazione: Yuan, F., Tan, Y.S., Wang, H. et al. IVNS1ABP mutation drives cellular senescence in newly identified progeroid neuropathy. Nat Commun 17, 4159 (2026). https://doi.org/10.1038/s41467-026-70756-x
Parole chiave: senescenza cellulare, neuropatia progeroide, IVNS1ABP, dinamiche dell’actina, cellule progenitrici neurali