Clear Sky Science · sv
IVNS1ABP‑mutation driver cellulär senescens i nyupptäckt progeroid neuropati
När nerver blir gamla för tidigt
Vissa barn visar tecken på åldrande långt före sin tid: grått hår, skör hud och gångsvårigheter redan under skolålder. Denna studie undersöker ett sådant nyskrivet tillstånd, spårar det från ett enda fel i en gen till åldrande hjärnceller och ger en inblick i hur vårt nervsystem kan bli äldre även hos oss alla.
En ny form av tidigt åldrandesjukdom
Forskarna beskriver en familj där flera tonåringar utvecklade en sällsynt ”progeroid neuropati”. Dessa unga personer hade fläckig hud, för tidigt grånande hår, gångsvårigheter och intellektuell funktionsnedsättning, tillsammans med förtunning av viktiga hjärnstrukturer. Genom DNA‑sekvensering fann man att de drabbade syskonen bar två kopior av en sällsynt förändring i genen IVNS1ABP. Denna gen var tidigare mest känd för sin roll i hur celler hanterar influensavirus, inte för åldrande eller nervsjukdom. Teamet satte igång för att ta reda på hur denna mutation kan få celler och nervsystemet att verka äldre än de borde. 
Återskapa sjukdomen i en skål
För att studera sjukdomen säkert och i detalj omprogrammerade teamet patienters hudceller och friska släktingars celler till inducerade pluripotenta stamceller, och styrde dessa till neurala progenitorceller, hjärncellernas föregångare. De använde också genredigering för att skapa isogena cellpar som var genetiskt identiska utom för den enda IVNS1ABP‑mutationen, och gjorde även kompletta gen‑knockouter. I patientceller, redigerade stamceller och deras neurala efterföljare framträdde samma bild: cellerna delade sig långsammare, tillbringade längre tid i varje fas av cellcykeln och misslyckades ofta med att dela sig rent i två dotterceller.
Celler som visar tecken på ålderdom
De defekta cellerna bar klassiska kännetecken för cellulärt åldrande. De samlade på sig DNA‑skador, synliga genom molekylära markörer som indikerar brutna eller stressade kromosomer. Skyddande kromatinmarkörer som hjälper till att hålla DNA organiserat var reducerade, samtidigt som cellkärnan ofta blev större. Många celler blev positiva för ett vanligt använt åldringsfärgämne och slog på p16 och närliggande gener som upprätthåller permanent tillväxthämning. När de odlades som tredimensionella ”mini‑hjärnor”, så kallade cerebrala organoider, lämnade mutanta neurala progenitorer cellcykeln tidigt och differentierade till neuroner i förtid. Dessa organoider var mindre med tunnare zoner av delande precursorceller men tjockare lager av mer mogna neuroner, vilket tyder på att gruppen av ”fröceller” som ska bygga hjärnan förbrukades för snabbt.
Hur en cytoskelettshjälpare går fel
När forskarna grävde djupare frågade de vilka proteiner som normalt samarbetar med IVNS1ABP. Med pull‑down‑experiment och masspektrometri fann de att det friska proteinet starkt interagerar med aktin och en grupp aktinassocierade proteiner som bygger och remodellerar cellens inre stomme. Den mutanta formen band däremot dåligt till dessa partner. I test‑rörsförsök främjade normalt IVNS1ABP effektivt bildandet av aktinfilament, medan den mutanta varianten var mycket svagare och inte band väl ens vid högre koncentrationer. Inuti mutanta neurala progenitorer försköts balansen bort från stabilt filamentöst aktin mot dess lösa, enhetsform, och aktinringen som normalt drar ihop sig för att snörpa av en delande cell blev tunn och ojämn. 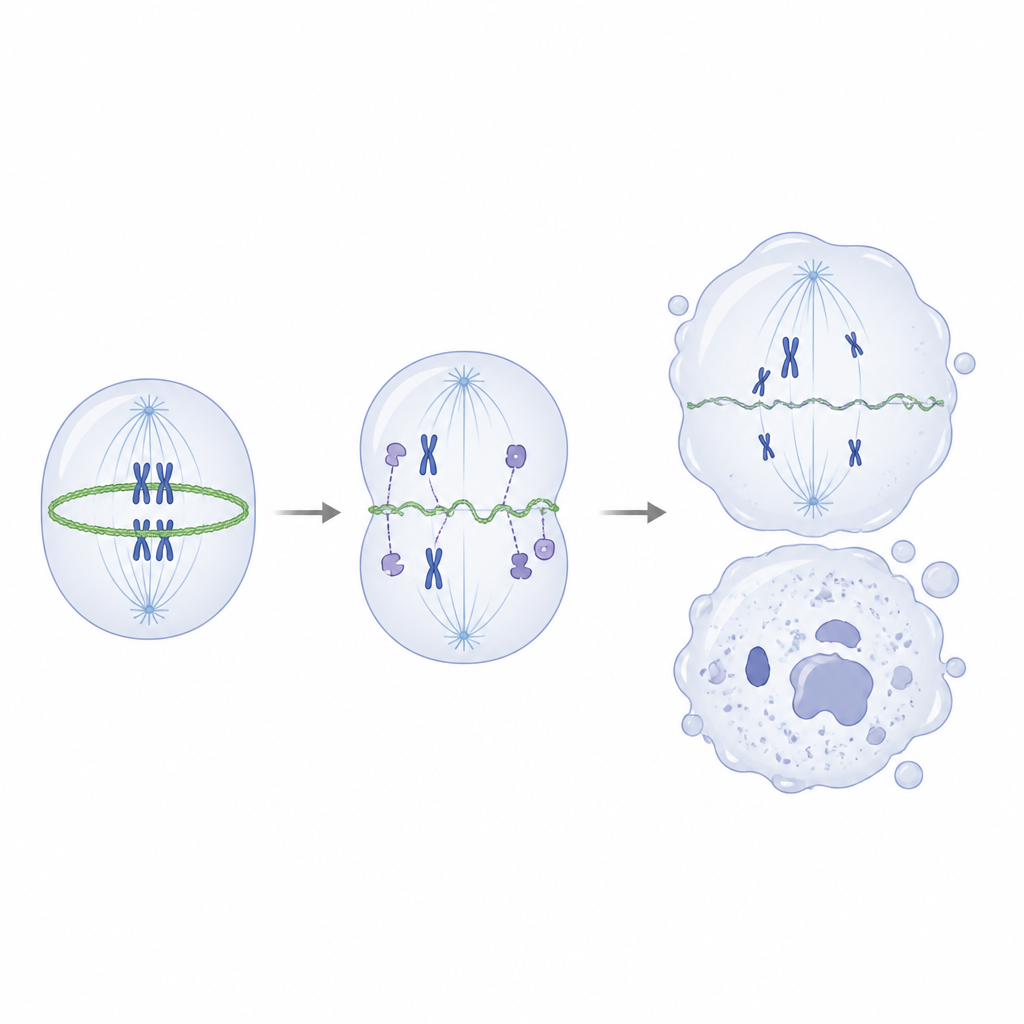
Från trasiga celldelningar till tidigt nervåldrande
Denne defekta stomme vid delning ledde till felställda kromosomer, abnorma spindlar och ojämna celldelningar, vilket i sin tur gav DNA‑skador och drev cellerna in i ett senescent, icke‑delande tillstånd. Viktigt är att när forskarna använde en låg dos av ett läkemedel som främjar aktinsammansättning kunde de delvis återställa aktinbalansen, förbättra formen på kontraktilringen, minska delningsfel och reducera markörer för DNA‑skada och cellulärt åldrande, trots att genmutationen fanns kvar. I cerebrala organoider räddade samma behandling delvis tillväxten och reserven av neurala progenitorer. För en lekmannare är slutsatsen att detta sällsynta barndomstillstånd härrör från en enda gen som normalt hjälper till att hantera cellens inre stomme under delning. När den hjälparen sviktar delar utvecklande nervceller sig dåligt, bränner ut sig tidigt och åldras för tidigt, vilket leder till färre och svagare neuroner och i förlängningen både tidiga åldersdrag och problem med rörelse och tänkande.
Citering: Yuan, F., Tan, Y.S., Wang, H. et al. IVNS1ABP mutation drives cellular senescence in newly identified progeroid neuropathy. Nat Commun 17, 4159 (2026). https://doi.org/10.1038/s41467-026-70756-x
Nyckelord: cellulär senescens, progeroid neuropati, IVNS1ABP, aktin‑dynamik, neurala progenitorceller