Clear Sky Science · pt
Mutação IVNS1ABP provoca senescência celular em neuropatia progeroide recém-identificada
Quando os nervos envelhecem cedo demais
Algumas crianças apresentam sinais de envelhecimento bem antes do esperado, desenvolvendo cabelos grisalhos, pele frágil e dificuldade para caminhar ainda na escola. Este estudo investiga uma dessas condições recém-identificadas, traçando-a desde um único gene defeituoso até as células cerebrais envelhecidas, e oferecendo uma janela sobre como o nosso sistema nervoso pode envelhecer em todos nós.
Um novo tipo de distúrbio de envelhecimento precoce
Os pesquisadores descrevem uma família em que vários adolescentes desenvolveram uma rara “neuropatia progeroide”. Esses jovens apresentavam pele malhada, envelhecimento prematuro dos cabelos, problemas de marcha e deficiência intelectual, além de afinamento de estruturas cerebrais importantes. Ao sequenciarem o DNA, os cientistas descobriram que os irmãos afetados carregavam duas cópias de uma alteração rara no gene chamado IVNS1ABP. Esse gene era conhecido principalmente por seu papel em como as células lidam com o vírus da gripe, não por envelhecimento ou doenças nervosas. A equipe decidiu investigar como essa mutação poderia fazer com que células e o sistema nervoso parecessem envelhecidos antes do tempo. 
Recriando a doença em cultura
Para estudar o distúrbio de forma segura e detalhada, a equipe reprogramou células da pele de pacientes e parentes não afetados em células-tronco pluripotentes induzidas, e então as direcionou para células progenitoras neurais, os precursores das células cerebrais. Eles também usaram edição genética para criar pares “isogênicos” de células geneticamente idênticas, exceto pela única mutação em IVNS1ABP, e até produziram nocaute completo do gene. Em células de pacientes, células-tronco editadas e seus descendentes neurais, apareceu o mesmo padrão: as células se dividiam mais lentamente, passavam mais tempo em cada fase do ciclo celular e frequentemente falhavam em se separar limpidamente em duas filhas.
Células mostrando sinais de idade
As células defeituosas exibiam marcas clássicas de envelhecimento celular. Acumularam danos no DNA, como indicado por sinais moleculares que marcam cromossomos quebrados ou estressados. Marcas protetoras na cromatina que ajudam a manter o DNA organizado foram reduzidas, enquanto o núcleo costumava aumentar de tamanho. Muitas células ficaram positivas em uma coloração amplamente usada para envelhecimento e ativaram p16 e genes relacionados que impõem parada permanente do crescimento. Quando cultivadas como “mini-cérebros” tridimensionais chamados organoides cerebrais, os progenitores neurais mutantes saíram do ciclo celular cedo e se transformaram em neurônios antes do previsto. Esses organoides eram menores e tinham zonas de células precursoras em divisão mais finas, mas camadas mais espessas de neurônios mais maduros, sugerindo que o reservatório de células “semente” que deveria construir o cérebro estava sendo consumido rápido demais.
Como um ajudante do citoesqueleto falha
Ao aprofundar, os cientistas investigaram quais proteínas normalmente se associam ao IVNS1ABP. Usando experimentos de pull-down e espectrometria de massa, encontraram que a proteína saudável interage fortemente com a actina e um grupo de proteínas associadas à actina que ajudam a construir e remodelar o arcabouço interno da célula. Em contraste, a forma mutante ligava-se mal a esses parceiros. Em ensaios in vitro, o IVNS1ABP normal promovia a montagem de filamentos de actina de forma eficiente, enquanto a versão mutante era muito mais fraca e falhava em se ligar bem mesmo em quantidades maiores. Dentro de progenitores neurais mutantes, o equilíbrio inclinou-se para longe da actina filamentosa robusta em direção à sua forma solta, monomérica, e o anel de actina que normalmente se contrai para apertar uma célula em divisão tornou-se fino e irregular. 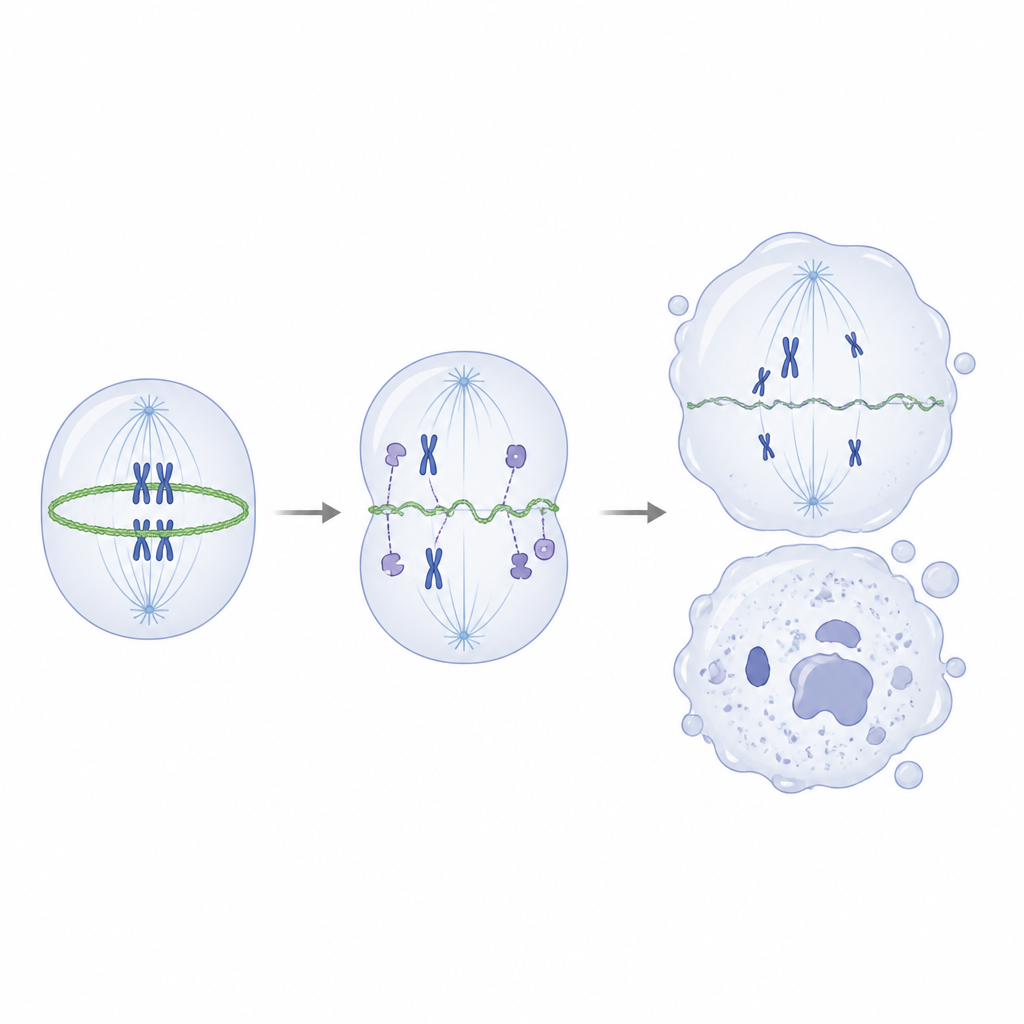
De divisões celulares defeituosas ao envelhecimento precoce dos nervos
Esse arcabouço defeituoso durante a divisão levou a cromossomos desalinhados, fusos anormais e divisões celulares desiguais, o que por sua vez produziu danos no DNA e empurrou as células para um estado senescente, sem divisão. Importante, quando os pesquisadores usaram uma baixa dose de um fármaco que promove a montagem de actina, conseguiram restaurar parcialmente o equilíbrio da actina, melhorar a forma do anel contrátil, reduzir erros de divisão e diminuir marcadores de danos no DNA e envelhecimento celular, mesmo com a mutação genética presente. Em organoides cerebrais, o mesmo tratamento resgatou parcialmente o crescimento e o reservatório de progenitores neurais. Para um leitor leigo, a conclusão é que essa condição rara da infância decorre de um único gene que normalmente ajuda a gerenciar o arcabouço interno da célula durante a divisão. Quando esse ajudante falha, as células nervosas em desenvolvimento se dividem mal, se esgotam cedo e envelhecem prematuramente, levando a neurônios menos numerosos e mais fracos e, por fim, tanto a características de envelhecimento precoce quanto a problemas de movimento e cognição.
Citação: Yuan, F., Tan, Y.S., Wang, H. et al. IVNS1ABP mutation drives cellular senescence in newly identified progeroid neuropathy. Nat Commun 17, 4159 (2026). https://doi.org/10.1038/s41467-026-70756-x
Palavras-chave: senescência celular, neuropatia progeroide, IVNS1ABP, dinâmica da actina, células progenitoras neurais