Clear Sky Science · de
IVNS1ABP-Mutation treibt zelluläre Seneszenz in neu identifizierter progeroider Neuropathie
Wenn Nerven zu früh altern
Manche Kinder zeigen Zeichen des Alterns lange vor ihrer Zeit: graue Haare, empfindliche Haut und Gangstörungen bereits während der Schulzeit. Diese Studie untersucht eine solche neu identifizierte Erkrankung, verfolgt ihren Weg von einem einzigen fehlerhaften Gen bis zu alternden Hirnzellen und bietet Einblicke, wie unser Nervensystem bei uns allen altern könnte.
Eine neue Form der frühzeitigen Alterserkrankung
Die Forscher beschreiben eine Familie, in der mehrere Jugendliche eine seltene „progeroide Neuropathie“ entwickelten. Diese jungen Menschen hatten gesprenkelte Haut, vorzeitiges Ergrauen, Gehprobleme und geistige Beeinträchtigungen sowie eine Ausdünnung wichtiger Hirnstrukturen. Durch DNA-Analysen fanden die Wissenschaftler heraus, dass die betroffenen Geschwister jeweils zwei Kopien einer seltenen Veränderung im Gen IVNS1ABP trugen. Dieses Gen war zuvor hauptsächlich für seine Rolle im Umgang der Zelle mit dem Grippevirus bekannt, nicht für Altern oder Nervenerkrankungen. Das Team machte sich daran zu untersuchen, wie diese Mutation Zellen und das Nervensystem vorzeitig altern lassen kann. 
Die Erkrankung im Reagenzglas nachbilden
Um die Erkrankung sicher und detailliert zu studieren, reprogrammierte das Team Hautzellen von Patienten und gesunden Verwandten zu induzierten pluripotenten Stammzellen und leitete diese dann zu neuralen Vorläuferzellen, den Vorläufern von Hirnzellen. Außerdem nutzten sie Geneditierung, um isogene Zellpaare zu erzeugen, die genetisch identisch waren bis auf die einzelne IVNS1ABP-Mutation, und stellten sogar vollständige Gen-Knockouts her. In Patienten-Zellen, editierten Stammzellen und ihren neuronalen Nachkommen zeigte sich dasselbe Muster: Die Zellen teilten sich langsamer, verbrachten länger in den einzelnen Phasen des Zellzyklus und scheiterten häufig daran, sich sauber in zwei Tochterzellen zu teilen.
Zellen mit Altersmerkmalen
Die fehlerhaften Zellen trugen klassische Kennzeichen zellulären Alterns. Sie akkumulierten DNA-Schäden, sichtbar an molekularen Markern für gebrochene oder gestresste Chromosomen. Schützende Chromatin-Marken, die helfen, DNA geordnet zu halten, waren reduziert, während der Zellkern selbst oft größer wurde. Viele Zellen zeigten positiv einen weithin verwendeten Altersfarbstoff und schalteten p16 und verwandte Gene ein, die ein dauerhaftes Wachstum anhalten. In dreidimensionalen „Mini-Gehirnen“, sogenannten zerebralen Organoiden, verließen mutante Vorläuferzellen den Zellzyklus früh und differenzierten vorzeitig zu Neuronen. Diese Organoide waren kleiner und hatten dünnere Zonen teilender Vorläufer, aber dickere Schichten reiferer Neuronen, was darauf hindeutet, dass der Vorrat an „Saat“-Zellen, der das Gehirn aufbauen sollte, zu schnell aufgebraucht wurde.
Wie ein zytoskelettaler Helfer fehlgeht
Bei tiefer gehender Untersuchung fragten die Wissenschaftler, welche Proteine normalerweise mit IVNS1ABP zusammenarbeiten. Mithilfe von Pull-down-Experimenten und Massenspektrometrie fanden sie, dass das gesunde Protein stark mit Actin und einer Gruppe von Actin-assoziierten Proteinen interagiert, die beim Aufbau und Umbau des inneren Zellgerüsts helfen. Im Gegensatz dazu band die mutante Form diese Partner schlecht. In Testrohr-Assays förderte normales IVNS1ABP effizient die Assemblierung von Actinfilamenten, während die mutante Version deutlich schwächer war und selbst in höheren Mengen nur schlecht bindete. In mutanten neuralen Vorläuferzellen verschob sich das Gleichgewicht weg von stabilem filamentösem Actin hin zu seiner lockeren, monomeren Form, und der Actinring, der sich normalerweise zusammenzieht, um eine teilende Zelle in zwei zu spalten, wurde dünn und ungleichmäßig. 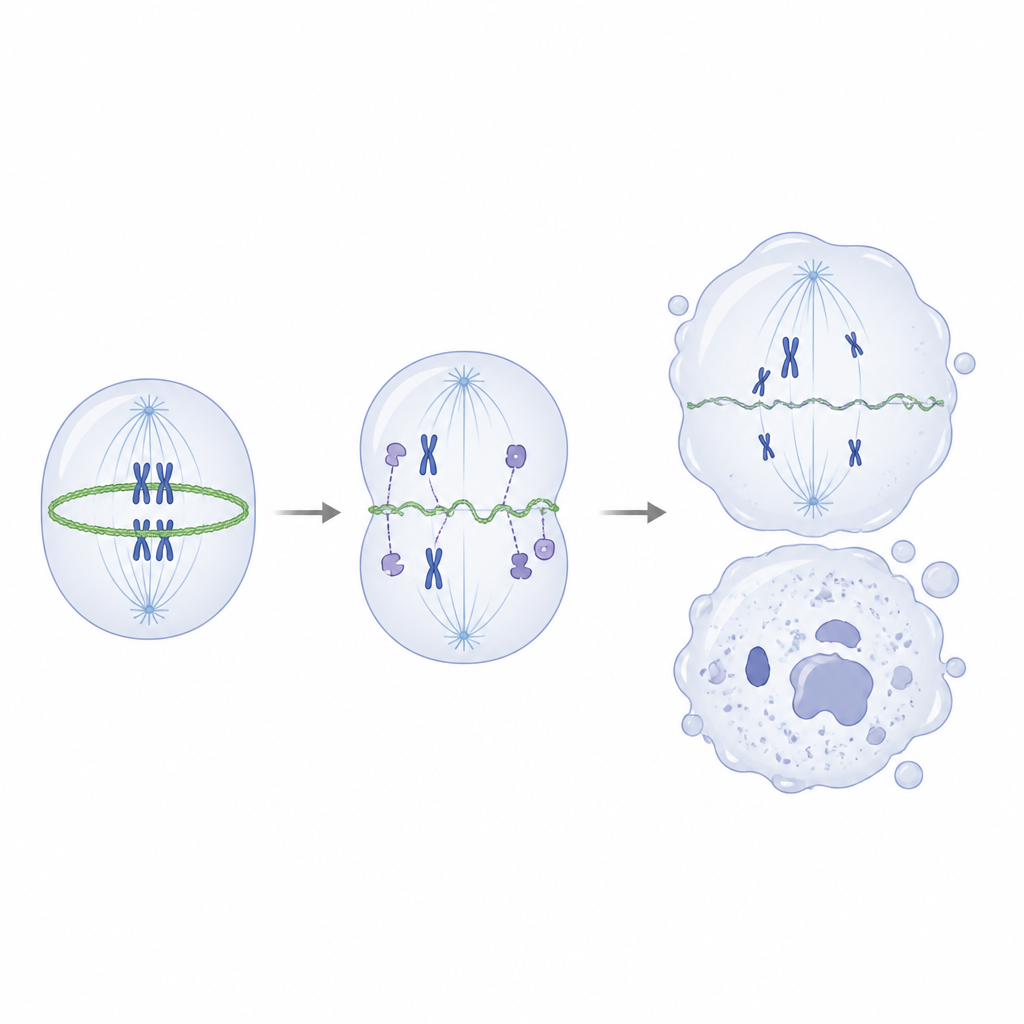
Von fehlerhaften Zellteilungen zu frühem Nervenaltern
Dieses beschädigte Gerüst während der Teilung führte zu fehl ausgerichteten Chromosomen, abnormen Spindeln und ungleichmäßigen Zellteilungen, was wiederum DNA-Schäden erzeugte und die Zellen in einen seneszenten, nicht teilenden Zustand drängte. Wichtig ist, dass die Forscher durch Gabe einer niedrigen Dosis eines Wirkstoffs, der die Actin-Assemblierung fördert, das Actin-Gleichgewicht teilweise wiederherstellen, die Form des kontraktilen Rings verbessern, Teilungsfehler reduzieren und Marker für DNA-Schäden und zelluläres Altern verringern konnten, obwohl die Genmutation bestehen blieb. In zerebralen Organoiden verbesserte dieselbe Behandlung teilweise das Wachstum und den Vorrat an neuralen Vorläufern. Für Laien lautet die Schlussfolgerung, dass diese seltene Kindheitskrankheit von einem einzelnen Gen herrührt, das normalerweise hilft, das innere Gerüst der Zelle während der Teilung zu steuern. Versagt dieser Helfer, teilen sich sich entwickelnde Nervenzellen schlecht, verbrauchen sich vorzeitig und altern zu früh, was zu weniger und schwächeren Neuronen und letztlich zu frühen Altersmerkmalen sowie Problemen mit Bewegung und Denken führt.
Zitation: Yuan, F., Tan, Y.S., Wang, H. et al. IVNS1ABP mutation drives cellular senescence in newly identified progeroid neuropathy. Nat Commun 17, 4159 (2026). https://doi.org/10.1038/s41467-026-70756-x
Schlüsselwörter: zelluläre Seneszenz, progeroide Neuropathie, IVNS1ABP, Actin-Dynamik, neurale Vorläuferzellen