Clear Sky Science · es
La mutación IVNS1ABP provoca senescencia celular en una neuropatía progeroide recién identificada
Cuando los nervios envejecen demasiado pronto
Algunos niños muestran signos de envejecimiento mucho antes de su tiempo: canas, piel frágil y dificultad para caminar mientras aún están en edad escolar. Este estudio investiga una de estas condiciones recién identificadas, rastreándola desde un solo gen defectuoso hasta las células cerebrales envejecidas, y ofrece una ventana sobre cómo puede envejecer el sistema nervioso en todos nosotros.
Un nuevo tipo de trastorno de envejecimiento precoz
Los investigadores describen una familia en la que varios adolescentes desarrollaron una rara “neuropatía progeroide”. Estos jóvenes presentaban piel moteada, canas prematuras, problemas para caminar y discapacidad intelectual, junto con adelgazamiento de estructuras cerebrales clave. Al analizar su ADN, los científicos encontraron que los hermanos afectados portaban dos copias de una variante rara en un gen llamado IVNS1ABP. Este gen se conocía principalmente por su papel en la interacción celular con el virus de la gripe, no por envejecimiento o enfermedad nerviosa. El equipo se propuso descubrir cómo esta mutación podía hacer que las células y el sistema nervioso parecieran viejos antes de tiempo. 
Recrear la enfermedad en el laboratorio
Para estudiar el trastorno de forma segura y detallada, el equipo reprogramó células de la piel de los pacientes y de familiares no afectados en células madre pluripotentes inducidas, y luego las guió hacia células progenitoras neurales, precursoras de las células cerebrales. También emplearon edición genética para crear pares isogénicos de células que eran genéticamente idénticas salvo por la única mutación en IVNS1ABP, e incluso generaron anulaciones completas del gen. En las células de pacientes, en las células madre editadas y en sus descendientes neuronales apareció el mismo patrón: las células se dividían más despacio, pasaban más tiempo en cada fase del ciclo celular y con frecuencia no lograban separarse limpiamente en dos hijas.
Células mostrando signos de envejecimiento
Las células defectuosas presentaban rasgos clásicos del envejecimiento celular. Acumularon daño en el ADN, evidenciado por marcadores moleculares que señalan cromosomas rotos o estresados. Los marcadores protectores de la cromatina que ayudan a mantener el ADN organizado estaban reducidos, mientras que el núcleo con frecuencia se volvía más grande. Muchas células dieron positivo en una tinción ampliamente usada para envejecimiento y activaron p16 y genes afines que imponen un arresto permanente del crecimiento. Cuando se cultivaron como “mini-cerebros” tridimensionales llamados organoides cerebrales, los progenitores neurales mutantes salieron del ciclo celular temprano y se convirtieron en neuronas antes de lo esperado. Estos organoides eran más pequeños y presentaban zonas de precursores en división más delgadas pero capas más gruesas de neuronas más maduras, lo que sugiere que la reserva de células “semilla” que debería construir el cerebro se estaba agotando demasiado rápido.
Cómo falla un ayudante del citoesqueleto
Al profundizar, los científicos preguntaron qué proteínas normalmente se asocian con IVNS1ABP. Usando experimentos de extracción y espectrometría de masas, encontraron que la proteína sana interactúa fuertemente con la actina y con un grupo de proteínas asociadas a la actina que ayudan a construir y remodelar el andamiaje interno de la célula. En contraste, la forma mutante unía mal a estos socios. En ensayos in vitro, IVNS1ABP normal promovía de forma eficiente el ensamblaje de filamentos de actina, mientras que la versión mutante era mucho más débil y no se unía bien incluso en mayores concentraciones. Dentro de los progenitores neurales mutantes, el equilibrio se inclinó desde la actina filamentosa estable hacia su forma suelta de unidades monoméricas, y el anillo de actina que normalmente se contrae para dividir una célula en dos quedó fino y desigual. 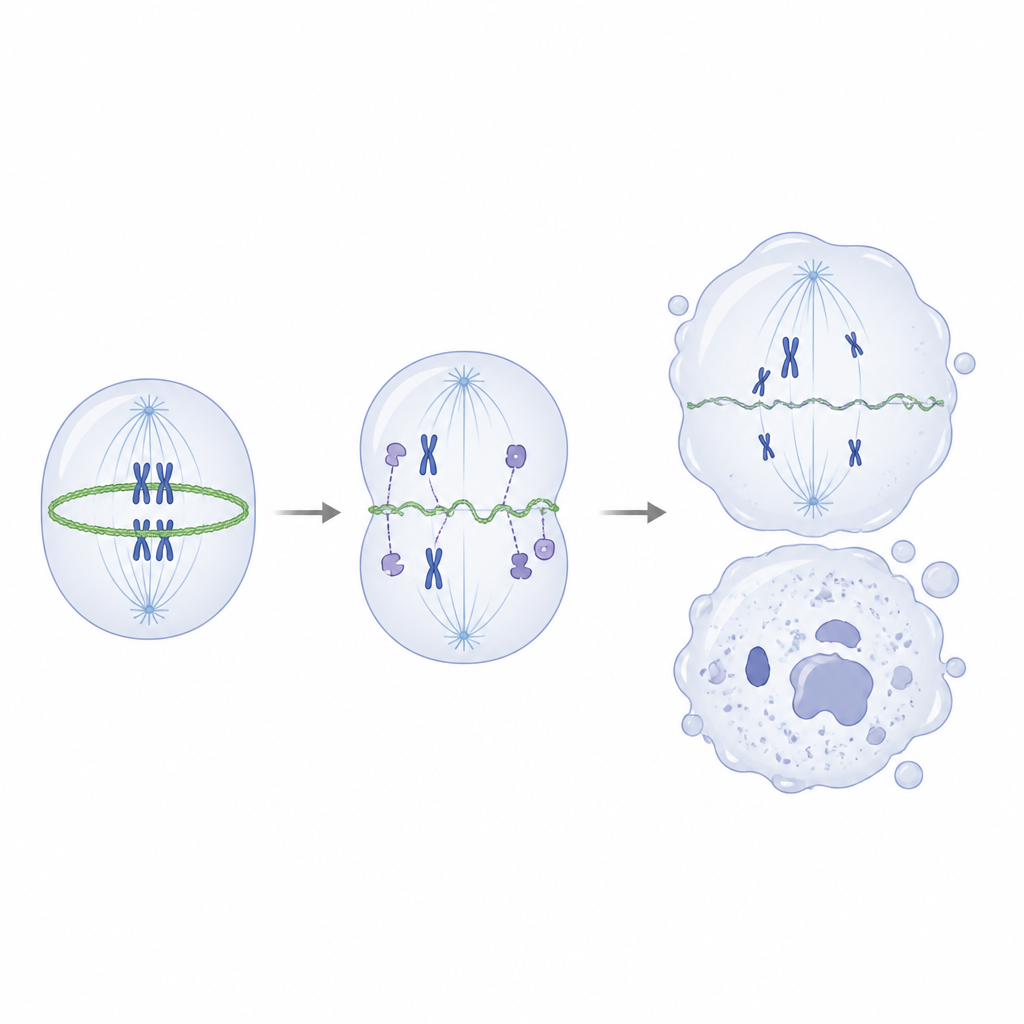
De separaciones celulares defectuosas al envejecimiento nervioso precoz
Este andamiaje defectuoso durante la división condujo a cromosomas mal alineados, husos anormales y divisiones celulares desiguales, lo que a su vez produjo daño en el ADN y empujó a las células hacia un estado senescente y no proliferativo. De forma importante, cuando los investigadores usaron una dosis baja de un fármaco que promueve el ensamblaje de actina, pudieron restaurar parcialmente el equilibrio de la actina, mejorar la forma del anillo contráctil, reducir errores en la división y disminuir marcadores de daño en el ADN y envejecimiento celular, aunque la mutación del gen permaneciera. En organoides cerebrales, el mismo tratamiento rescató en parte el crecimiento y la reserva de progenitores neurales. Para un lector no especialista, la conclusión es que esta rara afección infantil se origina en un solo gen que normalmente ayuda a gestionar el andamiaje interno de la célula durante la división. Cuando ese ayudante falla, las células nerviosas en desarrollo se dividen mal, se agotan prematuramente y envejecen demasiado pronto, lo que conduce a menos neuronas y de menor calidad y, en última instancia, a rasgos de envejecimiento precoz y problemas de movimiento y cognición.
Cita: Yuan, F., Tan, Y.S., Wang, H. et al. IVNS1ABP mutation drives cellular senescence in newly identified progeroid neuropathy. Nat Commun 17, 4159 (2026). https://doi.org/10.1038/s41467-026-70756-x
Palabras clave: senescencia celular, neuropatía progeroide, IVNS1ABP, dinámica de la actina, células progenitoras neurales