Clear Sky Science · tr
IVNS1ABP mutasyonu, yeni tanımlanan progeroid nöropatide hücresel senesansı tetikliyor
Sinirlerin Çok Erken Yaşlanması
Bazı çocuklar, zamanından çok önce yaşlanma belirtileri gösterir; okul çağındayken gri saç, hassas cilt ve yürüme güçlüğü gelişebilir. Bu çalışma, böyle yeni tanımlanmış bir durumu araştırıyor; tek bir hatalı genden başlayıp beyin hücrelerinin yaşlanmasına uzanan süreci izliyor ve sinir sistemimizin hepimizde nasıl erken yaşlanabileceğine dair bir pencere açıyor.
Yeni Bir Erken Yaşlanma Bozukluğu Türü
Araştırmacılar, birkaç ergen bireyde nadir bir “progeroid nöropati” gelişen bir aileyi tanımlıyorlar. Bu gençlerde lekeli cilt, erken saç ağarması, yürüme sorunları ve zihinsel gerilik ile birlikte önemli beyin yapılarını incelten bulgular vardı. DNA taramasıyla, etkilenmiş kardeşlerin hepsinin IVNS1ABP adlı gende nadir bir değişikliğin iki kopyasını taşıdığı bulundu. Bu gen daha önce esas olarak hücrelerin grip virüsünü nasıl işlediğiyle ilişkili olarak biliniyordu; yaşlanma veya sinir hastalıklarıyla pek ilişkilendirilmiyordu. Ekip, bu mutasyonun hücreleri ve sinir sistemini zamanından önce yaşlı göstermesine nasıl yol açabileceğini ortaya çıkarmaya karar verdi. 
Hastalığı Bir Plahta Yeniden Yaratmak
Bozukluğu güvenli ve ayrıntılı şekilde incelemek için ekip, hastalardan ve etkilenmemiş akrabalardan alınan deri hücrelerini indüklenmiş pluripotent kök hücrelere yeniden programladı ve bunları beyin hücrelerinin öncülleri olan sinir progenitör hücrelerine yönlendirdi. Ayrıca, tek bir IVNS1ABP mutasyonu dışında genetik olarak özdeş “izojenik” hücre çiftleri oluşturmak için gen düzenleme kullandılar ve tam gen yoklukları dahi ürettiler. Hasta hücrelerinde, düzenlenmiş kök hücrelerde ve bunların sinir soylarında aynı desen ortaya çıktı: hücreler daha yavaş bölünüyordu, hücre döngüsünün her aşamasında daha uzun süre kalıyorlardı ve sıklıkla iki yavruya temiz bir şekilde ayrılmayı başaramıyorlardı.
Yaşlanma Belirtileri Gösteren Hücreler
Hatalı hücreler hücresel yaşlanmanın klasik işaretlerini taşıyordu. Kırık veya stres altındaki kromozomları işaretleyen moleküler bayraklarla gösterilen DNA hasarı birikti. DNA’yı düzenli tutmaya yardımcı olan koruyucu kromatin işaretleri azaldı ve çekirdek genellikle daha büyük hale geldi. Birçok hücre yaygın kullanılan bir yaşlanma boyasına pozitifleşti ve kalıcı büyüme durdurmayı dayatan p16 ve ilgili genleri açtı. Üç boyutlu “mini-beyin” olarak adlandırılan serebral organoidler olarak büyütüldüğünde, mutan sinir progenitörleri hücre döngüsünden erken çıktı ve zamanından önce nöronlara dönüştü. Bu organoidler daha küçüktü ve bölünen öncü hücre bölgeleri daha incedi, ancak daha olgun nöron katmanları daha kalındı; bu da beyni oluşturması gereken “tohum” hücre havuzunun çok hızlı tükenmekte olduğunu düşündürüyor.
İskelet Yardımcısı Nasıl Bozuluyor
Daha derine inen bilim insanları, IVNS1ABP ile normalde hangi proteinlerin ortak çalıştığını sordu. Çekme deneyleri ve kütle spektrometrisi kullanarak, sağlıklı proteinin aktin ve hücrenin iç iskeletini inşa etmeye ve yeniden şekillendirmeye yardımcı olan aktinle ilişkili bir grup proteinle güçlü etkileşimde olduğunu buldular. Buna karşılık, mutant form bu ortaklarla zayıf bağlanıyordu. Deney tüpü testlerinde normal IVNS1ABP aktin filamentlerinin verimli bir şekilde oluşumunu desteklerken, mutant versiyon çok daha zayıftı ve daha yüksek miktarlarda bile iyi bağlanamadı. Mutant sinir progenitörleri içinde denge sağlam filamentöz aktinden gevşek, tek birimlik forma kaydı ve bölünen bir hücreyi ikiye ayırmak için normalde daralan aktin halkası ince ve düzensiz hâle geldi. 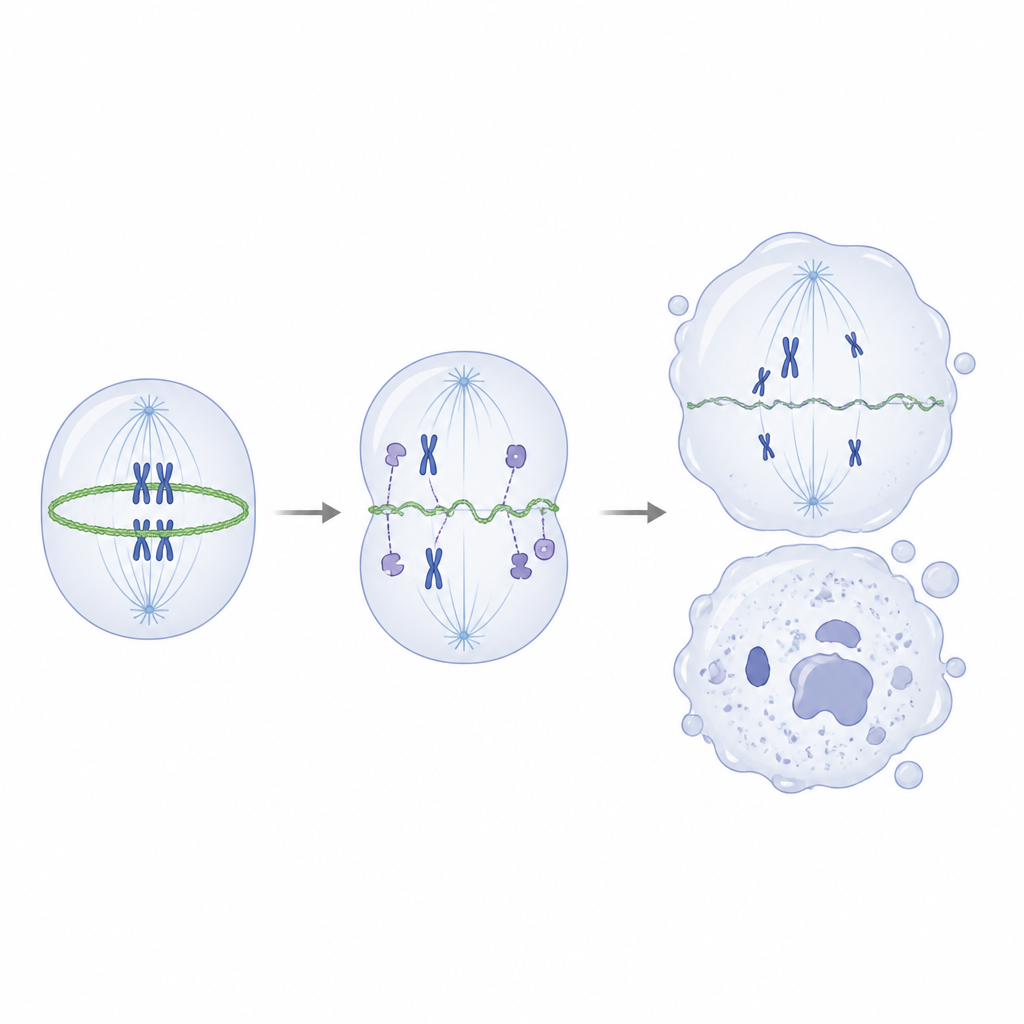
Kırık Hücre Bölünmelerinden Erken Sinir Yaşlanmasına
Bölünme sırasında bu bozuk iskelet yapısı kromozom hizalanmasının bozulmasına, anormal iğcik oluşumuna ve eşitsiz hücre bölünmelerine yol açtı; bu da DNA hasarı üretti ve hücreleri senesans denilen bölünmeyen bir duruma itti. Önemli olarak, araştırmacılar aktin oluşumunu teşvik eden düşük doz bir ilaç kullandıklarında aktin dengesini kısmen geri getirebildiler, kontraktil halkanın şeklini düzeltebildiler, bölünme hatalarını azalttılar ve gen mutasyonu devam etmesine rağmen DNA hasarı ve hücresel yaşlanma belirteçlerini düşürdüler. Serebral organoidlerde aynı tedavi büyümeyi ve sinir progenitör havuzunu kısmen kurtardı. Bir bilim dışı okuyucu için sonuç şudur: bu nadir çocukluk durumu, normalde hücre bölünmesi sırasında hücrenin iç iskeletini yönetmeye yardım eden tek bir genden kaynaklanıyor. O yardımcı işlevini yitirdiğinde, gelişen sinir hücreleri kötü bölünüyor, erken tükeniyor ve çok erken yaşlanıyor; bunun sonucu daha az ve daha zayıf nöron, erken yaşlanma belirtileri ile hareket ve düşünme sorunlarıdır.
Atıf: Yuan, F., Tan, Y.S., Wang, H. et al. IVNS1ABP mutation drives cellular senescence in newly identified progeroid neuropathy. Nat Commun 17, 4159 (2026). https://doi.org/10.1038/s41467-026-70756-x
Anahtar kelimeler: hücresel senesans, progeroid nöropati, IVNS1ABP, aktin dinamiği, sinir progenitör hücreleri