Clear Sky Science · pl
Mutacja IVNS1ABP wywołuje starzenie komórkowe w nowo zidentyfikowanej progeroidowej neuropatii
Kiedy nerwy starzeją się za wcześnie
U niektórych dzieci pojawiają się oznaki starzenia znacznie przed czasem: siwienie włosów, delikatna skóra i problemy z chodzeniem w wieku szkolnym. Badanie to analizuje jedno z takich nowo rozpoznanych schorzeń, śledząc je od pojedynczej usterki genetycznej aż po starzejące się komórki mózgu, i oferuje wgląd w to, jak może wyglądać starzenie się naszego układu nerwowego u wszystkich ludzi.
Nowy rodzaj zaburzenia przedwczesnego starzenia
Naukowcy opisują rodzinę, w której kilku nastolatków rozwinęło rzadką „progeroidową neuropatię”. Młode osoby miały plamistą skórę, przedwczesne siwienie włosów, problemy z chodzeniem i niepełnosprawność intelektualną, a także zanik istotnych struktur mózgowych. Przeskanowawszy ich DNA, badacze znaleźli, że dotknięte rodzeństwo miało dwie kopie rzadkiej zmiany w genie IVNS1ABP. Gen ten był wcześniej znany głównie z roli w reakcji komórek na wirus grypy, a nie z procesów starzenia czy chorób nerwowych. Zespół postanowił ustalić, jak ta mutacja może powodować, że komórki i układ nerwowy wydają się starzeć przedwcześnie. 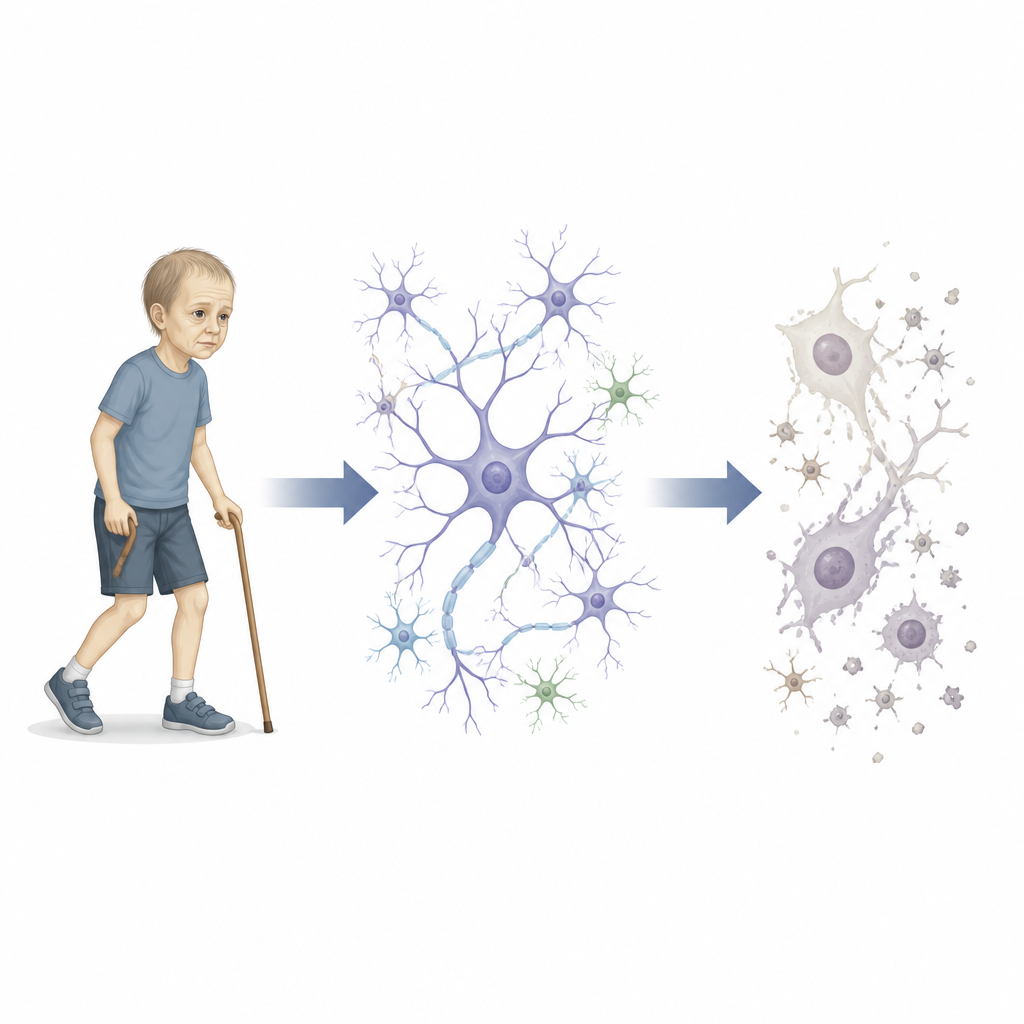
Odtworzenie choroby w laboratorium
Aby bezpiecznie i szczegółowo zbadać zaburzenie, zespół przeprogramował komórki skóry pacjentów i osób nieskażonych na indukowane komórki macierzyste pluripotentne, a następnie skierował je do komórek progenitorowych nerwowych — prekursorów komórek mózgowych. Użyto też edycji genów, by stworzyć izogeniczne pary komórek identyczne genetycznie poza jedną mutacją w IVNS1ABP, a także całkowite wyciszenia genu. We wszystkich badanych komórkach pochodzących od pacjentów, w zmodyfikowanych komórkach macierzystych i w ich neuronalnych potomkach pojawiał się ten sam wzorzec: komórki dzieliły się wolniej, spędzały więcej czasu w każdej fazie cyklu komórkowego i często nie udawało im się równomiernie rozdzielić na dwie komórki potomne.
Komórki wykazujące cechy starości
Uszkodzone komórki nosiły klasyczne cechy starzenia komórkowego. Gromadziły się uszkodzenia DNA, widoczne dzięki molekularnym znacznikom świadczącym o pęknięciach lub stresie chromosomów. Ochronne znaki w chromatynie, które pomagają utrzymać porządek DNA, były osłabione, a sam jądro komórkowe często się powiększało. Wiele komórek reagowało pozytywnie na powszechnie stosowany barwnik starzeniowy i włączało ekspresję p16 oraz powiązanych genów, które wymuszają trwały zahamowany wzrost. W trójwymiarowych „mini-mózgach” zwanych organoidami mózgowymi, mutantowe komórki progenitorowe opuszczały cykl komórkowy wcześniej i przekształcały się w neurony przedwcześnie. Organoidy były mniejsze, miały cieńsze strefy dzielących się prekursorów, ale grubsze warstwy bardziej dojrzałych neuronów, co sugeruje, że pula „nasiennych” komórek budujących mózg wyczerpywała się zbyt szybko.
Jak pomocnik cytoszkieletu zawodzi
Dążyjąc dalej, naukowcy sprawdzili, z którymi białkami normalnie współpracuje IVNS1ABP. Wykorzystując eksperymenty pull-down i spektrometrię mas, stwierdzili, że zdrowe białko silnie wchodzi w interakcje z aktyną oraz grupą białek związanych z aktyną, które pomagają budować i przebudowywać wewnętrzne rusztowanie komórki. Natomiast forma mutantowa słabo wiązała się z tymi partnerami. W testach in vitro normalny IVNS1ABP efektywnie wspierał formowanie filamentów aktynowych, podczas gdy wariant mutantowy był znacznie słabszy i nie wiązał się dobrze nawet przy wyższych stężeniach. W mutantowych komórkach progenitorowych nerwowych równowaga przesunęła się od stabilnej, filamentowej aktyny ku jej luźnej, monomerowej postaci, a pierścień aktynowy, który normalnie obkurcza się, żeby rozdzielić dzielącą się komórkę, stał się cienki i nierówny. 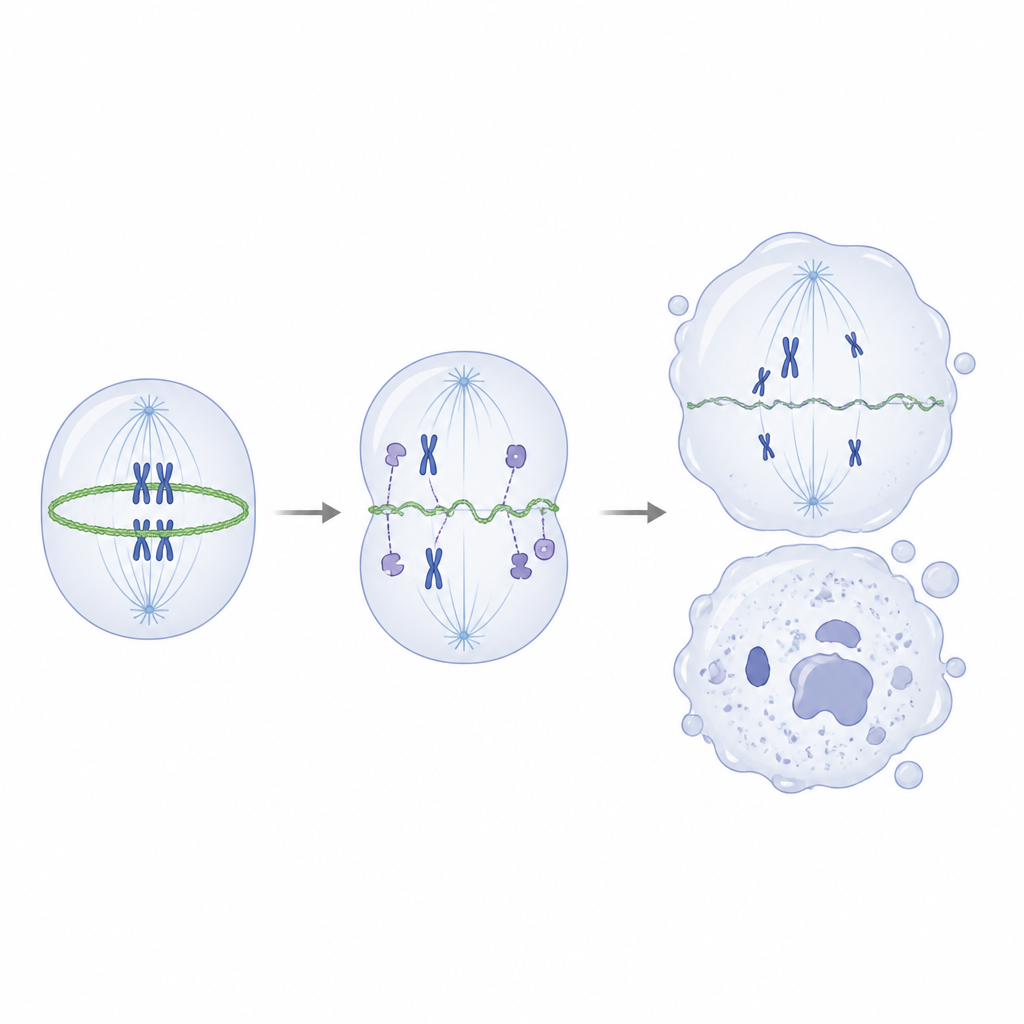
Od wadliwych podziałów komórkowych do przedwczesnego starzenia nerwów
To uszkodzone rusztowanie podczas podziału prowadziło do źle ustawionych chromosomów, nieprawidłowych wrzecion podziałowych i nierównych rozdziałów komórek, co z kolei powodowało uszkodzenia DNA i wpychało komórki w stan senescencji — trwałego zaprzestania podziałów. Co ważne, gdy badacze zastosowali niską dawkę leku pobudzającego składanie aktyny, udało się częściowo przywrócić równowagę aktynową, poprawić kształt pierścienia kurczliwego, zmniejszyć błędy podczas podziału oraz zredukować markery uszkodzeń DNA i starzenia komórkowego, mimo że mutacja genu pozostała. W organoidach mózgowych to samo leczenie częściowo ratowało wzrost i pulę komórek progenitorowych nerwowych. Dla laika wniosek jest taki: to rzadkie dziecięce schorzenie wynika z pojedynczego genu, który normalnie pomaga zarządzać wewnętrznym rusztowaniem komórki podczas podziału. Gdy ten pomocnik zawodzi, rozwijające się komórki nerwowe dzielą się nieprawidłowo, wyczerpują się zbyt wcześnie i starzeją za szybko, co prowadzi do mniejszej liczby i słabszych neuronów, a ostatecznie do przedwczesnych cech starzenia oraz problemów z ruchem i myśleniem.
Cytowanie: Yuan, F., Tan, Y.S., Wang, H. et al. IVNS1ABP mutation drives cellular senescence in newly identified progeroid neuropathy. Nat Commun 17, 4159 (2026). https://doi.org/10.1038/s41467-026-70756-x
Słowa kluczowe: starzenie komórkowe, progeroidowa neuropatia, IVNS1ABP, dynamika aktyny, komórki progenitorowe nerwowe