Clear Sky Science · zh
通过氧化性 SH2 均裂取代实现酮类的交叉去酰偶联
把常见化学品变成灵活的构建模块
化学家依赖一小套简单原料来构筑药物和材料中的复杂分子。本研究展示了如何引导最常见的原料之一——酮类——形成以往难以实现的新键,开辟了更快更精确设计药物样分子的全新途径。
为什么日常酮很重要
酮是有机化学中的主力分子,因易于合成、储存和改造而备受青睐。经典反应如醇醛缩合和 McMurry 偶联已能将酮转化为更复杂的产物,但这些方法常常需要大量金属试剂,且难以以可控方式连接两种不同的反应伙伴。尤其是,在拥挤环境中形成两个饱和碳原子之间的稳固键(即 C–C 单键)一直是重大挑战,尽管这样的拥挤碳中心在许多现代药物中是关键结构。
让两种自由基协同工作的全新途径
作者旨在让两种不同的酮以清晰且有选择性的方式“对话”。他们不是活化酮的常规模糊基团(羰基),而是着眼于断开靠近的碳–碳键以释放小而短寿的碎片——自由基。这些自由基在原理上可以以多种方式重新组合,包括不期望的自偶联或副反应。为驯服这种混乱,团队采用了一种称为 SH2 的策略,这是一种均裂取代形式,其中金属配合物短暂捕获一个自由基,然后被第二个外来自由基攻击。该外场路径有助于指引究竟是哪两块碎片结合。
掩蔽酮以控制其行为
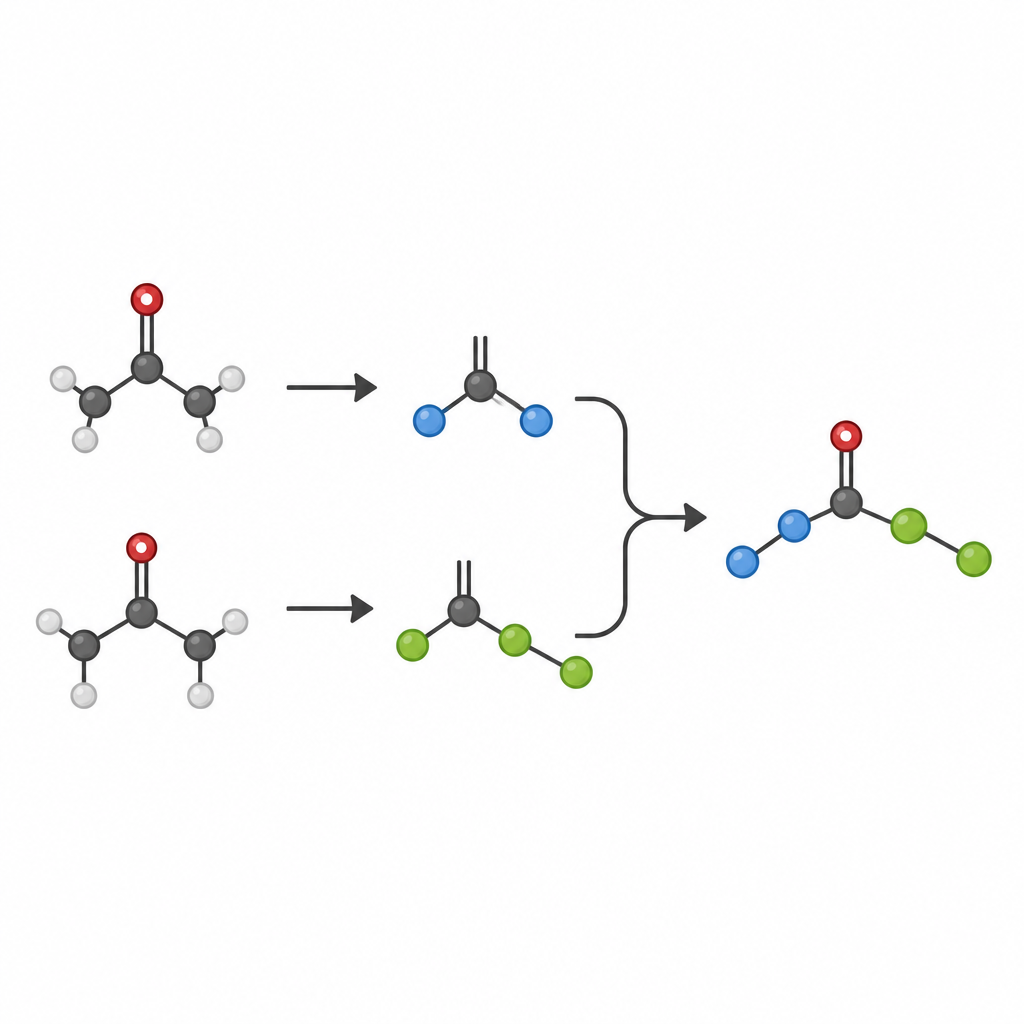
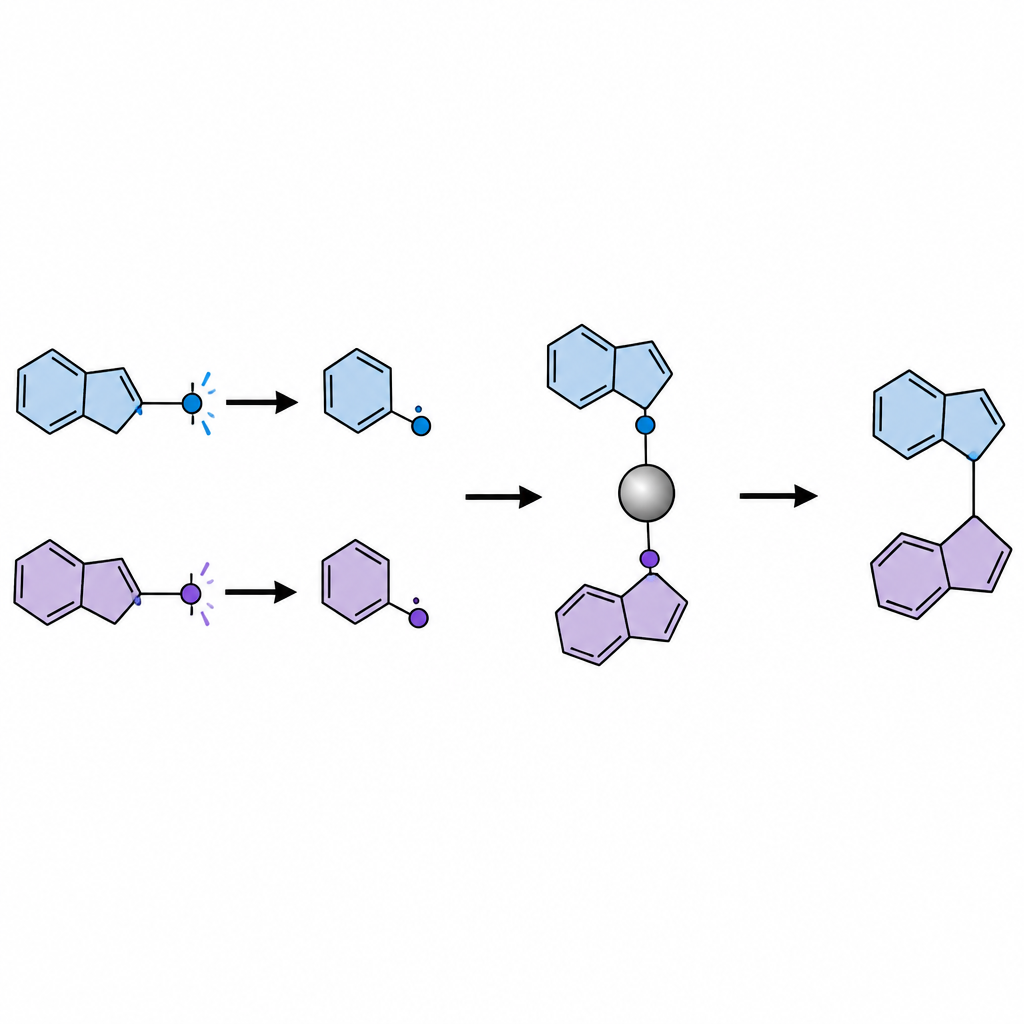
直接用光照射酮常会产生既有用又有害的自由基碎片。为绕过这一问题,研究者先将每个酮在一步操作中转化为在实验台上稳定的“掩蔽”形式——二氢喹唑啉酮。在蓝光下,有机光催化剂氧化这些掩蔽酮,促使其裂解并释放两种不同的自由基:一个更小且空间阻碍小的初级碎片,以及一个体积更大、二级或三级的碎片。镍催化剂选择性捕获较小的自由基形成持久的镍–碳络合物,而较大自由基则保持游离在溶液中。由于镍–初级键的形成比镍–三级键更为有利,体系自发地将自由基分配到不同角色。
为药物样分子构建拥挤碳中心
一旦组装完成,镍–初级络合物在 SH2 步被更大自由基攻击,形成新的碳–碳键并再生镍催化剂。利用这一方法,团队构建了多种产物,这些产物在氮、氧或硫原子邻位含有一个拥挤的四取代碳中心。包括 β-季胺、β-氨醇、β-二胺、β-氨硫醇及相关醚类,均为生物活性化合物中常见的基元。该反应耐受多种官能团,如烯烃、酯、卤素和环状体系,并在可见光下的温和条件下进行。作者还展示了此方法可以在已知药物分子的合成后期应用,温和地修饰其结构而不干扰其他敏感部分。
窥探反应机理
为理解该过程,研究者捕获瞬时自由基、研究光吸收催化剂的猝灭,并计算关键步骤的相对速率与能量。他们的证据指向这样一个机理:两种自由基来自掩蔽酮的氧化,而非过氧化物氧化剂,并且镍保持在较高的氧化态,从而避免了会与芳基卤化物反应的典型内场配位交叉偶联路径。计算显示镍–初级络合物的形成在能量上更有利,且两种自由基以相近速率生成,这些条件抑制了不期望的自偶联并有利于期望的交叉配对。
这对未来分子构建意味着什么
简单来说,这项工作教会了酮一种新技巧:如何以可控方式断裂,使得正确的碎片重新组合成新的、更复杂的结构。通过结合可见光、镍催化和巧妙的掩蔽酮,作者们创造了一条通用且灵活的通路,可构建在药物发现中备受重视的拥挤碳中心。该策略为化学家的工具箱增添了强有力的手段,便于在分子编辑和多样化中使用,尤其是在合成后期,小的改动可能对生物活性产生重大影响。
引用: Yang, JX., Zhang, MY., Wen, Q. et al. Cross-ketone deacylative coupling via oxidative SH2 homolytic substitution. Nat Commun 17, 4248 (2026). https://doi.org/10.1038/s41467-026-70619-5
关键词: 酮类偶联, 自由基化学, 镍催化, 光氧化还原, 季碳