Clear Sky Science · sv
Deacylativ korskoppling av ketoner via oxidativ SH2 homolytisk substitution
Att förvandla vanliga kemikalier till flexibla byggstenar
Kemister förlitar sig på ett litet antal enkla ingredienser för att bygga de komplexa molekyler som finns i läkemedel och material. Denna studie visar hur man får en av de vanligaste ingredienserna, ketoner, att bilda nya förbindelser som tidigare var svåra att uppnå, vilket öppnar nya vägar för att utforma läkemedelslika molekyler snabbare och mer precist.
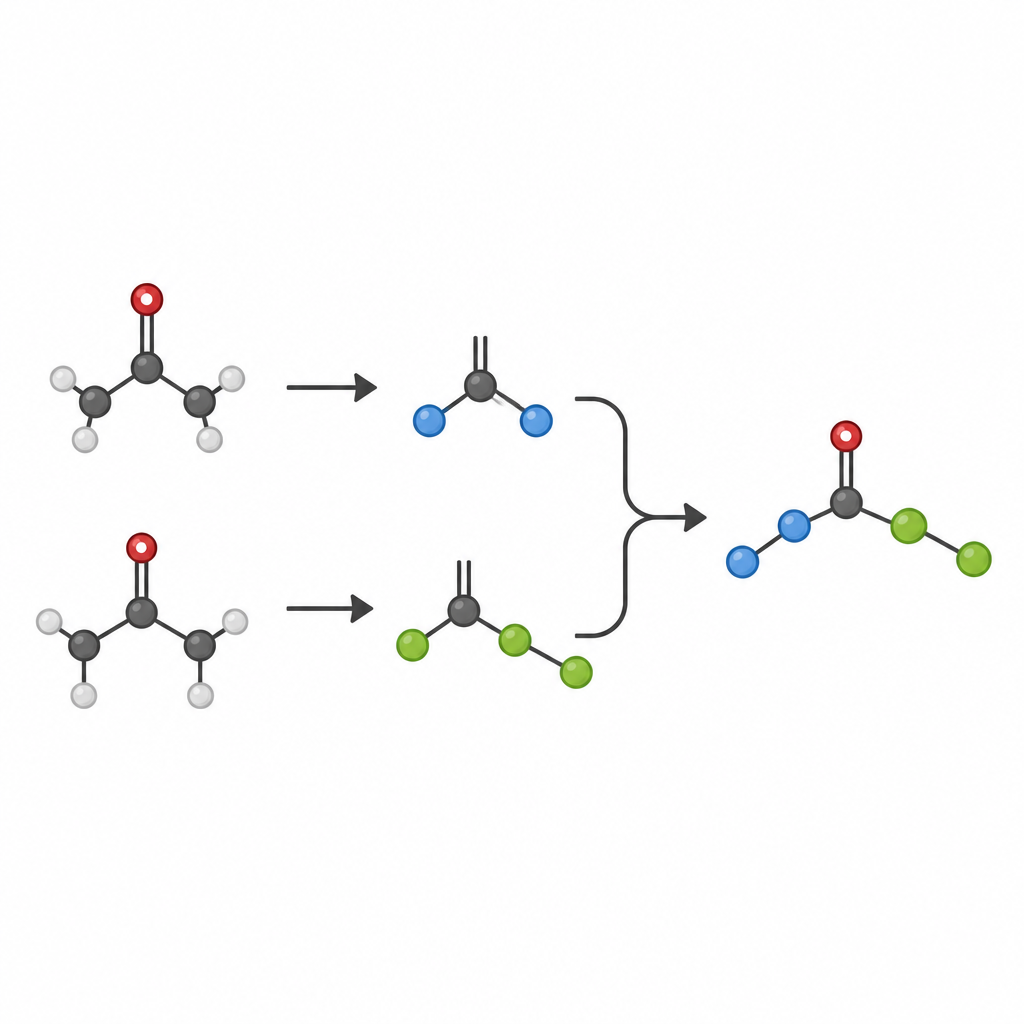
Varför vardagsketoner är viktiga
Ketoner är arbetsdjur i organisk kemi, uppskattade eftersom de är lätta att tillverka, lagra och modifiera. Klassiska reaktioner som aldolkondensation och McMurry-koppling omvandlar redan ketoner till mer komplexa produkter, men dessa metoder kräver ofta stora mängder metallreagenser och har svårt att förena två olika partners på ett kontrollerat sätt. Särskilt att bilda stabila länkar mellan två mättade kolatomer, de så kallade C–C enkelbindningarna i trånga miljöer, har förblivit en stor utmaning, även om sådana trånga kolcentra är centrala i många moderna läkemedel.
Ett nytt sätt att få två radikaler att samarbeta
Författarna försökte få två olika ketoner att reagera med varandra på ett rent och selektivt sätt. Istället för att aktivera den vanliga karbonyldelen av ketonen fokuserar de på att bryta en närliggande kol–kol-bindning för att frigöra små, kortlivade fragment som kallas radikaler. Dessa radikaler kan i princip återförenas på många sätt, inklusive oönskad självparning eller sidoreaktioner. För att tygla detta kaos använder teamet en strategi som kallas SH2, en form av homolytisk substitution där en metallkomplex tillfälligt håller en radikal och sedan attackeras av en andra radikal utifrån. Denna yttersfäriska väg hjälper till att styra vilka två bitar som faktiskt förenas.
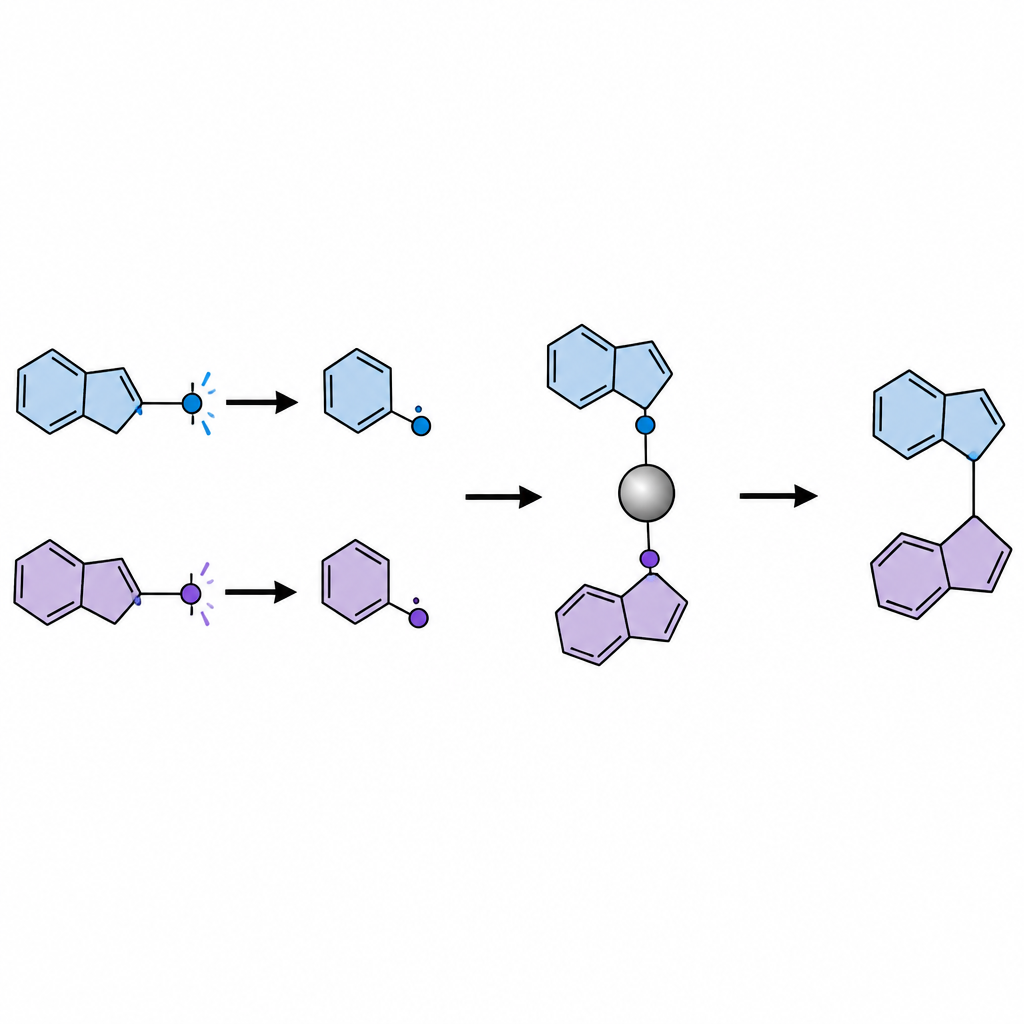
Maskering av ketoner för att kontrollera deras beteende
Att direkt bestråla ketoner med ljus genererar ofta både användbara och skadliga radikala fragment. För att undvika detta problem omvandlar forskarna varje keton till en bänksstabil "maskerad" form kallad dihydroquinazolinon i ett enkelt steg innan huvudreaktionen. Under blått ljus oxiderar en organisk fotokatalysator dessa maskerade ketoner, vilket får dem att splittras och frigöra två distinkta radikaler: ett mindre, mindre steriskt hindrat primärt fragment och ett bulkigare sekundärt eller tertiärt fragment. En nickelkatylsator fångar selektivt det mindre radikala fragmentet för att bilda ett bestående nickel–kol-komplex, medan det bulkigare radikala förblir fritt i lösningen. Eftersom nickel–primärkomplexet bildar en starkare bindning än vad nickel–tertiärkomplexet skulle göra, sorterar systemet naturligt radikalerna till sina olika roller.
Bygga trånga centra för läkemedelslika molekyler
När nickel–primärkomplexet väl är bildat attackeras det av det bulkigare radikala i ett SH2-steg, vilket skapar en ny kol–kol-bindning och regenererar nickelkatatalysatorn. Med denna metod konstruerar teamet ett brett spektrum produkter som innehåller ett trångt, fyrväldigt kolcentrum intill en kväve-, syre- eller svavelatom. Dessa inkluderar β-kvaternära aminer, β-aminoalkoholer, β-diaminer, β-aminotioler och relaterade etrar, alla motiv som är vanliga i bioaktiva föreningar. Reaktionen tolererar många funktionella grupper, såsom alkener, estrar, halider och ringsystem, och sker under milda förhållanden med synligt ljus. Författarna visar också att metoden kan användas sent i syntesen av kända läkemedel, där den försiktigt modifierar strukturer utan att störa andra känsliga delar.
En titt under reaktionens huva
För att förstå hur processen fungerar fångar forskarna de flyktiga radikalerna, studerar hur den ljusabsorberande katalysatorn släcks och beräknar relativa hastigheter och energier för nyckelsteg. Deras bevis pekar på en mekanism där båda radikalerna uppstår från oxidation av de maskerade ketonerna snarare än från peroxidsyrans oxidant, och där nickel förblir i ett högre oxidationsstadium och undviker den typiska innersfäriska korskopplingsvägen som skulle reagera med arylhalider. Beräkningar visar att bildandet av nickel–primärkomplexet är energimässigt föredraget, och att båda radikalerna produceras i liknande hastigheter — förhållanden som undertrycker oönskad självkoppling och gynnar önskad korsparning.
Vad detta betyder för framtida molekylbygge
Enkelt uttryckt lär denna studie ketoner en ny färdighet: hur de kan splittras på ett kontrollerat sätt så att rätt fragment återförenas till nya, mer komplexa strukturer. Genom att kombinera synligt ljus, en nickelkatatalysator och smart maskerade ketoner skapar författarna en generell och flexibel väg till trånga kolcentra som är högt värderade inom läkemedelsupptäckt. Denna strategi lägger till ett kraftfullt verktyg i kemistens verktygslåda för att redigera och diversifiera molekyler, särskilt i sena steg där små förändringar kan ge stora effekter på biologisk aktivitet.
Citering: Yang, JX., Zhang, MY., Wen, Q. et al. Cross-ketone deacylative coupling via oxidative SH2 homolytic substitution. Nat Commun 17, 4248 (2026). https://doi.org/10.1038/s41467-026-70619-5
Nyckelord: koppling av ketoner, radikal kemi, nickelkatalys, fotoredox, kvaternärt kol