Clear Sky Science · pl
Międzyketonowe sprzęganie deacylacyjne przez utleniającą substytucję homolityczną SH2
Przekształcanie powszechnych związków w elastyczne cegiełki
Chemicy opierają się na niewielkim zestawie prostych składników przy budowie złożonych cząsteczek spotykanych w lekach i materiałach. To badanie pokazuje, jak skłonić jeden z najpowszechniejszych składników, ketony, do tworzenia nowych połączeń, które wcześniej były bardzo trudne do osiągnięcia, otwierając nowe drogi do projektowania cząsteczek przypominających leki szybciej i precyzyjniej.
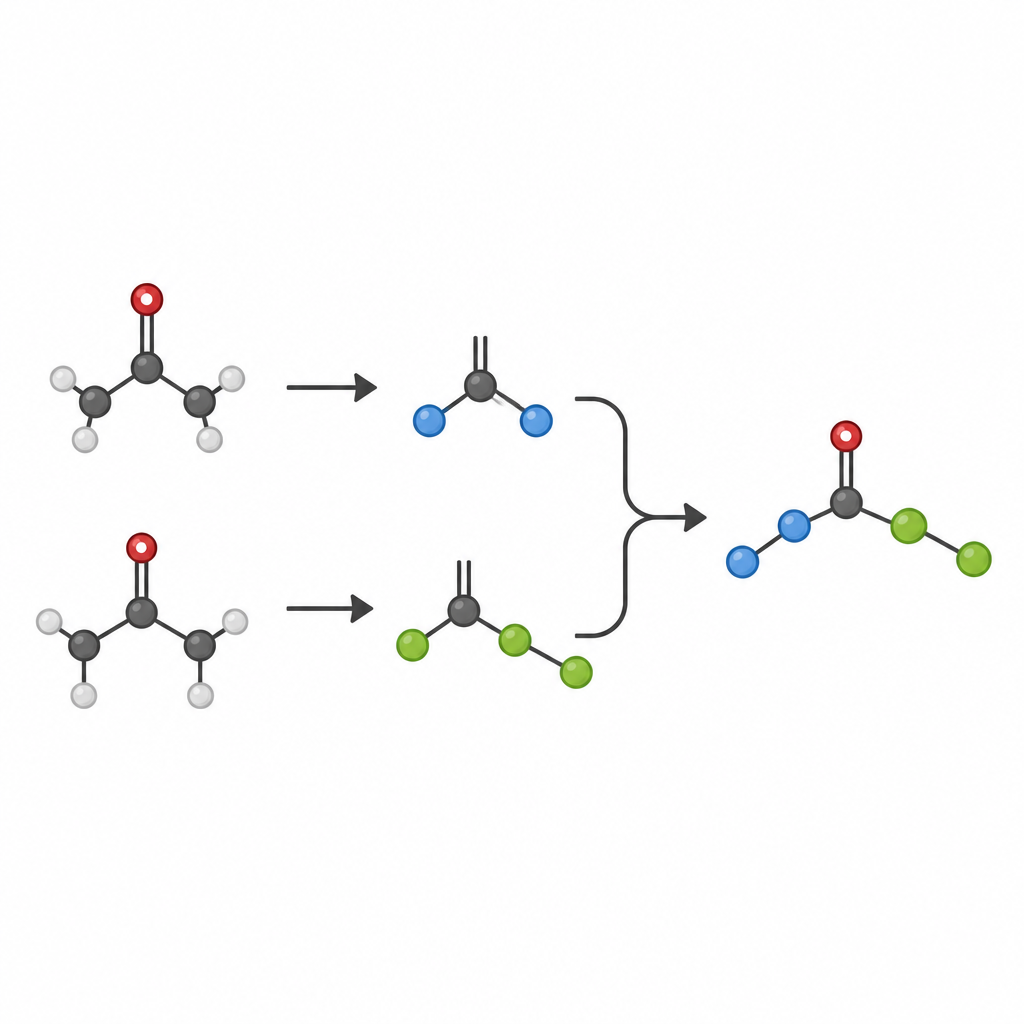
Dlaczego zwykłe ketony mają znaczenie
Ketony są podstawowymi związkami w chemii organicznej, cenionymi za to, że łatwo je syntezować, przechowywać i modyfikować. Klasyczne reakcje, takie jak reakcja aldolowa czy sprzęganie McMurry’ego, już przekształcają ketony w bardziej złożone produkty, lecz metody te często wymagają dużych ilości reagentów metalicznych i mają trudności ze łączeniem dwóch różnych partnerów w kontrolowany sposób. W szczególności tworzenie trwałych wiązań między dwoma nasyconymi atomami węgla — tzw. pojedynczych wiązań C–C w zatłoczonych środowiskach — pozostawało dużym wyzwaniem, mimo że takie zatłoczone centra węglowe są kluczowymi elementami wielu współczesnych leków.
Nowy sposób, by dwa rodniki współdziałały
Autorzy postanowili sprawić, by dwa różne ketony „porozmawiały” ze sobą w czysty i selektywny sposób. Zamiast aktywować zwykłą część karbonylową ketonu, skupili się na pękaniu sąsiedniego wiązania węglowo-węglowego, uwalniając małe, krótkotrwałe fragmenty zwane rodnikami. Te rodniki mogą się w zasadzie łączyć na wiele sposobów, w tym w niepożądane parowania czy reakcje uboczne. Aby okiełznać ten chaos, zespół zastosował strategię nazwaną SH2 — formę substytucji homolitycznej, w której kompleks metaliczny chwilowo wychwytuje jeden rodnik, a następnie jest atakowany przez drugi rodnik z zewnątrz. Ta zewnętrzna ścieżka pomaga ukierunkować, które dwa kawałki faktycznie się łączą.
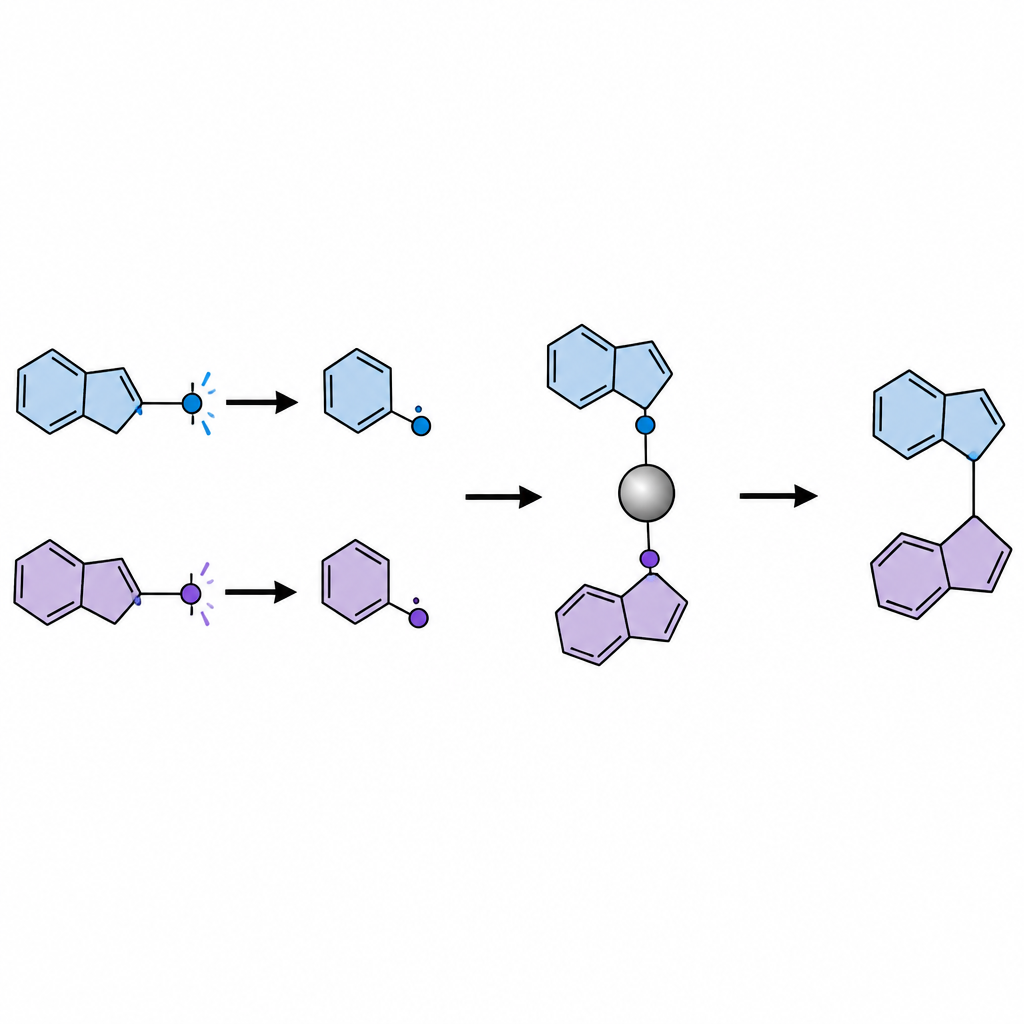
Maskowanie ketonów, by kontrolować ich zachowanie
Bezpośrednie naświetlanie ketonów często generuje zarówno przydatne, jak i szkodliwe fragmenty rodnikowe. Aby obejść ten problem, badacze przekształcają każdy keton w stabilną w warunkach laboratoryjnych „zamaskowaną” formę zwaną dihydrokinazolinonem w jednym prostym kroku przed główną reakcją. Pod wpływem niebieskiego światła organiczny fotokatalizator utlenia te zamaskowane ketony, powodując ich rozpad i uwolnienie dwóch odmiennych rodników: mniejszego, mniej sterycznie utrudnionego fragmentu pierwotnego oraz większego fragmentu wtórnego lub trzeciorzędowego. Katalizator niklowy selektywnie wychwytuje mniejszy rodnik, tworząc trwały kompleks nikiel–węgiel, podczas gdy większy rodnik pozostaje wolny w roztworze. Ponieważ kompleks niklowy związany z rodnikiem pierwotnym tworzy silniejsze wiązanie niż analogiczny kompleks z rodnikiem trzeciorzędowym, system naturalnie sortuje rodniki do różnych ról.
Budowanie zatłoczonych centrów dla struktur przypominających leki
Gdy kompleks nikiel–pierwotny zostanie zmontowany, większy rodnik atakuje go w kroku SH2, formując nowe wiązanie węglowo-węglowe i regenerując katalizator niklowy. Dzięki temu podejściu zespół zbudował szeroką gamę produktów zawierających zatłoczone, czterodrogowe centrum węglowe w pobliżu azotu, tlenu lub siarki. Należą do nich β-czwartorzędowe aminy, β-aminoalkohole, β-diaminy, β-aminotiole i powiązane estry — motywy powszechne w związkach bioaktywnych. Reakcja toleruje wiele grup funkcyjnych, takich jak alkeny, estry, halogenki i układy pierścieniowe, i zachodzi w łagodnych warunkach przy świetle widzialnym. Autorzy pokazują również, że metodę można zastosować późno w syntezie znanych leków, delikatnie modyfikując ich struktury bez naruszania innych wrażliwych fragmentów.
Rzut oka pod maskę reakcji
Aby zrozumieć, jak działa proces, badacze wychwytują efemeryczne rodniki, badają sposób, w jaki gaszony jest fotokatalizator absorbujący światło, i obliczają względne szybkości oraz energie kluczowych etapów. Ich dowody wskazują na mechanizm, w którym oba rodniki powstają w wyniku utlenienia zamaskowanych ketonów, a nie z utleniacza nadtlenkowego, oraz że nikiel pozostaje w wyższym stanie utlenienia, unikając typowej ścieżki wewnętrznej (inner-sphere) sprzęgania, która reagowałaby z halogenkami arylowymi. Obliczenia pokazują, że tworzenie kompleksu nikiel–pierwotny jest termodynamicznie uprzywilejowane, a oba rodniki powstają w podobnych szybkościach — warunki te tłumią niepożądane samospajanie i sprzyjają pożądanemu sprzęganiu krzyżowemu.
Co to oznacza dla przyszłego tworzenia cząsteczek
Mówiąc prosto, ta praca uczy ketony nowego triku: jak kontrolowanie się rozpadać, by właściwe fragmenty ponownie połączyły się w nowe, bardziej złożone struktury. Łącząc światło widzialne, katalizator niklowy i sprytnie zamaskowane ketony, autorzy stworzyli ogólną i elastyczną drogę do zatłoczonych centrów węglowych, które są wysoko cenione w odkrywaniu leków. Ta strategia wzbogaca zestaw narzędzi chemika o potężne rozwiązanie do edycji i dywersyfikacji cząsteczek, szczególnie w późnych etapach syntezy, gdzie drobne zmiany mogą mieć duże skutki dla aktywności biologicznej.
Cytowanie: Yang, JX., Zhang, MY., Wen, Q. et al. Cross-ketone deacylative coupling via oxidative SH2 homolytic substitution. Nat Commun 17, 4248 (2026). https://doi.org/10.1038/s41467-026-70619-5
Słowa kluczowe: sprzęganie ketonów, chemia rodnikowa, kataliza niklowa, fotoredoks, węgiel czwartorzędowy