Clear Sky Science · it
Accoppiamento deacilativo tra chetoni tramite sostituzione omolitica SH2 ossidativa
Trasformare sostanze comuni in blocchi costruttivi flessibili
I chimici si affidano a un piccolo insieme di ingredienti semplici per costruire le molecole complesse presenti nei medicinali e nei materiali. Questo studio mostra come indurre uno degli ingredienti più comuni, i chetoni, a formare nuove connessioni precedentemente difficili da ottenere, aprendo nuove strade per progettare molecole simili a farmaci in modo più rapido e preciso.
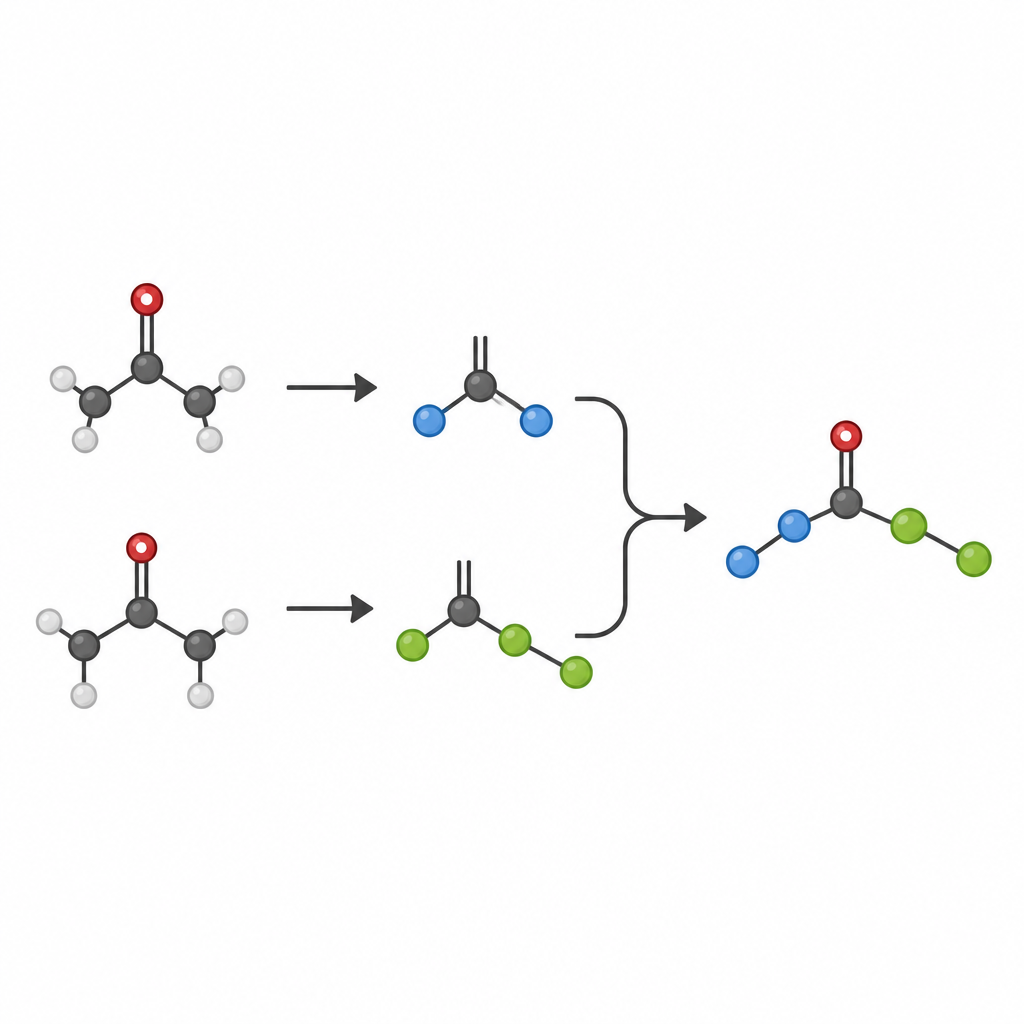
Perché i chetoni di tutti i giorni sono importanti
I chetoni sono molecole fondamentali in chimica organica, apprezzate perché sono facili da preparare, conservare e modificare. Reazioni classiche come l’aldolica e l’accoppiamento di McMurry già trasformano i chetoni in prodotti più complessi, ma questi metodi spesso richiedono grandi quantità di reagenti metallici e faticano a unire due partner diversi in modo controllato. In particolare, formare legami robusti tra due atomi di carbonio saturi, i cosiddetti legami singoli C–C in ambienti ingombrati, è rimasto una sfida importante, nonostante tali centri carboniosi affollati siano caratteristiche centrali in molti farmaci moderni.
Un nuovo modo per far collaborare due radicali
Gli autori si sono proposti di far «comunicare» due chetoni diversi in modo pulito e selettivo. Invece di attivare la porzione carbonilica usuale del chetone, si concentrano sulla rottura di un legame carbonio–carbonio adiacente per liberare piccoli frammenti a vita breve noti come radicali. Questi radicali possono, in linea di principio, ricombinarsi in molti modi, inclusi auto-accoppiamenti indesiderati o reazioni collaterali. Per domare questo caos, il gruppo usa una strategia chiamata SH2, una forma di sostituzione omolitica in cui un complesso metallico trattiene temporaneamente un radicale e poi viene attaccato da un secondo radicale dall’esterno. Questa via a sfera esterna aiuta a guidare quali due pezzi effettivamente si uniscono.
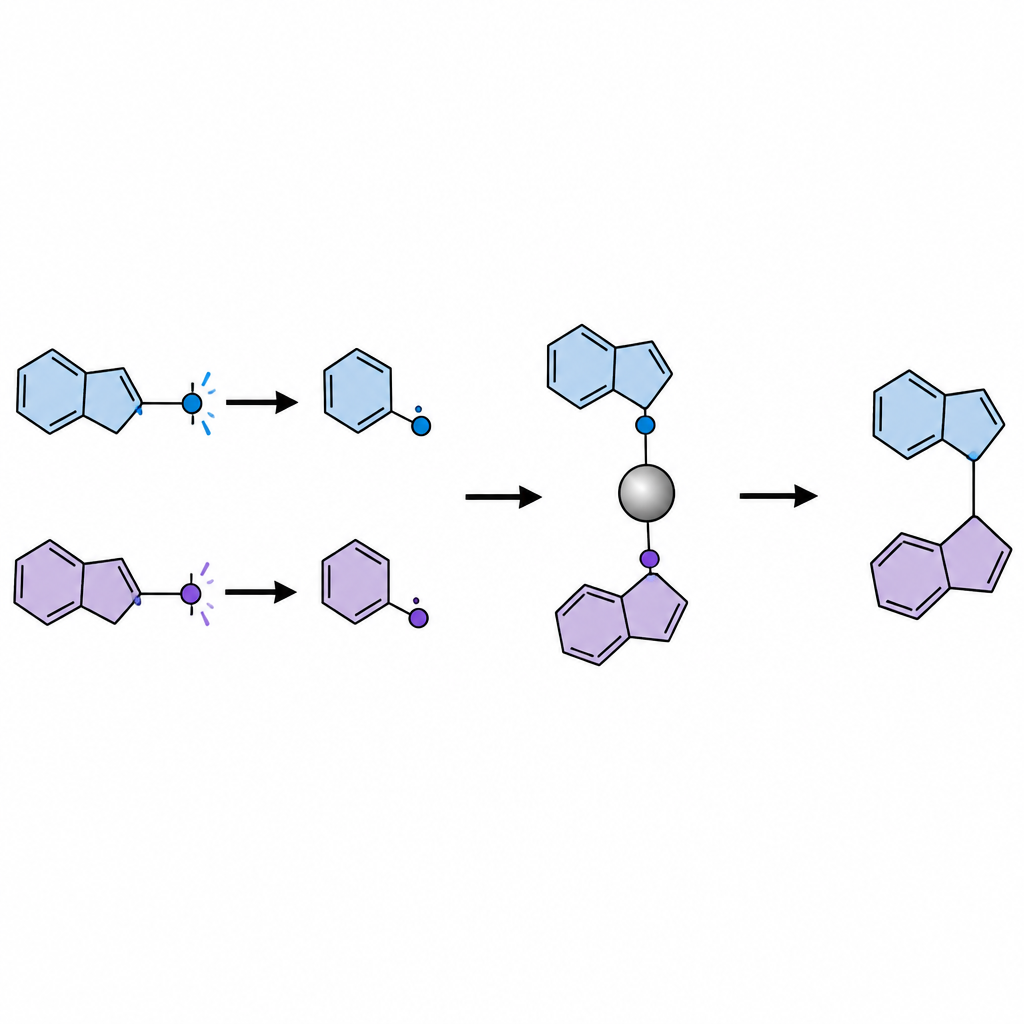
Mascherare i chetoni per controllarne il comportamento
Illuminare direttamente i chetoni spesso genera frammenti radicalari sia utili sia dannosi. Per aggirare questo problema, i ricercatori convertono ogni chetone in una forma «mascherata» stabile su banco chiamata diidrochinazolinone in un unico semplice passaggio prima della reazione principale. Sotto luce blu, un fotocatalizzatore organico ossida questi chetoni mascherati, facendoli scindere e rilasciare due radicali distinti: un frammento primario più piccolo e meno ingombrato e un frammento secondario o terziario più voluminoso. Un catalizzatore al nichel cattura selettivamente il radicale più piccolo formando un complesso nichel–carbonio persistente, mentre il radicale più ingombrante rimane libero in soluzione. Poiché il complesso nichel–primario forma un legame più forte rispetto a quello che si avrebbe con un radicale terziario, il sistema ordina naturalmente i radicali nei loro ruoli differenti.
Costruire centri ingombrati per molecole simili a farmaci
Una volta assemblato, il complesso nichel–primario viene attaccato dal radicale più voluminoso in un passaggio SH2, formando un nuovo legame carbonio–carbonio e rigenerando il catalizzatore al nichel. Con questo approccio, il team costruisce una vasta gamma di prodotti che contengono un centro carbonioso quaternario affollato accanto a un atomo di azoto, ossigeno o zolfo. Questi includono ammine β‑quaternarie, β‑amminoalcoli, β‑diamini, β‑aminotioli e eteri correlati, tutti motivi comuni nei composti bioattivi. La reazione tollera molti gruppi funzionali, come alcheni, esteri, alogeni e sistemi ad anello, e procede in condizioni miti con luce visibile. Gli autori mostrano inoltre che il metodo può essere applicato in fase tardiva alla sintesi di molecole farmaceutiche note, modificandone delicatamente le strutture senza disturbare altre parti sensibili.
Dare uno sguardo sotto il cofano della reazione
Per capire come funziona il processo, i ricercatori intrappolano i radicali fugaci, studiano come il catalizzatore che assorbe la luce viene quenchato e calcolano le velocità relative e le energie dei passaggi chiave. Le evidenze indicano un meccanismo in cui entrambi i radicali derivano dall’ossidazione dei chetoni mascherati piuttosto che dall’ossidante perossido, e in cui il nichel rimane in uno stato di ossidazione più elevato, evitando la tipica via di accoppiamento a sfera interna che reagirebbe con alogenuri arilici. I calcoli mostrano che la formazione del complesso nichel–primario è favorita dal punto di vista energetico, e che entrambi i radicali vengono prodotti a velocità simili, condizioni che sopprimono l’auto‑accoppiamento indesiderato e favoriscono l’accoppiamento incrociato desiderato.
Cosa significa per la sintesi di molecole future
In termini semplici, questo lavoro insegna ai chetoni un nuovo trucco: come scindersi in modo controllato affinché i frammenti giusti ricombinino in strutture nuove e più complesse. Combinando luce visibile, un catalizzatore al nichel e chetoni astutamente mascherati, gli autori creano una via generale e flessibile per ottenere centri carboniosi affollati, molto apprezzati nella scoperta di farmaci. Questa strategia aggiunge uno strumento potente nella cassetta degli attrezzi del chimico per modificare e diversificare le molecole, in particolare nelle fasi tardive dove piccoli cambiamenti possono avere grandi effetti sull’attività biologica.
Citazione: Yang, JX., Zhang, MY., Wen, Q. et al. Cross-ketone deacylative coupling via oxidative SH2 homolytic substitution. Nat Commun 17, 4248 (2026). https://doi.org/10.1038/s41467-026-70619-5
Parole chiave: accoppiamento di chetoni, chimica radicalare, catalisi al nichel, fotoredox, carbonio quaternario