Clear Sky Science · nl
Cross-ketone deacylatieve koppeling via oxidatieve SH2 homolytsubstitutie
Veelgebruikte chemicaliën als flexibele bouwstenen
Synthetische chemici vertrouwen op een klein aantal eenvoudige ingrediënten om de complexe moleculen in medicijnen en materialen op te bouwen. Deze studie laat zien hoe een van de meest voorkomende ingrediënten, ketonen, zó te beïnvloeden dat ze nieuwe verbindingen aangaan die voorheen moeilijk te maken waren, waarmee nieuwe routes ontstaan om medicijnachtige moleculen sneller en preciezer te ontwerpen.
Waarom alledaagse ketonen ertoe doen
Ketonen zijn werkpaarden in de organische chemie: ze zijn eenvoudig te bereiden, op te slaan en te modificeren. Klassieke reacties zoals de aldolreactie en McMurry-koppeling zetten ketonen al om in complexere producten, maar deze methoden vergen vaak grote hoeveelheden metalen reagentia en hebben moeite om twee verschillende partners gecontroleerd aan elkaar te koppelen. Met name het vormen van robuuste verbindingen tussen twee verzadigde koolstofatomen — de zogeheten C–C enkelbindingen in sterisch drukke omgevingen — blijft een grote uitdaging, ook al zijn zulke drukbezette koolstofcentra centrale elementen in veel moderne geneesmiddelen.
Een nieuwe manier om twee radicalen samen te laten werken
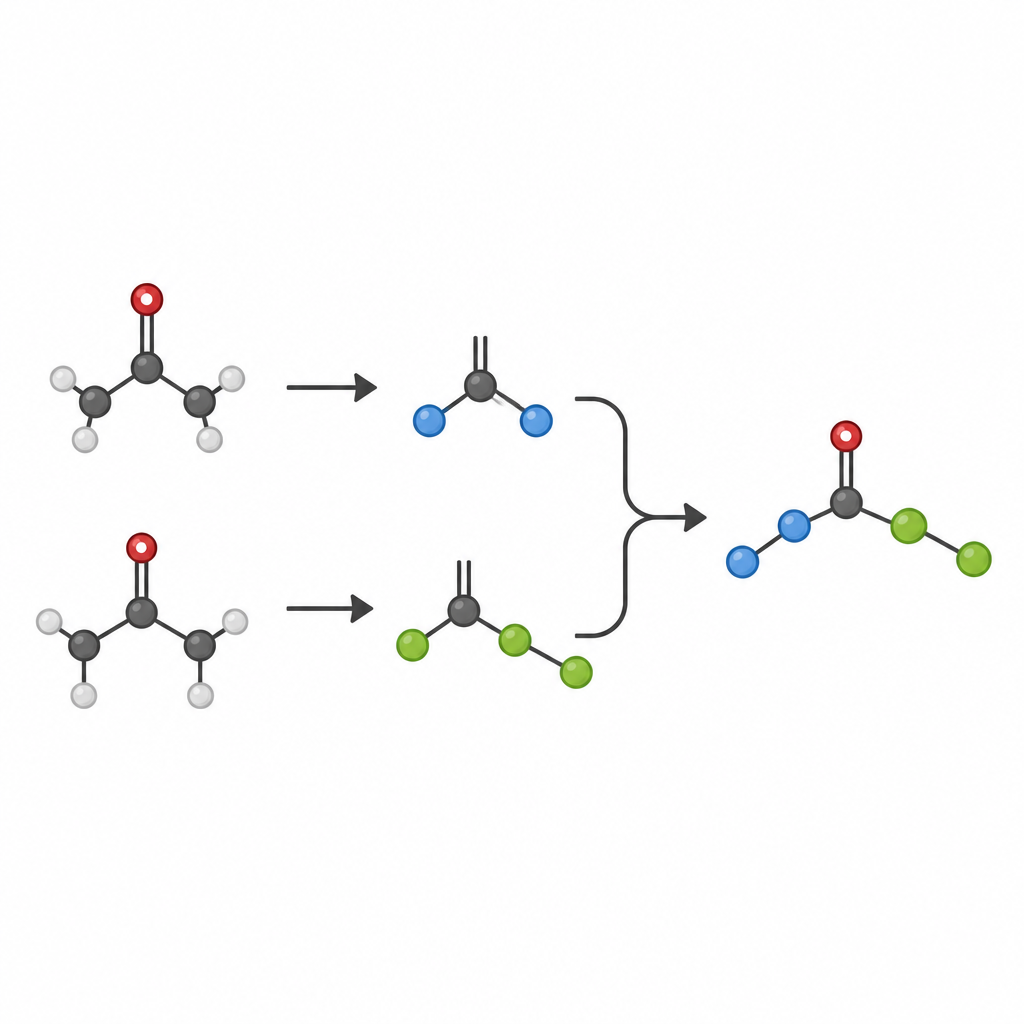
De auteurs wilden twee verschillende ketonen op een schone en selectieve manier met elkaar laten reageren. In plaats van het gebruikelijke geactiveerde carbonylgedeelte van de ketoon te activeren, richten ze zich op het breken van een nabije koolstof–koolstofbinding om kleine, kortlevende fragmenten vrij te maken die bekendstaan als radicalen. Deze radicalen kunnen in principe op veel manieren recombineren, inclusief ongewenste zelfkoppeling of bijreacties. Om deze chaos te temmen, gebruikt het team een strategie genaamd SH2, een vorm van homolytische substitutie waarbij een metaalcomplex kort één radicaal vasthoudt en vervolgens van buitenaf wordt aangevallen door een tweede radicaal. Dit buiten-sfeer pad helpt te sturen welke twee stukjes daadwerkelijk samenkomen.
Ketonen maskeren om hun gedrag te beheersen
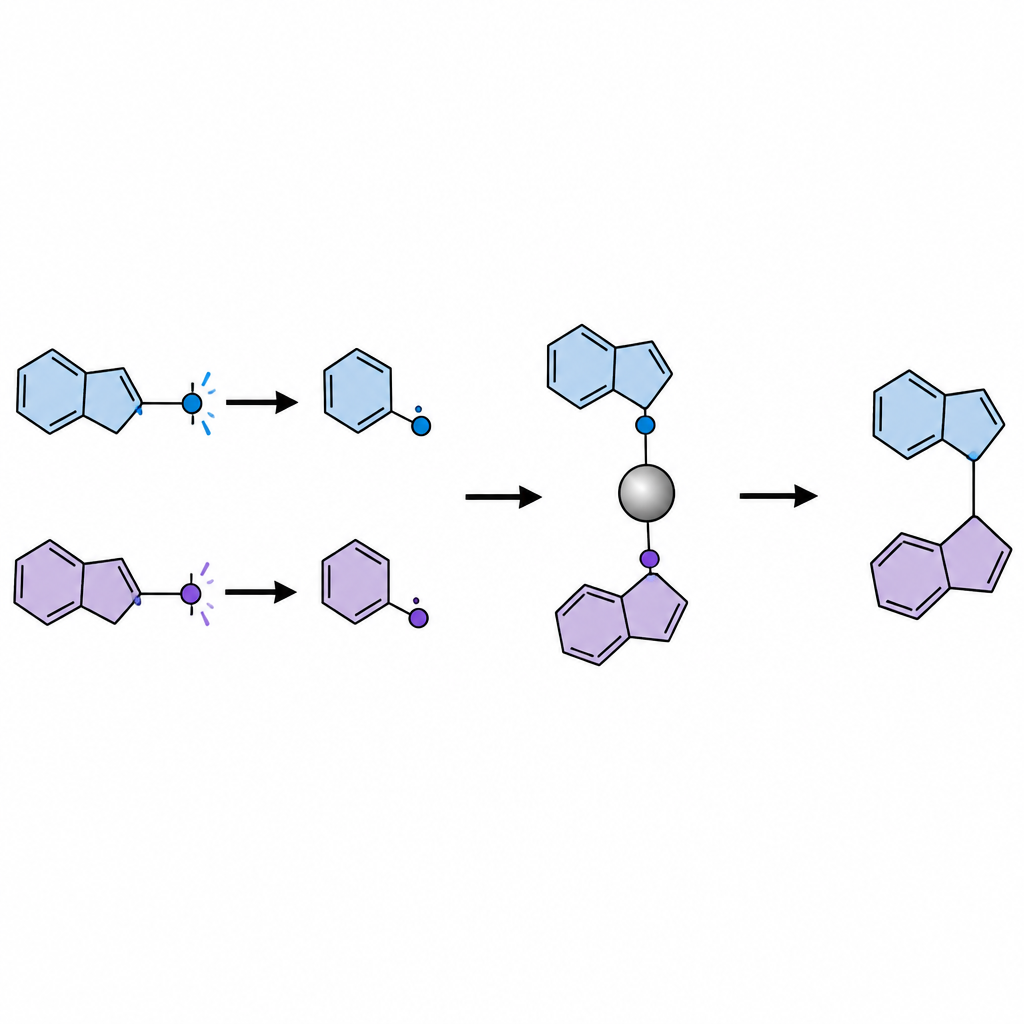
Direct bestralen van ketonen met licht genereert vaak zowel nuttige als schadelijke radicaalfragmenten. Om dit probleem te omzeilen, zetten de onderzoekers elke ketoon in één eenvoudige stap om in een bankstabiele "gemaskerde" vorm, een dihydroquinazolinon, voordat de hoofdreactie plaatsvindt. Onder blauw licht oxideert een organische fotokatalysator deze gemaskerde ketonen, waardoor ze uiteenvallen en twee verschillende radicalen vrijgeven: een kleiner, minder gehinderd primair fragment en een omvangrijker secundair of tertiair fragment. Een nikkelkatalysator pakt selectief het kleinere radicaal op om een persistent nikkel–koolstofcomplex te vormen, terwijl het omvangrijkere radicaal vrij in oplossing blijft. Omdat de nikkel–primaire binding sterker gevormd wordt dan een hypothetische nikkel–tertiaire binding, sorteert het systeem van nature de radicalen in hun verschillende rollen.
Drukke centra bouwen voor medicijnachtige moleculen
Eenmaal samengesteld wordt het nikkel–primaire complex aangevallen door het omvangrijkere radicaal in een SH2-stap, waarbij een nieuwe koolstof–koolstofbinding ontstaat en de nikkelkatalysator wordt geregenereerd. Met deze benadering bouwt het team een breed scala aan producten met een drukbezet, quaternair koolstofcentrum naast een stikstof-, zuurstof- of zwavelatoom. Hiertoe behoren β-quaternaire aminen, β-aminoalcoholen, β-diaminen, β-aminothiolen en verwante etherverbindingen — motieven die veel voorkomen in bioactieve stoffen. De reactie verdraagt vele functionele groepen, zoals alkenen, esters, haliden en ringstructuren, en verloopt onder milde condities met zichtbaar licht. De auteurs tonen ook aan dat de methode laat in de synthese van bekende geneesmiddelen kan worden toegepast, waardoor structuren voorzichtig kunnen worden aangepast zonder andere gevoelige delen te verstoren.
Onder de motorkap van de reactie kijken
Om te begrijpen hoe het proces werkt, vangen de onderzoekers de vluchtige radicalen, bestuderen ze hoe de lichtabsorberende katalysator wordt uitgegoten (gequencht) en berekenen ze relatieve snelheden en energieën van sleutelstappen. Hun bewijs wijst op een mechanisme waarbij beide radicalen ontstaan door oxidatie van de gemaskerde ketonen in plaats van door het peroxide-oxideermiddel, en waarbij nikkel in een hogere oxidatietoestand blijft, waardoor het typische inner-sphere cross-couplingpad — dat met arylhaliden zou reageren — wordt vermeden. Berekeningen tonen dat de vorming van het nikkel–primaire complex energetisch gunstiger is, en dat beide radicalen tegen vergelijkbare snelheden worden geproduceerd, omstandigheden die ongewenste zelfkoppeling onderdrukken en de gewenste kruisparing bevorderen.
Wat dit betekent voor toekomstig molecuulontwerp
In eenvoudige bewoordingen leert dit werk ketonen een nieuwe truc: hoe ze gecontroleerd kunnen uiteenvallen zodat de juiste fragmenten opnieuw samensmelten tot nieuwe, complexere structuren. Door zichtbaar licht, een nikkelkatalysator en slim gemaskerde ketonen te combineren, creëren de auteurs een algemene en flexibele route naar drukbezette koolstofcentra die zeer gewaardeerd worden in medicijnontdekking. Deze strategie voegt een krachtig instrument toe aan de gereedschapskist van de chemicus voor het bewerken en diversifiëren van moleculen, vooral in late stadia waar kleine wijzigingen grote effecten op biologische activiteit kunnen hebben.
Bronvermelding: Yang, JX., Zhang, MY., Wen, Q. et al. Cross-ketone deacylative coupling via oxidative SH2 homolytic substitution. Nat Commun 17, 4248 (2026). https://doi.org/10.1038/s41467-026-70619-5
Trefwoorden: ketoonkoppeling, radicaalchemie, nikkelkatalyse, fotoredox, quaternair koolstof