Clear Sky Science · pt
Acoplamento desacilativo entre cetonas via substituição homolítica SH2 oxidativa
Transformando substâncias comuns em blocos de construção flexíveis
Químicos dependem de um conjunto pequeno de ingredientes simples para montar as moléculas complexas presentes em medicamentos e materiais. Este estudo mostra como induzir um dos ingredientes mais comuns, as cetonas, a formar novas conexões que antes eram muito difíceis de alcançar, abrindo novas rotas para projetar moléculas com características farmacêuticas de forma mais rápida e precisa.
Por que cetonas do dia a dia importam
As cetonas são moléculas essenciais na química orgânica, valorizadas por serem fáceis de sintetizar, armazenar e modificar. Reações clássicas como a aldólica e o acoplamento de McMurry já transformam cetonas em produtos mais complexos, mas esses métodos frequentemente exigem grandes quantidades de reagentes metálicos e têm dificuldade em unir dois parceiros diferentes de maneira controlada. Em particular, formar ligações robustas entre dois átomos de carbono saturados — as chamadas ligações C–C simples em ambientes congestionados — continua sendo um grande desafio, embora tais centros de carbono congestionados sejam características centrais em muitos medicamentos modernos.
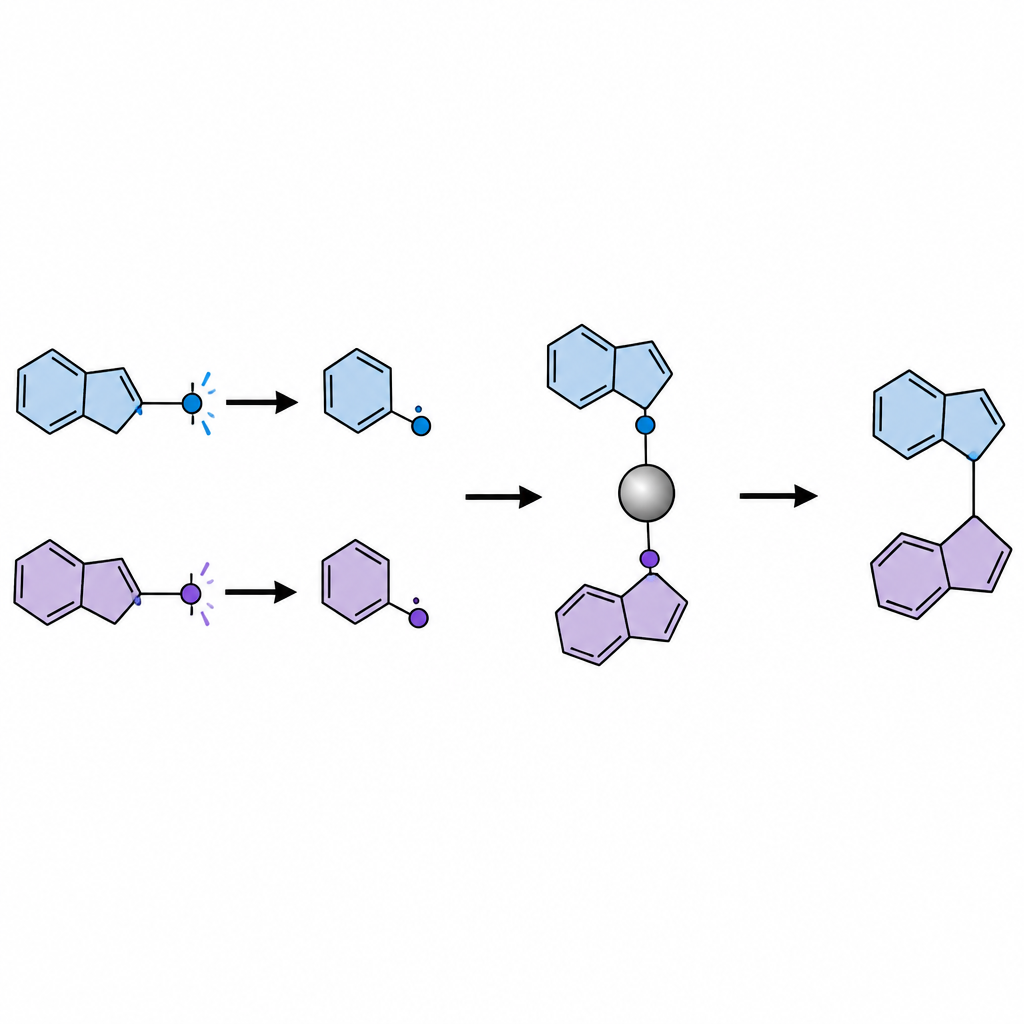
Uma nova maneira de fazer dois radicais cooperarem
Os autores buscaram fazer com que duas cetonas diferentes interagissem de forma limpa e seletiva. Em vez de ativar a porção carbonila habitual da cetona, eles focam em quebrar uma ligação carbono–carbono próxima para liberar pequenos fragmentos de curta vida conhecidos como radicais. Em princípio, esses radicais podem recombinar de muitas maneiras, incluindo pareamento próprio indesejado ou reações laterais. Para domar esse caos, a equipe usa uma estratégia chamada SH2, uma forma de substituição homolítica em que um complexo metálico retém temporariamente um radical e então é atacado por um segundo radical vindo do exterior. Essa via de esfera externa ajuda a orientar quais dois pedaços realmente se unem.
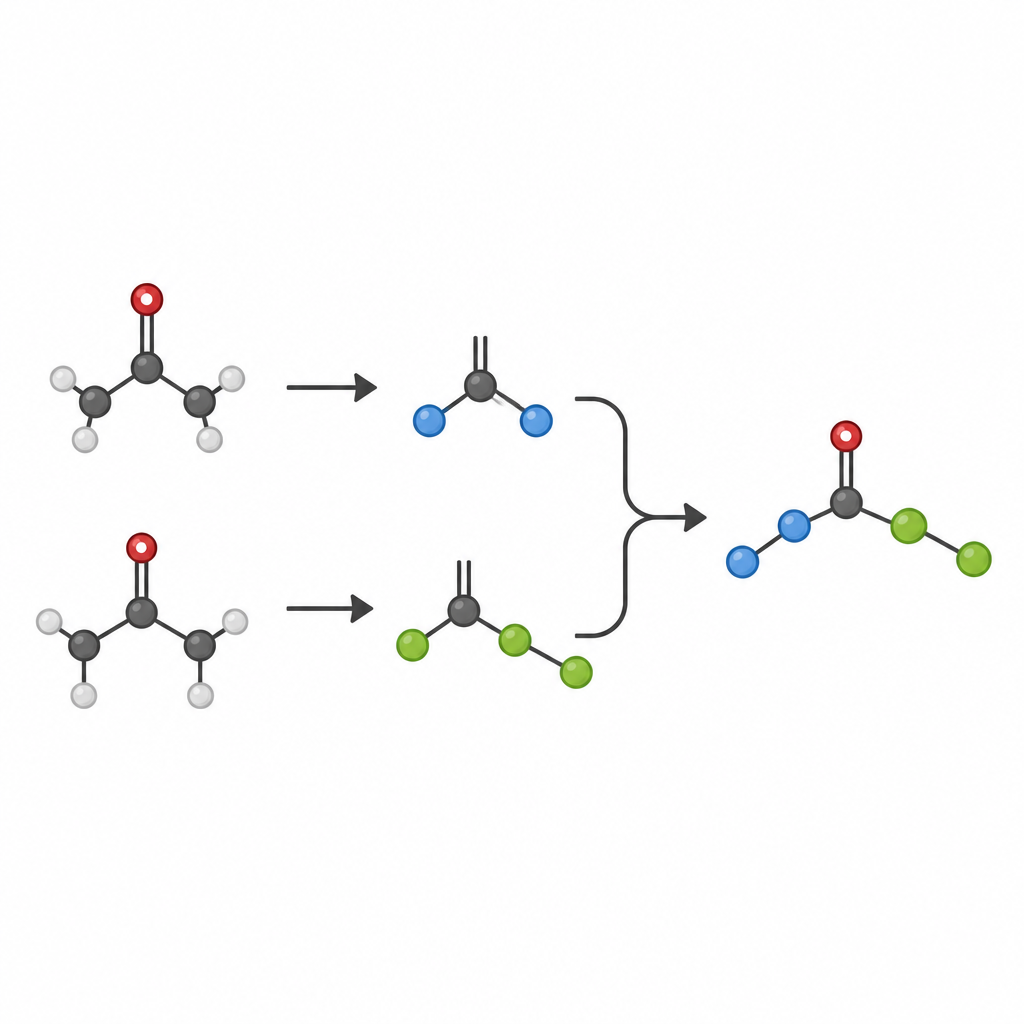
Mascarando cetonas para controlar seu comportamento
Incidir luz diretamente sobre cetonas frequentemente gera fragmentos radicalares úteis e também prejudiciais. Para contornar esse problema, os pesquisadores convertem cada cetona em uma forma “mascarada” estável em bancada chamada diidroquinazolinona em uma etapa simples antes da reação principal. Sob luz azul, um fotocatalisador orgânico oxida essas cetonas mascaradas, fazendo com que elas se rompam e liberem dois radicais distintos: um fragmento primário menor e menos impedido e um fragmento secundário ou terciário mais volumoso. Um catalisador de níquel captura seletivamente o radical menor para formar um complexo níquel–carbono persistente, enquanto o radical mais volumoso permanece livre em solução. Como o complexo níquel–primário forma uma ligação mais forte do que o que seria formado com um radical terciário, o sistema naturalmente separa os radicais em seus papéis distintos.
Construindo centros congestionados para moléculas tipo fármaco
Depois de montado, o complexo níquel–primário é atacado pelo radical mais volumoso em um passo SH2, forjando uma nova ligação carbono–carbono e regenerando o catalisador de níquel. Usando essa abordagem, a equipe constrói uma ampla gama de produtos que contêm um centro de carbono quaternário congestionado adjacente a um átomo de nitrogênio, oxigênio ou enxofre. Isso inclui aminas β-quaternárias, álcoois β-amino, β-diaminas, β-aminotióis e éteres relacionados — todos motivos comuns em compostos bioativos. A reação tolera muitos grupos funcionais, como alcenos, ésteres, haletos e sistemas cíclicos, e opera sob condições brandas com luz visível. Os autores também mostram que o método pode ser aplicado tardiamente na síntese de fármacos conhecidos, modificando suas estruturas de forma delicada sem perturbar outras partes sensíveis.
Espreitando sob o capô da reação
Para entender como o processo funciona, os pesquisadores aprisionam os radicais efêmeros, estudam como o catalisador fotoabsorvente é desativado e calculam as velocidades e energias relativas dos passos-chave. As evidências apontam para um mecanismo em que ambos os radicais surgem da oxidação das cetonas mascaradas, em vez de provirem do oxidante peróxido, e em que o níquel permanece em um estado de oxidação mais alto, evitando a via típica de acoplamento de esfera interna que reagiria com haletos arílicos. Cálculos mostram que a formação do complexo níquel–primário é energeticamente preferível, e que ambos os radicais são produzidos em taxas similares, condições que suprimem o autopareamento indesejado e favorecem o pareamento cruzado desejado.
O que isso significa para a síntese de moléculas no futuro
Em termos simples, este trabalho ensina às cetonas uma nova habilidade: como se fragmentar de forma controlada para que os pedaços certos se recombinem em estruturas novas e mais complexas. Ao combinar luz visível, um catalisador de níquel e cetonas inteligentemente mascaradas, os autores criam uma rota geral e flexível para centros de carbono congestionados, altamente valorizados na descoberta de fármacos. Essa estratégia adiciona uma ferramenta poderosa ao conjunto do químico para editar e diversificar moléculas, particularmente em etapas tardias em que pequenas alterações podem ter grandes efeitos na atividade biológica.
Citação: Yang, JX., Zhang, MY., Wen, Q. et al. Cross-ketone deacylative coupling via oxidative SH2 homolytic substitution. Nat Commun 17, 4248 (2026). https://doi.org/10.1038/s41467-026-70619-5
Palavras-chave: acoplamento de cetonas, química radicalar, catálise com níquel, fotoredox, carbono quaternário