Clear Sky Science · ru
Декарбонильное перекрестное сшивание кетонов через окислительную SH2-гомолитическую замену
Преобразование обычных веществ в гибкие строительные блоки
Химики опираются на небольшой набор простых компонентов для создания сложных молекул, встречающихся в лекарствах и материалах. В этом исследовании показано, как подтолкнуть один из самых распространённых компонентов — кетоны — к образованию новых связей, которые ранее было трудно получить, что открывает новые пути для более быстрого и точного проектирования лекарственно подобных молекул.
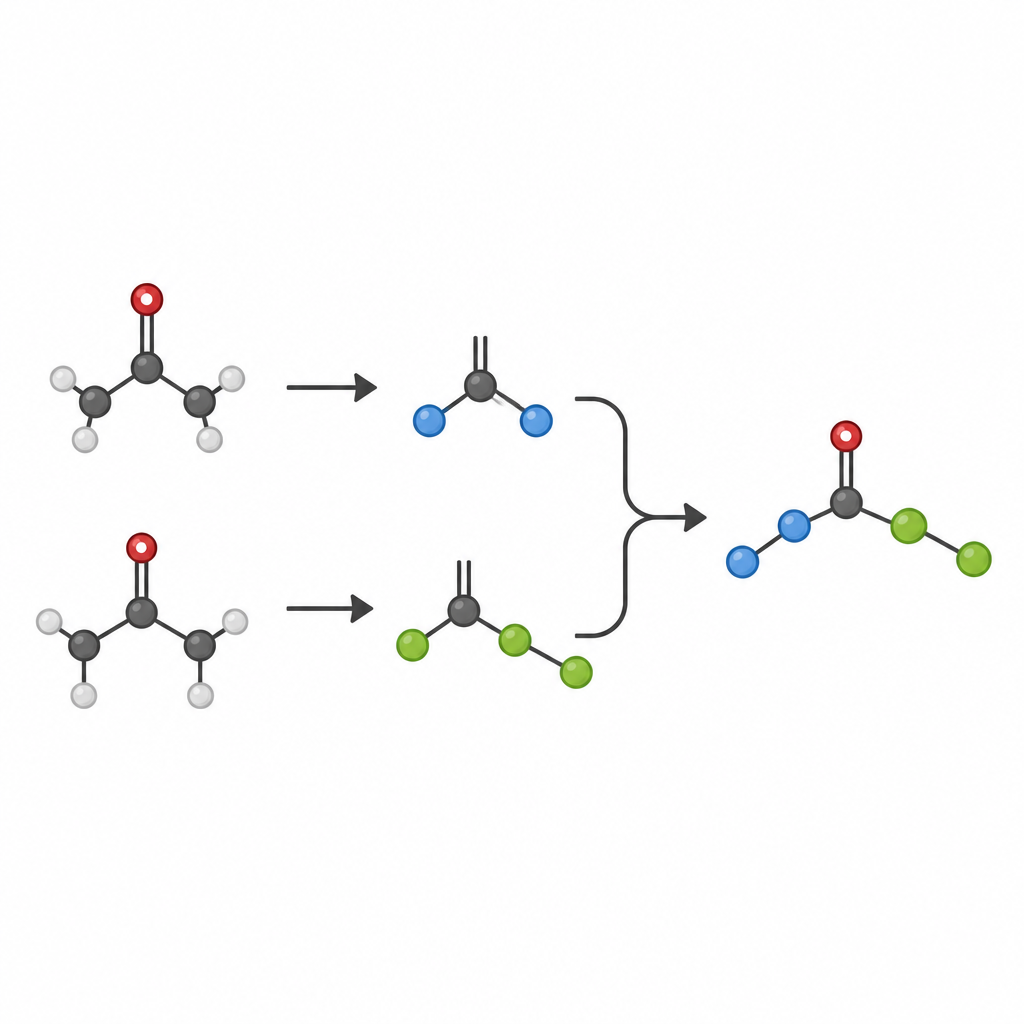
Почему обычные кетоны важны
Кетоны — это рабочие лошадки органической химии: их легко синтезировать, хранить и модифицировать. Классические реакции, такие как альдольная реакция и сшивание МакМёрри, уже превращают кетоны в более сложные продукты, но эти методы часто требуют больших количеств металлических реагентов и с трудом соединяют два разных партнёра в контролируемом виде. Особенно проблематично формирование прочных связей между двумя насыщенными атомами углерода — так называемых C–C одинарных связей в стерически перегруженных окружениях — хотя такие загруженные углеродные центры являются ключевыми элементами во многих современных лекарствах.
Новый способ заставить два радикала работать вместе
Авторы поставили цель заставить два разных кетона «пообщаться» друг с другом чисто и селективно. Вместо активации привычной карбонильной части кетона они сфокусировались на разрыве соседней углерод–углеродной связи, чтобы освободить небольшие кратковременные фрагменты — радикалы. Такие радикалы, в принципе, могут рекомбинировать множеством способов, включая нежелательное самосочетание или побочные реакции. Чтобы укротить этот хаос, команда применяет стратегию SH2 — форму гомолитической замены, при которой металлический комплекс временно удерживает один радикал, а затем на него атакует второй радикал с внешней стороны. Этот внешне-сферный путь помогает направлять, какие именно два фрагмента соединяются.
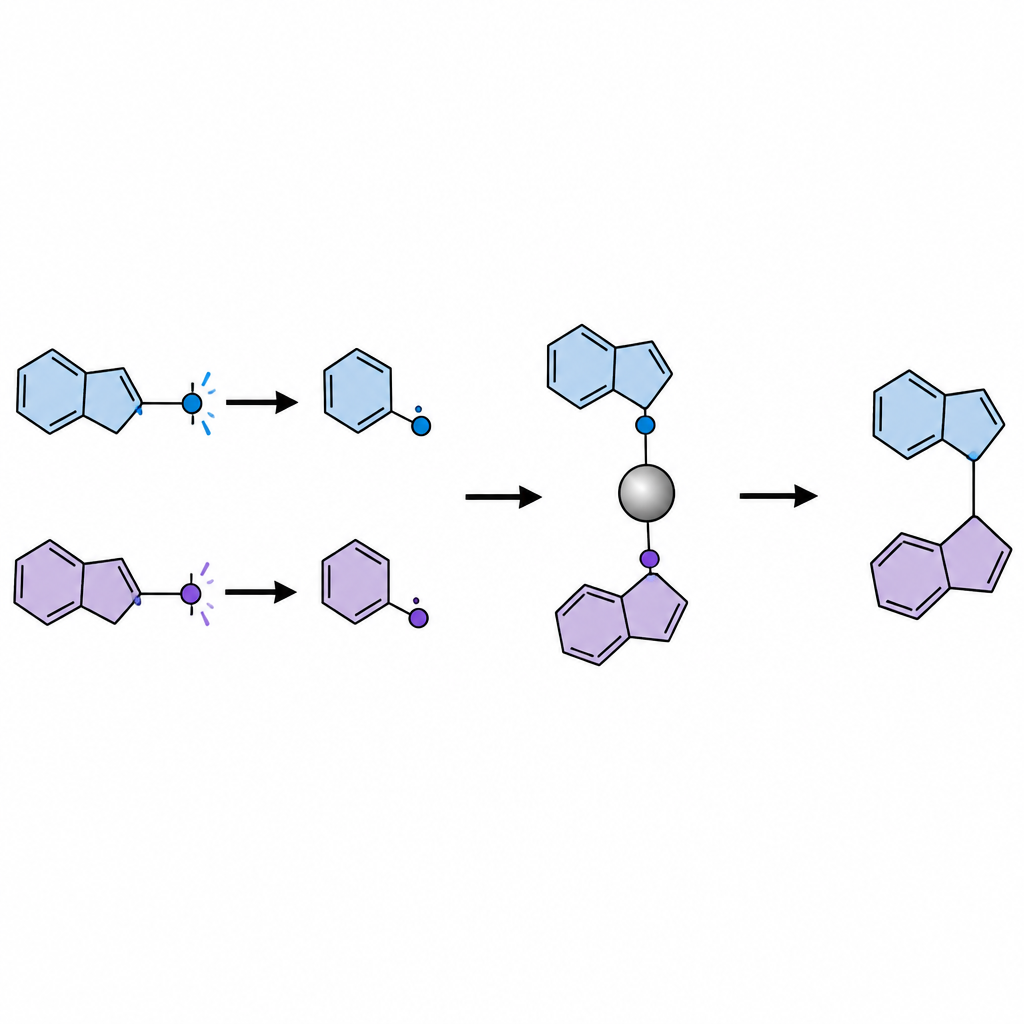
Маскировка кетонов для контроля их поведения
Прямое облучение кетонов часто порождает как полезные, так и вредные радикальные фрагменты. Чтобы обойти эту проблему, исследователи переводят каждый кетон в устойчивую при хранении «маскированную» форму — дигидрохиназолинон — в один простой шаг перед основной реакцией. Под голубым светом органический фотокатализатор окисляет эти маскированные кетоны, заставляя их разрываться и высвобождать два различных радикала: меньший, менее стерически затруднённый первичный фрагмент и более объёмный вторичный или третичный фрагмент. Никелевый катализатор селективно захватывает меньший радикал, образуя персистентный никель–углеродный комплекс, в то время как более объёмный радикал остаётся свободным в растворе. Поскольку связь никель–первичный прочнее, чем никель–третичный, система естественно сортирует радикалы по их ролям.
Построение стерически загруженных центров для лекарственно подобных молекул
После сборки никель–первичный комплекс атакуется более объёмным радикалом в шаге SH2, формируя новую углерод–углеродную связь и восстанавливая никелевый катализатор. С помощью этого подхода команда получает широкий спектр продуктов с загруженным четырёхзамещённым углеродным центром рядом с атомом азота, кислорода или серы. Среди них β-квартерные амины, β-аминоспирты, β-диамины, β-аминотиолы и родственные эфиры — мотивы, часто встречающиеся в биологически активных соединениях. Реакция терпима к множеству функциональных групп, таким как алкены, эфиры, галогениды и циклические системы, и протекает в мягких условиях под видимым светом. Авторы также показывают, что метод применим на поздних стадиях синтеза известных лекарств, мягко модифицируя их структуру без нарушения других чувствительных участков.
Заглядывая под капот реакции
Чтобы понять механизм процесса, исследователи ловят мимолётные радикалы, изучают, как тушится фотокатализатор, и вычисляют относительные скорости и энергии ключевых шагов. Их данные указывают на механизм, в котором оба радикала возникают в результате окисления маскированных кетонов, а не от пероксидного окислителя, и где никель остаётся в более высокой степени окисления, избегая типичного внутренне-сферного пути перекрестного сшивания, который реагировал бы с арилгалоидами. Расчёты показывают, что образование никель–первичного комплекса энергетически предпочтительнее, и что оба радикала образуются с похожими скоростями, что подавляет нежелательное самосшивание и способствует желанному перекрёстному объединению.
Что это значит для будущего создания молекул
Проще говоря, эта работа обучает кетоны новому приёму: как контролируемо раскладываться, чтобы нужные фрагменты рекомбинировали в новые, более сложные структуры. Сочетая видимый свет, никелевый катализатор и продуманно маскированные кетоны, авторы создают общий и гибкий путь к стерически загруженным углеродным центрам, высоко ценимым в поиске лекарств. Эта стратегия добавляет мощный инструмент в набор химика для редактирования и диверсификации молекул, особенно на поздних стадиях, где небольшие изменения могут сильно повлиять на биологическую активность.
Цитирование: Yang, JX., Zhang, MY., Wen, Q. et al. Cross-ketone deacylative coupling via oxidative SH2 homolytic substitution. Nat Commun 17, 4248 (2026). https://doi.org/10.1038/s41467-026-70619-5
Ключевые слова: сшивание кетонов, радикальная химия, никелевый катализ, фоторедокс, квартерный углерод