Clear Sky Science · es
Acoplamiento desacilativo entre cetonas mediante sustitución homolítica SH2 oxidativa
Convertir compuestos comunes en bloques de construcción flexibles
Los químicos dependen de un conjunto reducido de ingredientes sencillos para construir las moléculas complejas presentes en medicinas y materiales. Este estudio muestra cómo inducir a uno de los ingredientes más comunes, las cetonas, a formar conexiones nuevas que antes eran muy difíciles de lograr, abriendo rutas frescas para diseñar moléculas tipo fármaco de forma más rápida y precisa.
Por qué importan las cetonas cotidianas
Las cetonas son moléculas versátiles en química orgánica, valoradas porque son fáciles de sintetizar, almacenar y modificar. Reacciones clásicas como la aldólica y el acoplamiento de McMurry ya convierten cetonas en productos más complejos, pero estos métodos a menudo requieren grandes cantidades de reactivos metálicos y tienen dificultades para unir dos socios diferentes de manera controlada. En particular, formar enlaces resistentes entre dos átomos de carbono saturados, los llamados enlaces simples C–C en entornos congestionados, sigue siendo un reto importante, aunque tales centros de carbono congestionado son rasgos centrales en muchos fármacos modernos.
Una nueva manera de hacer que dos radicales cooperen
Los autores se propusieron lograr que dos cetonas distintas se ‘comuniquen’ entre sí de forma limpia y selectiva. En lugar de activar la porción carbonilo habitual de la cetona, se centran en romper un enlace carbono–carbono próximo para liberar fragmentos pequeños y de corta vida conocidos como radicales. En principio, estos radicales pueden recombinarse de muchas maneras, incluyendo apareamientos no deseados o reacciones secundarias. Para domesticar este caos, el equipo utiliza una estrategia llamada SH2, una forma de sustitución homolítica en la que un complejo metálico retiene momentáneamente un radical y luego es atacado por un segundo radical desde el exterior. Esta vía de esfera externa ayuda a guiar qué dos piezas se unen realmente.
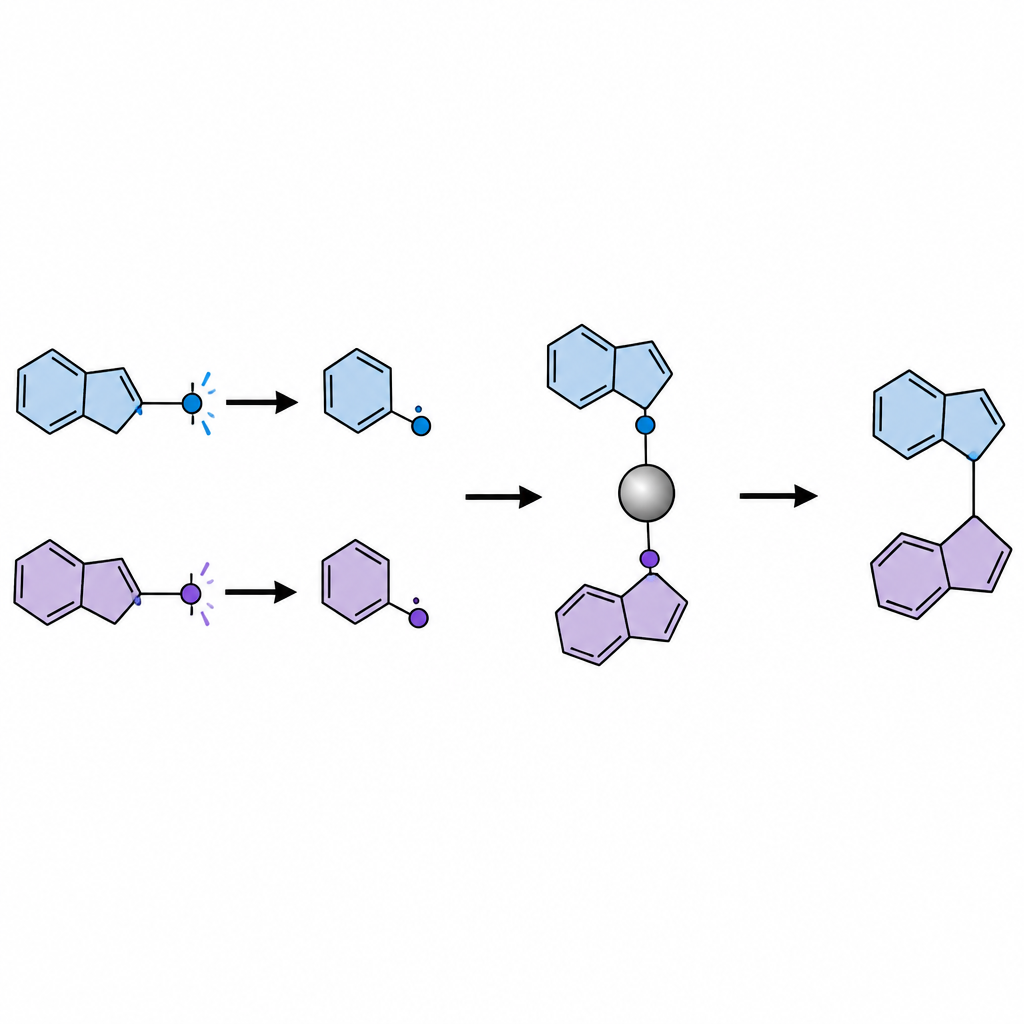
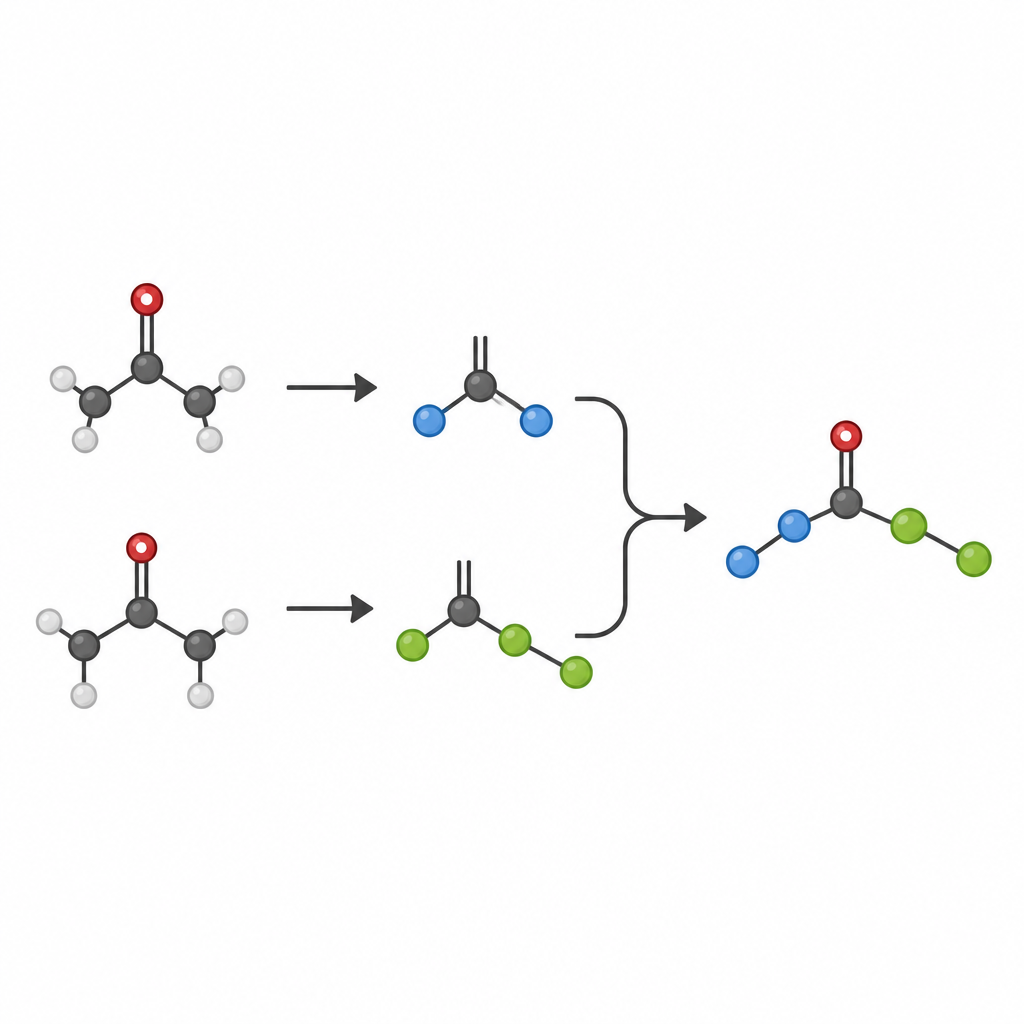
Enmascarar cetonas para controlar su comportamiento
Iluminar directamente las cetonas suele generar tanto fragmentos radicalarios útiles como perjudiciales. Para sortear este problema, los investigadores convierten cada cetona en una forma «enmascarada» estable en banco llamada dihidroquinazolinona en un paso simple antes de la reacción principal. Bajo luz azul, un fotocatalizador orgánico oxida estas cetonas enmascaradas, provocando su ruptura y la liberación de dos radicales distintos: un fragmento primario más pequeño y menos impedido y un fragmento secundario o terciario más voluminoso. Un catalizador de níquel captura selectivamente el radical más pequeño para formar un complejo persistente níquel–carbono, mientras que el radical más voluminoso permanece libre en disolución. Debido a que el complejo níquel–primario forma un enlace más fuerte que el que formaría un complejo níquel–terciario, el sistema ordena de manera natural a los radicales en sus distintos roles.
Construir centros congestionados para moléculas tipo fármaco
Una vez ensamblado, el complejo níquel–primario es atacado por el radical más voluminoso en un paso SH2, forjando un nuevo enlace carbono–carbono y regenerando el catalizador de níquel. Usando este enfoque, el equipo construye una amplia gama de productos que contienen un centro de carbono congestionado (cuaternario) junto a un átomo de nitrógeno, oxígeno o azufre. Estos incluyen aminas β-cuaternarias, alcoholes β-amino, β-diaminas, β-aminotióles y éteres relacionados, todos motivos comunes en compuestos bioactivos. La reacción tolera muchos grupos funcionales, como alquenos, ésteres, haluros y sistemas de anillo, y opera en condiciones suaves con luz visible. Los autores también muestran que el método puede aplicarse en etapas tardías de la síntesis de fármacos conocidos, modificando sus estructuras de forma delicada sin perturbar otras partes sensibles.
Mirando bajo el capó de la reacción
Para entender cómo funciona el proceso, los investigadores atrapan los radicales fugaces, estudian cómo se apaga el fotocatalizador absorbente de luz y calculan las velocidades y energías relativas de los pasos clave. Sus evidencias apuntan a un mecanismo donde ambos radicales surgen de la oxidación de las cetonas enmascaradas en lugar de proceder del oxidante peróxido, y donde el níquel permanece en un estado de oxidación más alto, evitando la vía típica de acoplamiento de esfera interna que reaccionaría con haluros arílicos. Los cálculos muestran que la formación del complejo níquel–primario es energéticamente preferida, y que ambos radicales se producen a ritmos similares, condiciones que suprimen el autoacoplamiento no deseado y favorecen el apareamiento cruzado deseado.
Qué significa esto para la futura fabricación de moléculas
En términos sencillos, este trabajo enseña a las cetonas un nuevo truco: cómo romperse de manera controlada para que los fragmentos adecuados se recombinen en estructuras nuevas y más complejas. Al combinar luz visible, un catalizador de níquel y cetonas enmascaradas ingeniosamente, los autores crean una vía general y flexible hacia centros de carbono congestionados que son muy valorados en el descubrimiento de fármacos. Esta estrategia añade una herramienta poderosa al conjunto del químico para editar y diversificar moléculas, particularmente en etapas tardías donde pequeños cambios pueden tener grandes efectos sobre la actividad biológica.
Cita: Yang, JX., Zhang, MY., Wen, Q. et al. Cross-ketone deacylative coupling via oxidative SH2 homolytic substitution. Nat Commun 17, 4248 (2026). https://doi.org/10.1038/s41467-026-70619-5
Palabras clave: acoplamiento de cetonas, química radicalaria, catálisis con níquel, fotoredox, carbono cuaternario