Clear Sky Science · fr
Couplage déacylatif inter-cétone via substitution homolytique SH2 oxydative
Transformer des produits courants en blocs de construction flexibles
Les chimistes s’appuient sur un petit ensemble d’ingrédients simples pour assembler les molécules complexes présentes dans les médicaments et les matériaux. Cette étude montre comment inciter l’un des ingrédients les plus répandus, les cétones, à former de nouvelles connexions jusque-là difficiles à obtenir, ouvrant ainsi de nouvelles voies pour concevoir des molécules de type médicament plus rapidement et avec plus de précision.
Pourquoi les cétones du quotidien comptent
Les cétones sont des molécules de travail en chimie organique, appréciées parce qu’elles sont faciles à synthétiser, à stocker et à modifier. Des réactions classiques telles que l’aldol ou le couplage de McMurry transforment déjà des cétones en produits plus complexes, mais ces méthodes nécessitent souvent de grandes quantités de réactifs métalliques et peinent à joindre deux partenaires différents de façon contrôlée. En particulier, former des liaisons solides entre deux atomes de carbone saturés — les liaisons simples C–C dans des environnements encombrés — est resté un défi majeur, bien que ces centres carbonés encombrés soient des éléments centraux dans de nombreux médicaments modernes.
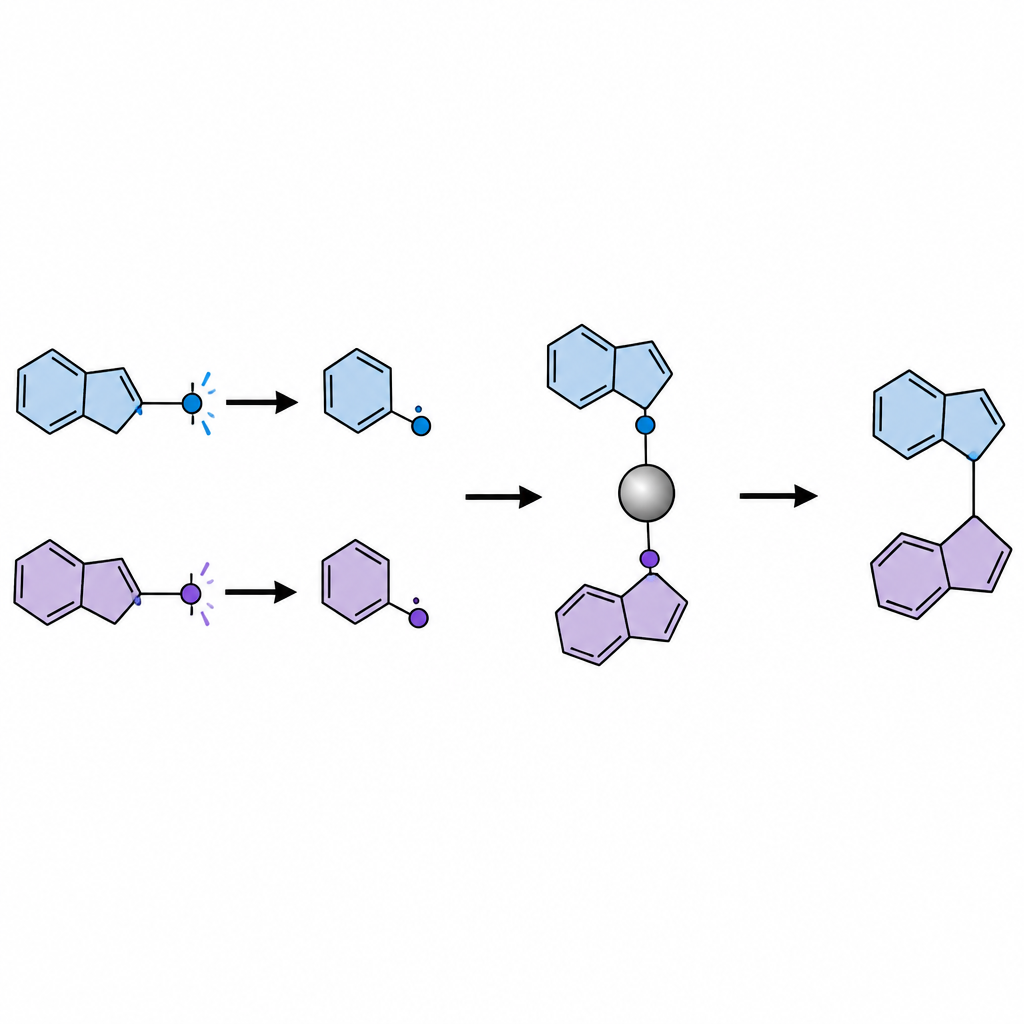
Une nouvelle manière de faire coopérer deux radicaux
Les auteurs ont cherché à faire communiquer deux cétones différentes de façon propre et sélective. Plutôt que d’activer la partie carbonyle habituelle de la cétone, ils se concentrent sur la rupture d’une liaison carbone–carbone voisine pour libérer de petits fragments éphémères appelés radicaux. Ces radicaux peuvent, en principe, se recombiner de nombreuses façons, y compris par appariement entre eux ou par réactions secondaires indésirables. Pour maîtriser ce chaos, l’équipe utilise une stratégie appelée SH2, une forme de substitution homolytique dans laquelle un complexe métallique retient brièvement un radical puis est attaqué par un second radical venant de l’extérieur. Cette voie dite en sphère externe aide à orienter quels deux morceaux se rejoignent réellement.
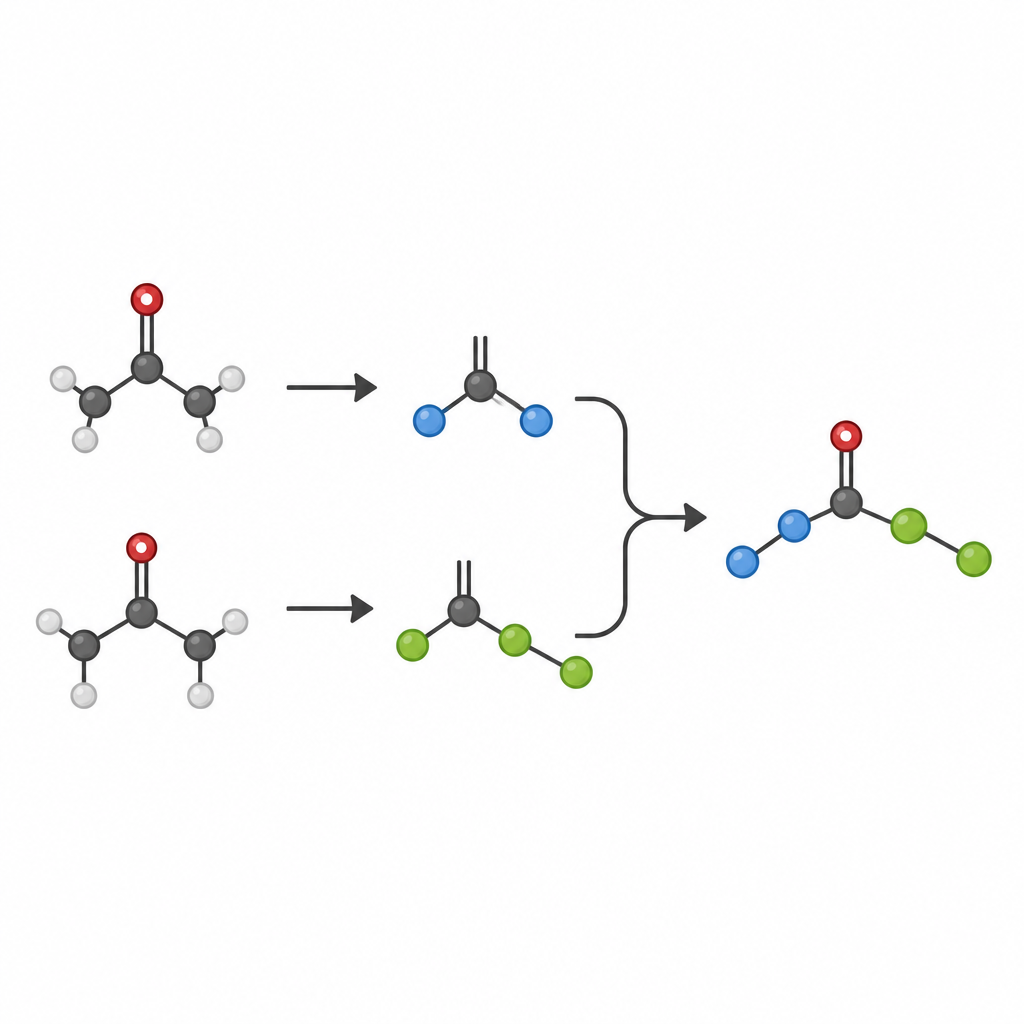
Masquer les cétones pour contrôler leur comportement
Exposer directement les cétones à la lumière génère souvent des fragments radicalaires à la fois utiles et nuisibles. Pour contourner ce problème, les chercheurs convertissent chaque cétone en une forme « masquée » stable sur paillasse, la dihydroquinazolinone, en une seule étape avant la réaction principale. Sous lumière bleue, un photocatalyseur organique oxyde ces cétones masquées, les faisant se rompre et libérer deux radicaux distincts : un fragment primaire plus petit et peu encombré, et un fragment secondaire ou tertiaire plus volumineux. Un catalyseur au nickel capture sélectivement le radical le plus petit pour former un complexe nickel–carbone persistant, tandis que le radical plus encombré reste libre en solution. Comme la formation du complexe nickel–primaire engendre une liaison plus forte que le complexe nickel–tertiaire, le système trie naturellement les radicaux selon leurs rôles.
Construire des centres encombrés pour des molécules proches des médicaments
Une fois assemblé, le complexe nickel–primaire est attaqué par le radical plus volumineux lors d’une étape SH2, forgeant une nouvelle liaison carbone–carbone et régénérant le catalyseur au nickel. Grâce à cette approche, l’équipe construit une large gamme de produits contenant un centre carboné quaternaire encombré adjacent à un atome d’azote, d’oxygène ou de soufre. Cela inclut des amines β-quaternaires, des β-aminoalcools, des β-diamines, des β-aminothiols et des éthers apparentés, motifs fréquents dans les composés bioactifs. La réaction tolère de nombreux groupes fonctionnels — alcènes, esters, halogènes et systèmes cycliques — et fonctionne dans des conditions douces avec de la lumière visible. Les auteurs montrent également que la méthode peut s’appliquer tardivement dans la synthèse de médicaments connus, modifiant délicatement leur structure sans perturber d’autres parties sensibles.
Un coup d’œil sous le capot de la réaction
Pour comprendre le fonctionnement du procédé, les chercheurs piègent les radicaux fugitifs, étudient la façon dont le photocatalyseur est désactivé et calculent les vitesses relatives et les énergies des étapes clés. Leurs preuves indiquent un mécanisme où les deux radicaux proviennent de l’oxydation des cétones masquées plutôt que de l’oxydant peroxydé, et où le nickel reste dans un état d’oxydation élevé, évitant la voie habituelle de couplage en sphère interne qui réagirait avec des halogénures arylés. Les calculs montrent que la formation du complexe nickel–primaire est énergétiquement favorisée, et que les deux radicaux sont produits à des vitesses similaires, conditions qui suppriment l’auto-appariement indésirable et favorisent l’appariement croisé souhaité.
Ce que cela signifie pour la synthèse future de molécules
En termes simples, ce travail apprend une nouvelle astuce aux cétones : se rompre de façon contrôlée pour que les bons fragments se recombinent en structures nouvelles et plus complexes. En combinant la lumière visible, un catalyseur au nickel et des cétones astucieusement masquées, les auteurs mettent au point une voie générale et flexible vers des centres carbonés encombrés très prisés en découverte de médicaments. Cette stratégie ajoute un outil puissant à la boîte à outils du chimiste pour éditer et diversifier des molécules, en particulier à des stades tardifs où de petits changements peuvent avoir de grands effets sur l’activité biologique.
Citation: Yang, JX., Zhang, MY., Wen, Q. et al. Cross-ketone deacylative coupling via oxidative SH2 homolytic substitution. Nat Commun 17, 4248 (2026). https://doi.org/10.1038/s41467-026-70619-5
Mots-clés: couplage de cétones, chimie radicalaire, catalyse au nickel, photoredox, carbone quaternaire