Clear Sky Science · zh
丁酸盐延长线粒体缺陷小鼠的健康与寿命
为何肠道对衰竭的“细胞引擎”至关重要
线粒体疾病是罕见病,细胞内的微小“动力工厂”开始衰竭,导致多个器官出现连锁问题并常常缩短寿命。目前的治疗主要局限于对症处理。这项小鼠研究发现了肠道中意想不到的助力:某些能产生丁酸盐的细菌。研究显示,恢复这一来源于肠道的分子可以修复渗漏的肠道,缓解多种类似衰老的病变,并显著延长严重线粒体缺陷动物的寿命。
当细胞的动力工厂出故障
研究人员首先构建了一种小鼠模型,使得关键线粒体调控因子 TFAM 在成年后可被全身关闭。一旦移除了这一维持线粒体 DNA 的“守护者”,动物迅速出现类似加速衰老的综合征:脂肪和肌肉流失、抓握无力、血糖控制差、肺部纤维化、心血管异常、肾功能衰竭、贫血,以及包括运动障碍和筑巢行为受损在内的脑退行性迹象。许多器官出现炎症和细胞衰老的分子标志物,小鼠过早死亡,表明广泛的线粒体功能失常本身就能驱动多器官衰败。
渗漏的肠道与紊乱的微生物群落
鉴于线粒体对肠上皮细胞健康至关重要,团队检查了这些动物的肠道。他们发现肠道结构变短、分裂的细胞减少,保护性的黏液层变薄,尽管产生黏液的杯状细胞数量正常。更多的杯状细胞“卡住”了黏液未能释放。参与封闭细胞间隙和产生抗菌防御的基因被下调,肠道通透性增加:荧光示踪物漏入血液,血液中细菌产物的标志显著升高。与此同时,肠道细菌群落发生转变。通常以膳食碳水化合物为食并产生有益短链脂肪酸的微生物减少,而其他类群扩张。化学分析证实,粪便中所有主要短链脂肪酸的水平,以及血液中若干种类,明显下降。
另一种线粒体疾病模型中的共同模式
为检验这种肠道破坏是否仅与一种基因操作相关,科学家转向第二种小鼠品系,该品系随年龄积累线粒体 DNA 的随机突变并出现早发的多病共病。这些动物同样表现出更渗漏的肠道屏障、连接和抗菌基因表达减少、以及更简单且失衡的肠道微生物群。尤其是专门产丁酸盐的细菌被耗竭,粪便丁酸盐水平选择性降低,而其他短链脂肪酸相对保留。这提示丧失产丁酸的微生物伙伴是线粒体衰退的共同特征。
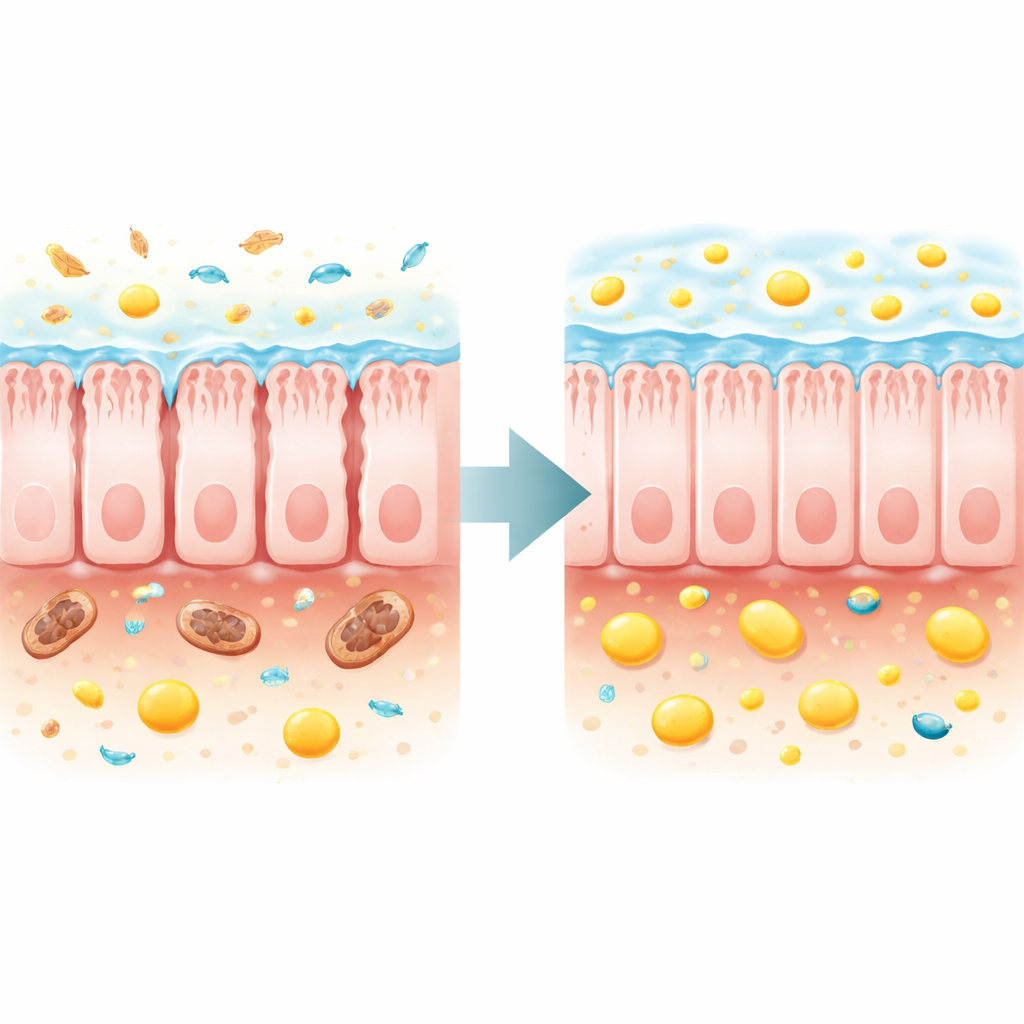
替代丧失的微生物帮助并重建屏障
作者接着探问修复肠道生态或直接恢复丁酸盐是否能改善全身健康。将健康供体的粪便微生物移植到 TFAM 缺陷小鼠,适度减缓体重下降、改善肌力和便秘,提升粪便中丁酸盐及相关脂肪酸,并使最大寿命相比接受病态微生物的鼠群延长约 70%。一种更有针对性的方法是使用膳食补充物三丁酸甘油酯(tributyrin),该物在肠内被转化为丁酸盐。此治疗提高了粪便丁酸盐、延缓消瘦、增强肌力、使空腹血糖正常化并减少肾损伤。值得注意的是,它将病鼠的中位寿命延长约四分之一,最大寿命延长超过四分之三。
肠道分子如何与基因对话
丁酸盐不仅是肠上皮细胞的能量底物,也是影响基因开关的化学信号。在病态小鼠中,研究者发现组蛋白蛋白上的特定化学标记——在组蛋白 H3 的特定位点上添加的小酰基——在肠组织中大幅减少。这些标记有助于开放围绕维持肠道屏障和应对压力基因的 DNA。用抗生素耗尽正常小鼠的微生物群也产生了类似的这些标记丧失,将其与微生物代谢物相关联。给予 TFAM 缺陷小鼠三丁酸甘油酯恢复了这些组蛋白修饰,并将肠道基因表达转回更健康的模式,包括参与细胞间连接、组织支架和抗氧化损伤反应的基因。
支持衰竭线粒体的新途径
简而言之,这项研究表明,当线粒体功能受损时,肠道变得渗漏,友好微生物发生变化,从而使机体缺乏丁酸盐。这种丧失反过来削弱肠道屏障并扰乱基因调控,加剧全身性疾病。重建宿主与微生物之间的伙伴关系——无论是移植更健康的微生物群,还是提供释放丁酸盐的补充剂——都能缓解多种症状并延长线粒体功能严重受损小鼠的寿命。尽管在将这些策略应用于人类之前还需大量工作,但这些发现突出了肠道及其微生物化学作为治疗源自细胞“动力工厂”失常疾病的新兴有希望的干预点。
引用: Gabandé-Rodríguez, E., Gómez de las Heras, M.M., Ramírez-Ruiz de Erenchun, P. et al. Butyrate extends health and lifespan in mice with mitochondrial deficiency. Nat Commun 17, 3909 (2026). https://doi.org/10.1038/s41467-026-70547-4
关键词: 线粒体疾病, 肠道微生物组, 丁酸盐, 肠道屏障, 短链脂肪酸