Clear Sky Science · es
El butirato prolonga la salud y la vida en ratones con deficiencia mitocondrial
Por qué importa el intestino para los motores celulares que fallan
Las enfermedades mitocondriales son trastornos poco frecuentes en los que las pequeñas “centrales eléctricas” dentro de nuestras células comienzan a fallar, provocando una cascada de problemas en muchos órganos y a menudo acortando la vida. Hoy por hoy, los tratamientos se limitan principalmente a manejar los síntomas. Este estudio en ratones descubre un aliado inesperado que vive en el intestino: ciertas bacterias que producen un ácido graso llamado butirato. El trabajo muestra que restaurar esta molécula derivada del intestino puede reforzar una barrera intestinal permeable, aliviar múltiples enfermedades similares al envejecimiento y extender de forma notable la esperanza de vida en animales con defectos mitocondriales severos.
Cuando las centrales celulares se deterioran
Los investigadores primero diseñaron un ratón en el que un regulador mitocondrial clave, TFAM, puede desconectarse en todo el cuerpo en la edad adulta. Una vez que se eliminó este “guardián” molecular del ADN mitocondrial, los animales desarrollaron rápidamente un síndrome que recuerda al envejecimiento acelerado: pérdida de grasa y músculo, agarre débil, mal control de la glucosa, cicatrización pulmonar, anomalías cardíacas y vasculares, insuficiencia renal, anemia y signos de degeneración cerebral, incluidos problemas de movimiento y conducta anidatoria alterada. Muchos órganos mostraron inflamación y marcadores moleculares de senescencia celular, y los ratones murieron prematuramente, lo que indica que la falla mitocondrial generalizada por sí sola puede impulsar el colapso multiorgánico.
Un intestino permeable y una comunidad microbiana alterada
Como las mitocondrias son cruciales para la salud de las células intestinales, el equipo examinó el intestino de los animales. Encontraron estructuras intestinales más cortas, menos células en división y una capa protectora de mucosidad más delgada a pesar de que el número de células caliciformes productoras de mucosidad era normal. Más de estas células estaban “atoradas” reteniendo mucosidad en lugar de liberarla. Se redujo la expresión de genes que ayudan a sellar los espacios entre las células y los que producen defensas antimicrobianas, y el intestino se volvió más permeable: un trazador fluorescente filtró hacia la sangre y un marcador sanguíneo de productos bacterianos aumentó de forma pronunciada. Al mismo tiempo, la composición de las bacterias intestinales cambió. Los microbios que normalmente prosperan con los carbohidratos dietéticos y producen ácidos grasos de cadena corta beneficiosos disminuyeron, mientras que otros grupos se expandieron. El análisis químico confirmó que los niveles de todos los principales ácidos grasos de cadena corta en las heces, y varios en la sangre, se redujeron de forma notable.
Un patrón común en otro modelo de enfermedad mitocondrial
Para comprobar si esta alteración intestinal era única de un truco genético, los científicos recurrieron a una segunda cepa de ratón que acumula mutaciones aleatorias en el ADN mitocondrial a medida que envejece y desarrolla multimorbilidad prematura. Estos animales también presentaron una barrera intestinal más permeable, menor expresión de genes de unión y antimicrobianos, y una comunidad microbiana intestinal más simple y desbalanceada. En particular, las bacterias especializadas en producir butirato estaban agotadas, y los niveles fecales de butirato eran selectivamente más bajos, mientras que otros ácidos grasos de cadena corta se mantenían relativamente. Esto apuntó a la pérdida de socios productores de butirato como una característica compartida del deterioro mitocondrial.
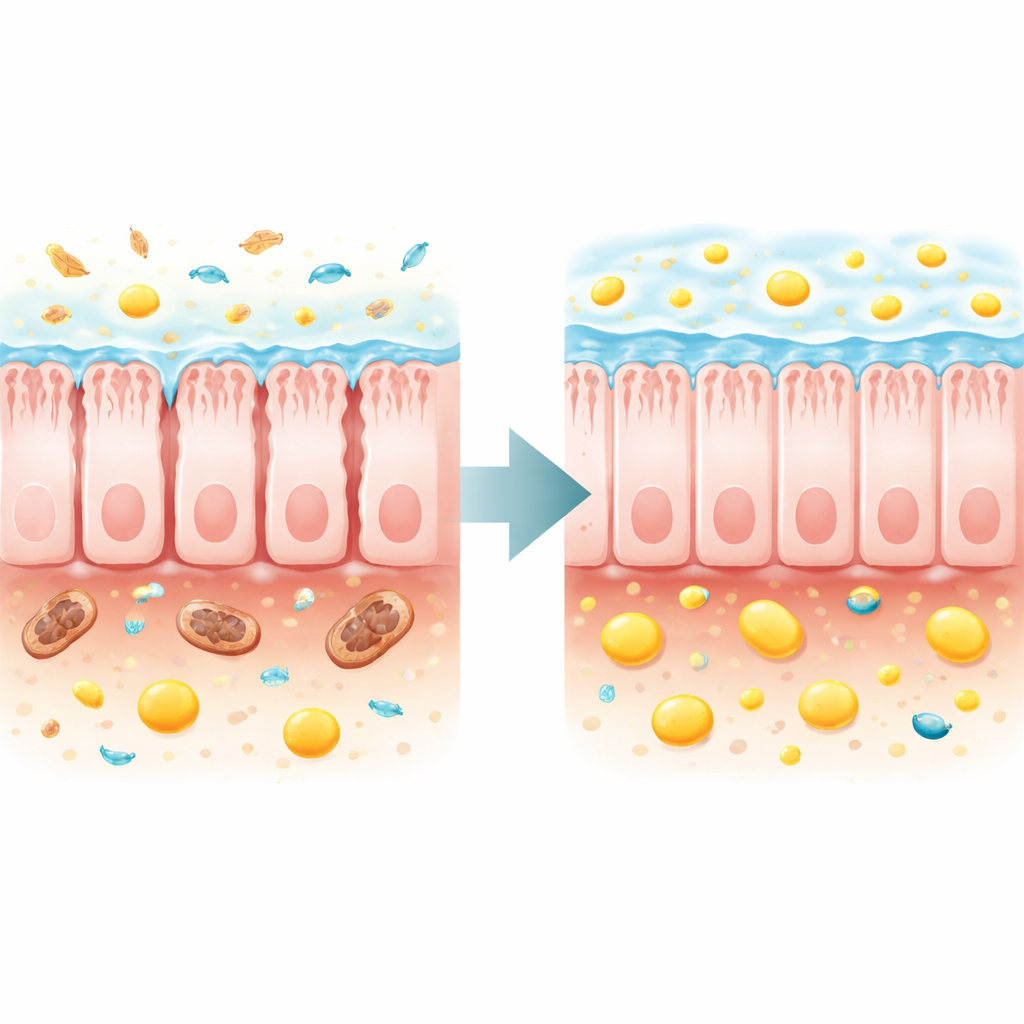
Reponer la ayuda microbiana perdida y reconstruir la barrera
Los autores se preguntaron entonces si reparar el ecosistema intestinal o restaurar directamente el butirato podría mejorar la salud de todo el organismo. Transferir microbios fecales de donantes sanos a los ratones deficientes en TFAM desaceleró modestamente la pérdida de peso, mejoró la fuerza muscular y el estreñimiento, elevó los niveles fecales de butirato y ácidos grasos relacionados, y aumentó la esperanza máxima de vida en aproximadamente un 70% en comparación con ratones que recibieron microbiota enferma. Un enfoque más dirigido empleó un suplemento dietético, tributirina, que se convierte en butirato en el intestino. Este tratamiento elevó el butirato fecal, retrasó el desgaste, fortaleció los músculos, normalizó la glucemia en ayunas y redujo el daño renal. De forma notable, amplió la mediana de vida en torno a una cuarta parte y la esperanza máxima de vida en más de tres cuartas partes en los ratones enfermos.
Cómo una molécula intestinal habla con los genes
Se sabe que el butirato no solo sirve como combustible para las células intestinales, sino también como señal química que puede influir en qué genes se activan o desactivan. En los ratones enfermos, los investigadores hallaron que etiquetas químicas específicas en las proteínas histonas—pequeños grupos acilo añadidos a la histona H3 en posiciones definidas—se reducían mucho en el tejido intestinal. Estas marcas ayudan a abrir el ADN alrededor de genes que preservan la barrera intestinal y gestionan el estrés. Agotar la microbiota de ratones sanos con antibióticos produjo una pérdida similar de estas marcas, vinculándolas a los metabolitos microbianos. Alimentar a los ratones deficientes en TFAM con tributirina restauró estas modificaciones de histonas y desplazó la actividad génica intestinal hacia un patrón más saludable, incluyendo genes implicados en las uniones célula‑a‑célula, el armazón del tejido y las respuestas al daño oxidativo.
Una nueva forma de apoyar a las mitocondrias que fallan
En términos sencillos, este estudio sugiere que cuando las mitocondrias fallan, el intestino se vuelve permeable y sus microbios aliados cambian, dejando al organismo sin butirato. Esa pérdida, a su vez, debilita la barrera intestinal y altera la regulación génica, alimentando la enfermedad sistémica. Reconstruir la asociación entre el huésped y la microbiota—ya sea trasplantando una comunidad microbiana más sana o suministrando un suplemento liberador de butirato—puede aliviar muchos síntomas y prolongar la vida en ratones con disfunción mitocondrial severa. Aunque se necesita mucho trabajo antes de que tales estrategias puedan aplicarse a las personas, los hallazgos ponen de relieve el intestino y su química microbiana como palancas prometedoras para tratar trastornos arraigados en centrales celulares deterioradas.
Cita: Gabandé-Rodríguez, E., Gómez de las Heras, M.M., Ramírez-Ruiz de Erenchun, P. et al. Butyrate extends health and lifespan in mice with mitochondrial deficiency. Nat Commun 17, 3909 (2026). https://doi.org/10.1038/s41467-026-70547-4
Palabras clave: enfermedad mitocondrial, microbioma intestinal, butirato, barrera intestinal, ácidos grasos de cadena corta