Clear Sky Science · de
Butyrat verlängert Gesundheit und Lebensdauer bei Mäusen mit mitochondrialer Defizienz
Warum der Darm für versagende Zellkraftwerke wichtig ist
Mitochondriale Erkrankungen sind seltene Störungen, bei denen die winzigen „Kraftwerke“ in unseren Zellen zu versagen beginnen, eine Kaskade von Problemen in vielen Organen auslösen und oft die Lebensspanne verkürzen. Die heutigen Behandlungen beschränken sich meist auf die Symptombehandlung. Diese Studie an Mäusen enthüllt einen unerwarteten Verbündeten im Darm: bestimmte Bakterien, die eine Fettsäure namens Butyrat produzieren. Die Arbeit zeigt, dass die Wiederherstellung dieses darmabgeleiteten Moleküls einen undichten Darm abdichten, mehrere altersähnliche Erkrankungen lindern und die Lebensdauer von Tieren mit schweren mitochondrialen Defekten deutlich verlängern kann.
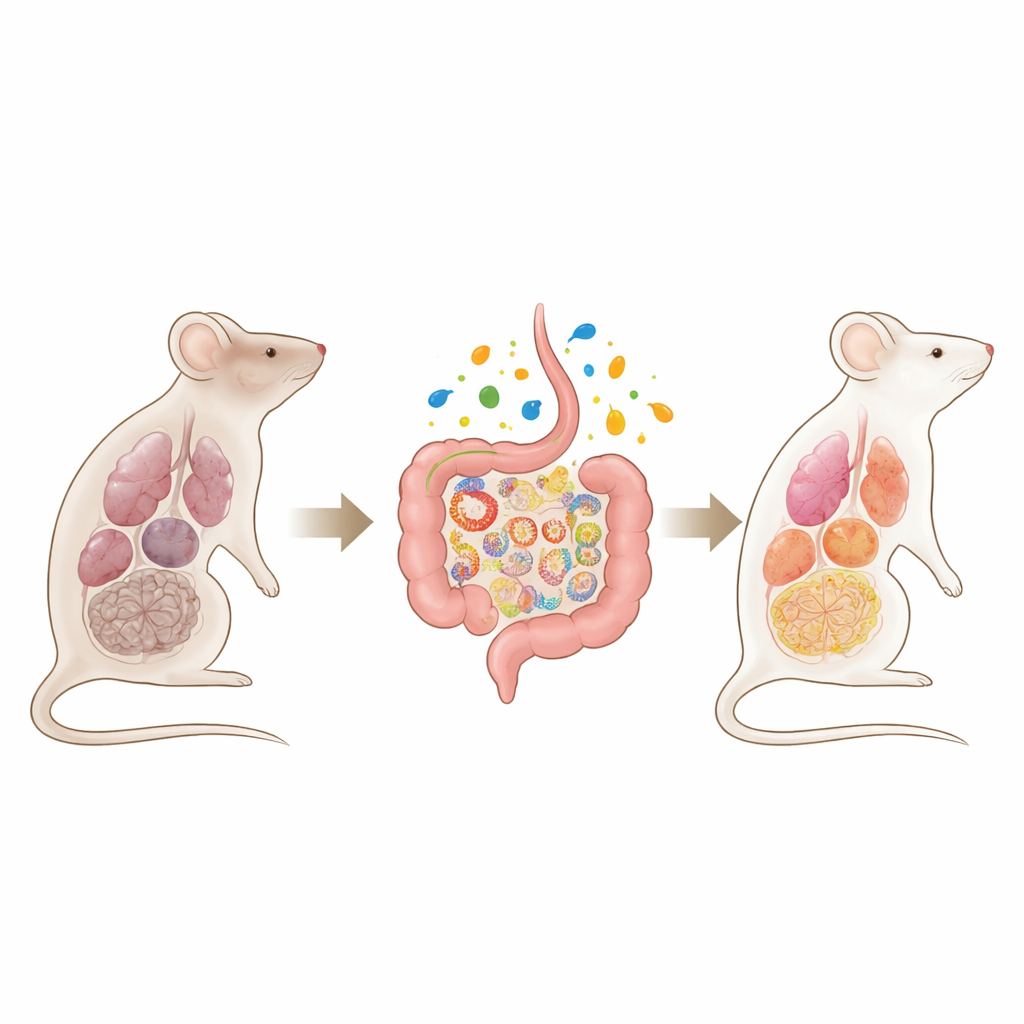
Wenn die Zellkraftwerke versagen
Die Forschenden erzeugten zunächst eine Maus, bei der ein wichtiger mitochondrialer Regulator, TFAM, im Erwachsenenalter im ganzen Körper abgeschaltet werden kann. Sobald dieser molekulare „Wächter“ der mitochondrialen DNA entfernt war, entwickelten die Tiere rasch ein Syndrom, das beschleunigtem Altern ähnelt: Verlust von Fett und Muskelmasse, schwacher Griff, schlechte Blutzuckerregulation, Lungenvernarbung, Herz‑ und Gefäßanomalien, Nierenversagen, Anämie und Anzeichen von Gehirnabbau einschließlich Bewegungsstörungen und beeinträchtigtem Nistverhalten. Viele Organe zeigten Entzündungen und molekulare Marker zellulärer Seneszenz, und die Mäuse starben vorzeitig, was darauf hindeutet, dass ein weitreichendes mitochondriales Versagen allein einen Multi‑Organ‑Kollaps antreiben kann.
Ein undichter Darm und eine gestörte mikrobielle Gemeinschaft
Da Mitochondrien für die Gesundheit der Darmzellen entscheidend sind, untersuchte das Team die Därme der Tiere. Sie fanden verkürzte Darmstrukturen, weniger teilende Zellen und eine dünnere schützende Schleimschicht trotz normaler Anzahl schleimproduzierender Becherzellen. Mehr dieser Zellen blieben „festgehalten“, indem sie Schleim zurückhielten statt ihn freizusetzen. Gene, die dabei helfen, die Zwischenräume zwischen Zellen zu verschließen und antimikrobielle Abwehrstoffe zu produzieren, waren herunterreguliert, und der Darm wurde durchlässiger: ein fluoreszierender Tracer gelangte ins Blut und ein Blutmarker bakterieller Produkte stieg stark an. Gleichzeitig verschob sich die Zusammensetzung der Darmbakterien. Mikroben, die üblicherweise von Nahrungskohlenhydraten leben und gesundheitsfördernde kurzkettige Fettsäuren produzieren, gingen zurück, während andere Gruppen zunahmen. Chemische Analysen bestätigten, dass die Spiegel aller wichtigen kurzkettigen Fettsäuren im Kot und mehrerer im Blut deutlich reduziert waren.
Ein ähnliches Muster in einem weiteren Modell mitochondrialer Erkrankung
Um zu prüfen, ob diese Darmstörung auf einen genetischen Trick beschränkt war, wandten sich die Wissenschaftler einer zweiten Mausstamm zu, der im Alter zufällig Mutationen in mitochondrialer DNA anhäuft und vorzeitige Multimorbidität entwickelt. Auch diese Tiere hatten eine undichtere Darmbarriere, reduzierte Expression von Junction‑ und antimikrobiellen Genen sowie eine vereinfachte, unausgewogene Gemeinschaft von Darmmikroben. Insbesondere Bakterien, die auf die Produktion von Butyrat spezialisiert sind, waren reduziert, und die Butyratspiegel im Kot waren selektiv erniedrigt, während andere kurzkettige Fettsäuren relativ verschont blieben. Das deutet darauf hin, dass der Verlust butyratproduzierender Partner ein gemeinsames Kennzeichen mitochondrialer Verschlechterung ist.
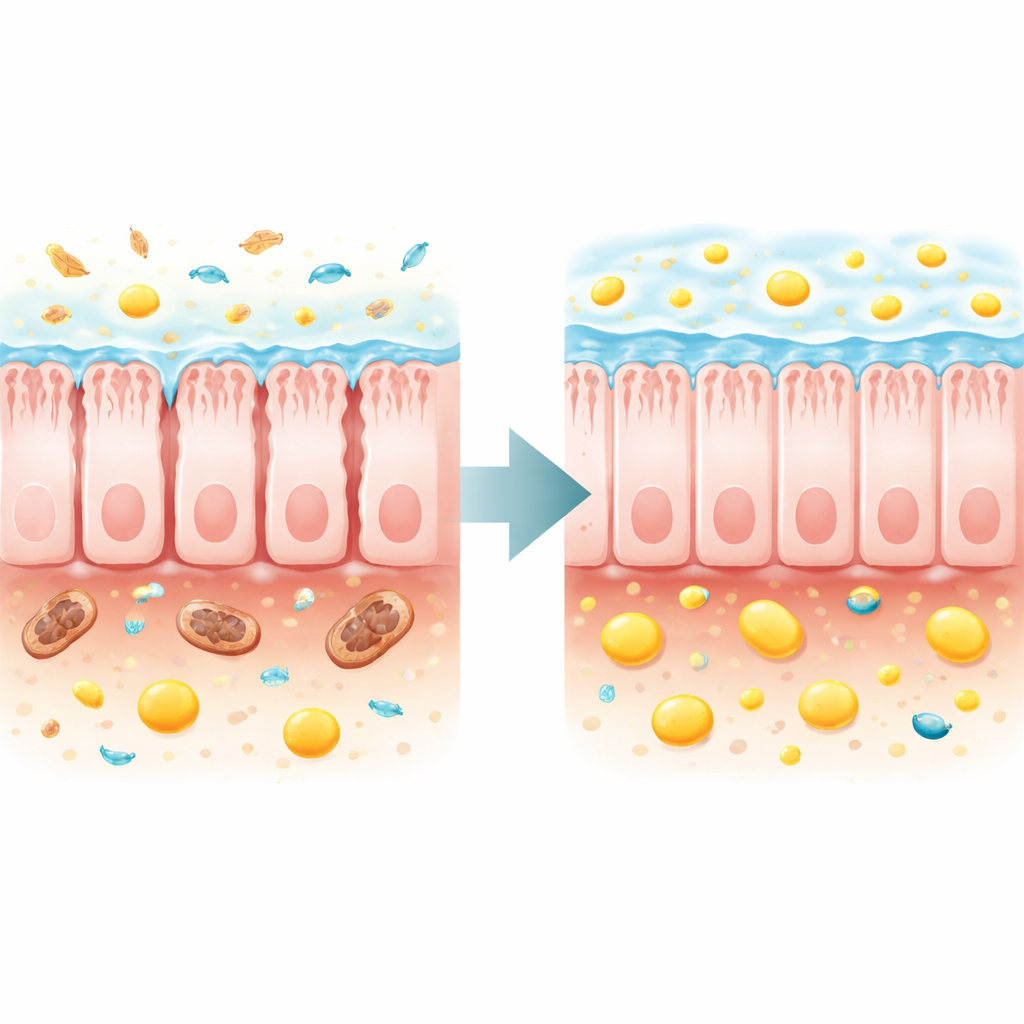
Verlorene mikrobielle Hilfe ersetzen und die Barriere wieder aufbauen
Die Autor:innen fragten dann, ob die Reparatur des Darmökosystems oder die direkte Wiederherstellung von Butyrat die Gesundheit des gesamten Körpers verbessern könnte. Die Übertragung von kotbürtigen Mikroben gesunder Spender auf TFAM‑defiziente Mäuse verlangsamte den Gewichtsverlust moderat, verbesserte Muskelkraft und Verstopfung, erhöhte Butyrat und verwandte Fettsäuren im Kot und verlängerte die maximale Lebensdauer um etwa 70 % im Vergleich zu Mäusen, die krankes Mikrobiota erhielten. Ein gezielterer Ansatz verwendete ein Nahrungsergänzungsmittel, Tributyrin, das im Darm in Butyrat umgewandelt wird. Diese Behandlung erhöhte das Butyrat im Kot, verzögerte die Auszehrung, stärkte die Muskeln, normalisierte den Nüchternblutzucker und verringerte Nierenschäden. Bemerkenswerterweise verlängerte sie die mediane Lebensdauer der kranken Mäuse um ungefähr ein Viertel und die maximale Lebensdauer um mehr als drei Viertel.
Wie ein Darmmolekül mit Genen kommuniziert
Butyrat ist nicht nur als Brennstoff für Darmzellen bekannt, sondern auch als chemisches Signal, das beeinflussen kann, welche Gene an‑ oder abgeschaltet werden. In den erkrankten Mäusen fanden die Forschenden, dass bestimmte chemische Markierungen an Histonproteinen – kleine Acylgruppen, die an definierten Positionen an Histon H3 angefügt sind – im Darmgewebe stark reduziert waren. Diese Markierungen helfen, die DNA um Gene zu öffnen, die die Barriere des Darms erhalten und mit Stress umgehen. Die Entleerung normaler Mäuse von ihrem Mikrobiom durch Antibiotika führte zu einem ähnlichen Verlust dieser Markierungen und verband sie so mit mikrobiellen Metaboliten. Die Fütterung der TFAM‑defizienten Mäuse mit Tributyrin stellte diese Histonmodifikationen wieder her und verschob die intestinale Genaktivität zurück zu einem gesünderen Muster, einschließlich Genen, die an Zell‑zu‑Zell‑Verbindungen, dem Gerüst des Gewebes und Antworten auf oxidative Schäden beteiligt sind.
Ein neuer Weg, versagende Mitochondrien zu unterstützen
Vereinfacht gesagt legt diese Studie nahe, dass, wenn Mitochondrien versagen, der Darm undicht wird und seine freundlichen Mikroben sich verändern, wodurch der Körper an Butyrat verarmt. Dieser Verlust schwächt wiederum die Darmbarriere und stört die Genregulation, was systemische Erkrankungen antreibt. Die Wiederherstellung der Partnerschaft zwischen Wirt und Mikrobiota – entweder durch Transplantation einer gesünderen mikrobiellen Gemeinschaft oder durch Zufuhr eines butyratfreisetzenden Ergänzungsmittels – kann viele Symptome lindern und das Leben von Mäusen mit schwerer mitochondrialer Dysfunktion verlängern. Obwohl noch viel Arbeit nötig ist, bevor solche Strategien beim Menschen angewandt werden können, heben die Befunde den Darm und seine mikrobielle Chemie als vielversprechende neue Ansatzpunkte für die Behandlung von Erkrankungen hervor, die in defekten zellulären Kraftwerken wurzeln.
Zitation: Gabandé-Rodríguez, E., Gómez de las Heras, M.M., Ramírez-Ruiz de Erenchun, P. et al. Butyrate extends health and lifespan in mice with mitochondrial deficiency. Nat Commun 17, 3909 (2026). https://doi.org/10.1038/s41467-026-70547-4
Schlüsselwörter: mitochondriale Krankheit, Darmmikrobiom, Butyrat, intestinaler Barrier, kurzkettige Fettsäuren