Clear Sky Science · ru
Бутира́т продлевает здоровье и продолжительность жизни у мышей с митохондриальной недостаточностью
Почему кишечник важен при сбоях «энергетических станций» клеток
Митохондриальные болезни — редкие расстройства, при которых крошечные «электростанции» внутри клеток начинают давать сбой, вызывая каскад проблем во многих органах и часто сокращая продолжительность жизни. Современные методы лечения в основном направлены на облегчение симптомов. Исследование на мышах выявляет неожиданный союзник, обитающий в кишечнике: некоторые бактерии, продуцирующие жирную кислоту бутират. Работа показывает, что восстановление этого кишечного метаболита может укрепить протекающий кишечник, смягчить множество проявлений, сходных со старением, и значительно продлить жизнь животных с тяжёлыми митохондриальными дефектами.
Когда «энергетические станции» клеток выходят из строя
Исследователи сначала создали мышь, у которой ключевой митохондриальный регулятор TFAM можно выключить по всему организму во взрослом возрасте. После удаления этого молекулярного «хранителя» митохондриальной ДНК животные быстро развили синдром, напоминающий ускорённое старение: потерю жира и мышечной массы, слабый захват, нарушение контроля уровня сахара в крови, рубцевание лёгких, изменения в сердце и сосудах, почечную недостаточность, анемию и признаки дегенерации мозга, включая нарушения движений и ухудшение способности обустраивать гнёзда. Во многих органах наблюдалось воспаление и молекулярные маркёры клеточного сенесценса, а мыши умирали преждевременно, что указывает на то, что широкомасштабная митохондриальная недостаточность сама по себе может приводить к полиорганной декомпенсации.
Протекающий кишечник и нарушенное микробное сообщество
Поскольку митохондрии важны для здоровья кишечных клеток, команда изучила кишечник животных. Они обнаружили укороченные кишечные структуры, меньше делящихся клеток и более тонкий защитный слой слизи при нормальном числе бокаловидных клеток, производящих слизь. Больше таких клеток «застревало», удерживая слизь вместо её высвобождения. Гены, обеспечивающие уплотнение межклеточных контактов и выработку антимикробной защиты, были подавлены, и кишечник стал более проницаемым: флуоресцентный трассер проникал в кровь, а в крови резко повышался маркёр бактериальных продуктов. В то же время состав кишечной микробиоты сместился. Микробы, обычно питающиеся диетическими углеводами и производящие полезные короткоцепочечные жирные кислоты, сократилось, в то время как другие группы разрослись. Химический анализ подтвердил, что уровни всех основных короткоцепочечных жирных кислот в фекалиях и нескольких из них в крови были значительно снижены.
Общий паттерн в другой модели митохондриального заболевания
Чтобы выяснить, уникально ли это нарушение кишечника для одной генетической манипуляции, учёные обратились ко второй штаммовой линии мышей, у которой с возрастом накапливаются случайные мутации в митохондриальной ДНК и развивается преждевременная множественная заболеваемость. У этих животных также наблюдался более проницаемый кишечный барьер, сниженная экспрессия генов плотных контактов и антимикробных факторов и более простое, несбалансированное сообщество кишечных микробов. В частности, бактерии, специализирующиеся на продуцировании бутирата, были истощены, и уровни бутирата в фекалиях были избирательно ниже, тогда как другие короткоцепочечные жирные кислоты относительно сохранялись. Это указывало на утрату бутират-продуцирующих партнёров как на общий признак митохондриального упадка.
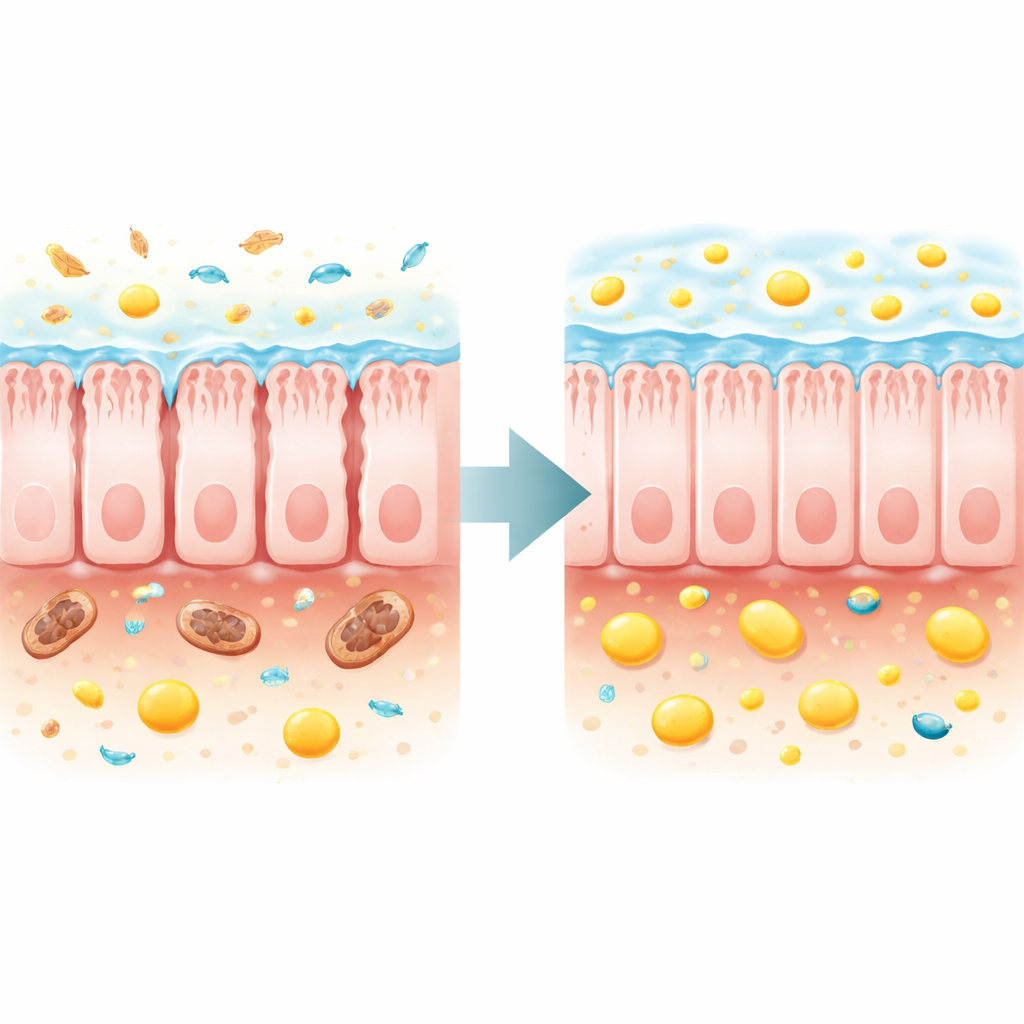
Восстановление утраченной микробной помощи и укрепление барьера
Авторы затем задали вопрос, может ли восстановление кишечной экосистемы или прямое восполнение бутирата улучшить здоровье всего организма. Перенос фекальной микробиоты от здоровых доноров мышам с дефицитом TFAM в умеренной степени замедлил потерю веса, улучшил силу мышц и запоры, повысил уровни фекального бутирата и родственных жирных кислот и увеличил максимальную продолжительность жизни примерно на 70% по сравнению с мышами, получившими поражённую микробиоту. Более целенаправленный подход использовал добавку в рацион — трибутирин, которая в кишечнике превращается в бутират. Это лечение повысило фекальный бутират, отсрочило истощение, укрепило мышцы, нормализовало уровень сахара в крови в голодании и уменьшило повреждение почек. Что примечательно, оно увеличило медиану продолжительности жизни примерно на четверть и максимальную продолжительность жизни более чем на три четверти у больных мышей.
Как молекула кишечника «разговаривает» с генами
Бутират известен не только как топливо для кишечных клеток, но и как химический сигнал, способный влиять на то, какие гены включаются или выключаются. У больных мышей исследователи обнаружили, что специфические химические метки на гистонах — небольшие ацилированные группы, добавляемые к гистону H3 в определённых позициях — были сильно уменьшены в тканях кишечника. Эти метки помогают раскручивать ДНК вокруг генов, которые поддерживают барьер кишечника и отвечают на стресс. Истощение нормальной микробиоты у здоровых мышей антибиотиками вызвало похожую потерю этих меток, связывая их с микробными метаболитами. Кормление TFAM‑дефицитных мышей трибутирином восстановило эти гистоновые модификации и вернуло активность кишечных генов к более здоровому профилю, включая гены, участвующие в межклеточных контактах, структурной опоре ткани и ответах на окислительное повреждение.
Новый способ поддержать умирающие митохондрии
Проще говоря, это исследование показывает, что при сбое митохондрий кишечник становится проницаемым, его дружелюбные микробы меняются, и организму не хватает бутирата. Эта утрата ослабляет кишечный барьер и нарушает регуляцию генов, подпитывая системное заболевание. Восстановление партнёрства между хозяином и микробиотой — либо пересадкой более здорового микробного сообщества, либо поставкой добавки, выделяющей бутират — может смягчить многие симптомы и продлить жизнь мышей с тяжёлой митохондриальной дисфункцией. Хотя до применения таких стратегий у людей ещё далеко, результаты подчёркивают кишечник и его микробную химию как перспективные новые рычаги для лечения расстройств, связанных с нарушением клеточных «энергетических станций».
Цитирование: Gabandé-Rodríguez, E., Gómez de las Heras, M.M., Ramírez-Ruiz de Erenchun, P. et al. Butyrate extends health and lifespan in mice with mitochondrial deficiency. Nat Commun 17, 3909 (2026). https://doi.org/10.1038/s41467-026-70547-4
Ключевые слова: митохондриальная болезнь, микробиом кишечника, бутират, кишечный барьер, короткоцепочечные жирные кислоты