Clear Sky Science · it
Il butirrato estende salute e durata della vita nei topi con deficit mitocondriale
Perché l’intestino conta per gli “impianti di energia” che cedono
Le malattie mitocondriali sono disturbi rari in cui le piccole “centrali” all’interno delle nostre cellule cominciano a guastarsi, scatenando una cascata di problemi in molti organi e spesso accorciando la vita. Le terapie attuali sono per lo più limitate alla gestione dei sintomi. Questo studio nei topi scopre un alleato inaspettato che vive nell’intestino: alcuni batteri che producono un acido grasso chiamato butirrato. Il lavoro mostra che ripristinare questa molecola di origine intestinale può riparare un intestino permeabile, alleviare molte patologie simili all’invecchiamento e prolungare significativamente la durata della vita in animali con gravi difetti mitocondriali.
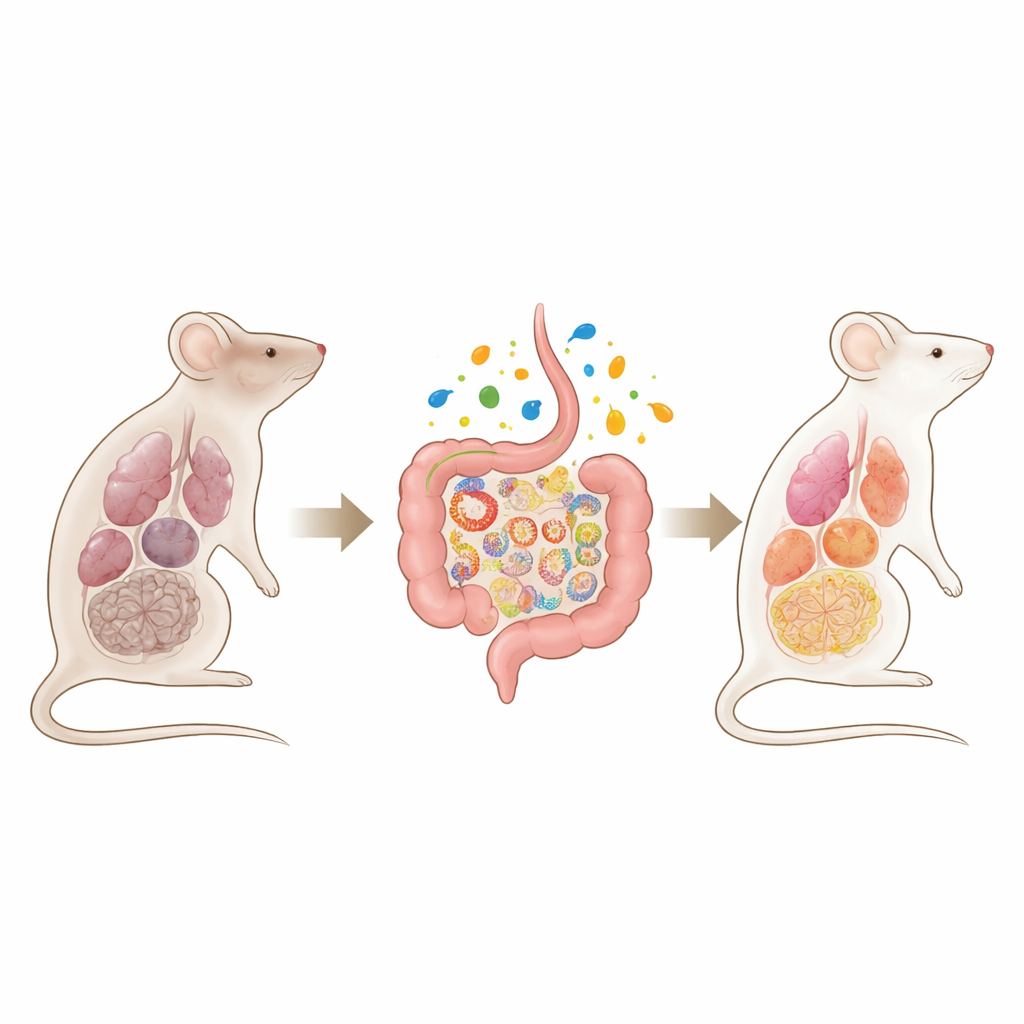
Quando gli impianti energetici cellulari si guastano
I ricercatori hanno prima creato un topo in cui un regolatore mitocondriale chiave, TFAM, può essere spento in tutto il corpo in età adulta. Una volta rimosso questo “guardiano” molecolare del DNA mitocondriale, gli animali hanno sviluppato rapidamente una sindrome che somiglia a un invecchiamento accelerato: perdita di grasso e muscolo, presa debole, cattivo controllo della glicemia, fibrosi polmonare, anomalie di cuore e vasi, insufficienza renale, anemia e segni di degenerazione cerebrale, inclusi problemi di movimento e comportamento di nidificazione compromesso. Molti organi mostravano infiammazione e marcatori molecolari di senescenza cellulare, e i topi morivano prematuramente, indicando che il guasto mitocondriale diffuso da solo può guidare il collasso multi‑organo.
Un intestino permeabile e una comunità microbica alterata
Poiché i mitocondri sono fondamentali per la salute delle cellule intestinali, il team ha esaminato l’intestino degli animali. Hanno trovato strutture intestinali più corte, meno cellule in proliferazione e uno strato protettivo di muco più sottile nonostante un numero normale di cellule caliciformi produttrici di muco. Più di queste cellule risultavano “bloccate” trattenendo il muco invece di rilasciarlo. I geni che aiutano a sigillare gli spazi tra le cellule e a produrre difese antimicrobiche erano down‑regolati, e l’intestino è diventato più permeabile: un tracciante fluorescente è passato nel sangue e un indicatore ematico di prodotti batterici è aumentato nettamente. Allo stesso tempo, la composizione dei batteri intestinali è cambiata. I microbi che normalmente prosperano sui carboidrati alimentari e producono acidi grassi a catena corta benefici sono diminuiti, mentre altri gruppi si sono espansi. L’analisi chimica ha confermato che i livelli di tutti gli acidi grassi a catena corta principali nelle feci, e diversi nel sangue, erano nettamente ridotti.
Un modello ricorrente in un altro modello di malattia mitocondriale
Per verificare se questa perturbazione intestinale fosse un fenomeno limitato a un trucco genetico, gli scienziati si sono rivolti a una seconda linea di topi che accumulano mutazioni casuali nel DNA mitocondriale con l’età e sviluppano multimorbilità prematura. Anche questi animali avevano una barriera intestinale più permeabile, espressione ridotta di geni delle giunzioni e antimicrobici, e una comunità microbica intestinale più semplice e sbilanciata. In particolare, i batteri specializzati nella produzione di butirrato erano impoveriti, e i livelli fecali di butirrato risultavano selettivamente più bassi, mentre altri acidi grassi a catena corta erano relativamente risparmiati. Ciò suggerisce che la perdita dei partner produttori di butirrato sia un segno comune del declino mitocondriale.
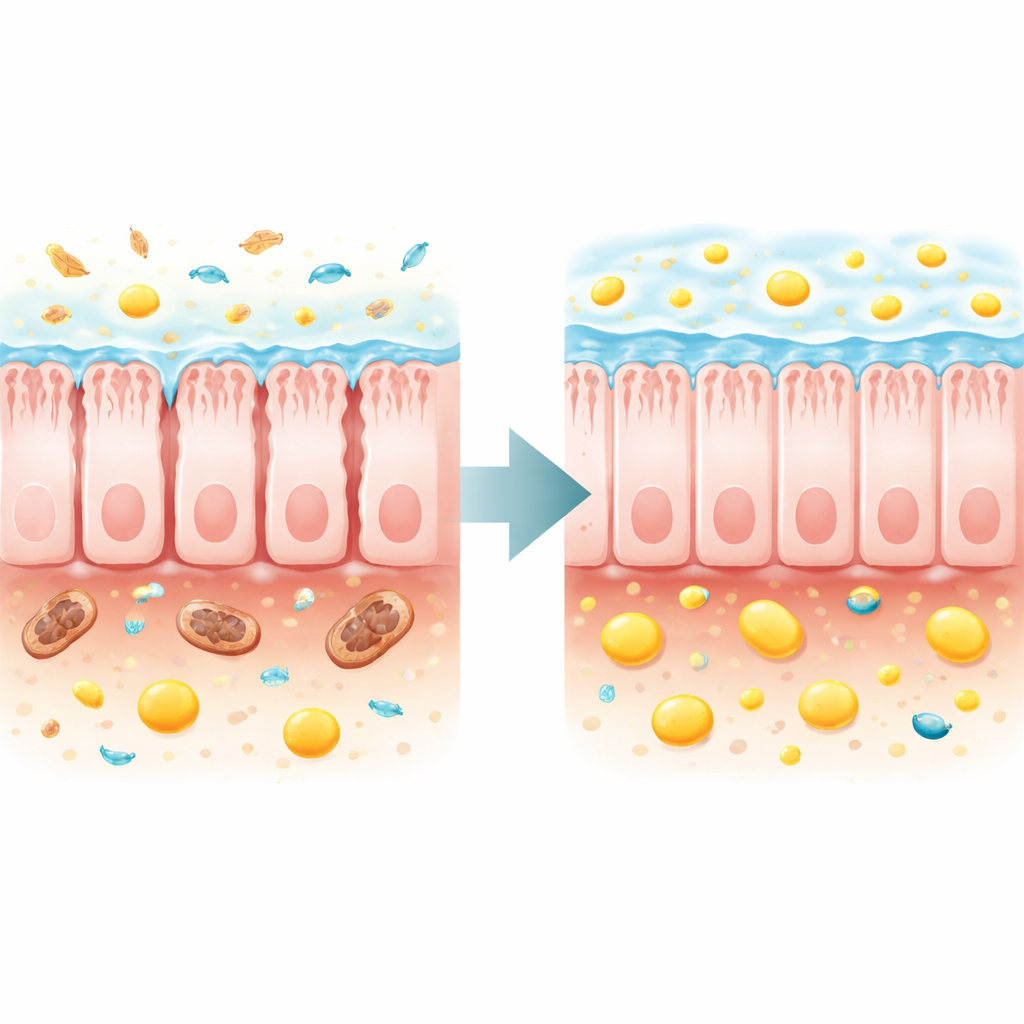
Sostituire l’aiuto microbico perso e ricostruire la barriera
Gli autori si sono poi chiesti se riparare l’ecosistema intestinale o ripristinare direttamente il butirrato potesse migliorare la salute dell’intero organismo. Il trapianto di microbi fecali da donatori sani nei topi TFAM‑deficienti ha rallentato modestamente la perdita di peso, migliorato la forza muscolare e la stitichezza, aumentato il butirrato fecale e acidi grassi correlati, e allungato la massima durata della vita di circa il 70% rispetto ai topi che ricevevano microbiota malato. Un approccio più mirato ha usato un integratore alimentare, il tributirina, che viene convertito in butirrato nell’intestino. Questo trattamento ha aumentato il butirrato fecale, ritardato il deperimento, rafforzato i muscoli, normalizzato la glicemia a digiuno e ridotto il danno renale. In modo notevole, ha esteso la durata mediana della vita di circa un quarto e la durata massima di più dei tre quarti nei topi malati.
Come una molecola intestinale comunica con i geni
Il butirrato è noto non solo come combustibile per le cellule intestinali ma anche come segnale chimico che può influenzare quali geni vengono attivati o silenziati. Nei topi malati, i ricercatori hanno trovato che specifici segni chimici sulle proteine istoniche—piccoli gruppi acilici aggiunti all’istone H3 in posizioni definite—erano fortemente ridotti nel tessuto intestinale. Questi segni aiutano ad aprire il DNA attorno ai geni che preservano la barriera intestinale e gestiscono lo stress. Privare topi normali del loro microbiota con antibiotici ha prodotto una perdita simile di questi marcatori, collegandoli ai metaboliti microbici. Somministrare tributirina ai topi TFAM‑deficienti ha ripristinato queste modificazioni istoniche e ha spostato l’attività genica intestinale verso un profilo più sano, includendo geni coinvolti nelle giunzioni cellula‑cellula, nello scheletro del tessuto e nelle risposte al danno ossidativo.
Un nuovo modo per sostenere mitocondri in difficoltà
In termini semplici, questo studio suggerisce che quando i mitocondri vacillano, l’intestino diventa permeabile e i suoi microbi “amici” cambiano, privando l’organismo di butirrato. Questa perdita, a sua volta, indebolisce la barriera intestinale e altera la regolazione genica, alimentando la malattia sistemica. Ricostruire la collaborazione tra ospite e microbiota—tramite il trapianto di una comunità microbica più sana o fornendo un integratore che rilascia butirrato—può alleviare molti sintomi e prolungare la vita nei topi con grave disfunzione mitocondriale. Pur richiedendo molto lavoro prima di poter applicare tali strategie alle persone, i risultati sottolineano l’intestino e la sua chimica microbica come leve promettenti per trattare disturbi radicati in centrali energetiche cellulari danneggiate.
Citazione: Gabandé-Rodríguez, E., Gómez de las Heras, M.M., Ramírez-Ruiz de Erenchun, P. et al. Butyrate extends health and lifespan in mice with mitochondrial deficiency. Nat Commun 17, 3909 (2026). https://doi.org/10.1038/s41467-026-70547-4
Parole chiave: malattia mitocondriale, microbioma intestinale, butirrato, barriera intestinale, acidi grassi a catena corta