Clear Sky Science · nl
Butyraat verlengt gezondheid en levensduur bij muizen met mitochondriale tekortkoming
Waarom de darm telt bij falende cel‑motoren
Mitochondriale ziekten zijn zeldzame aandoeningen waarbij de kleine "energiecentrales" in onze cellen beginnen te falen, wat een cascade van problemen in vele organen veroorzaakt en vaak de levensduur verkort. Behandelingen zijn vandaag grotendeels beperkt tot symptoombeheer. Deze studie in muizen onthult een onverwachte bondgenoot in de darm: bepaalde bacteriën die een vetzuur produceren dat butyraat heet. Het werk toont aan dat het herstel van dit darmafgeleide molecuul een lekkende darm kan herstellen, meerdere ouderdomsachtige ziekten kan verlichten en de levensduur van dieren met ernstige mitochondriale defecten aanzienlijk kan verlengen.
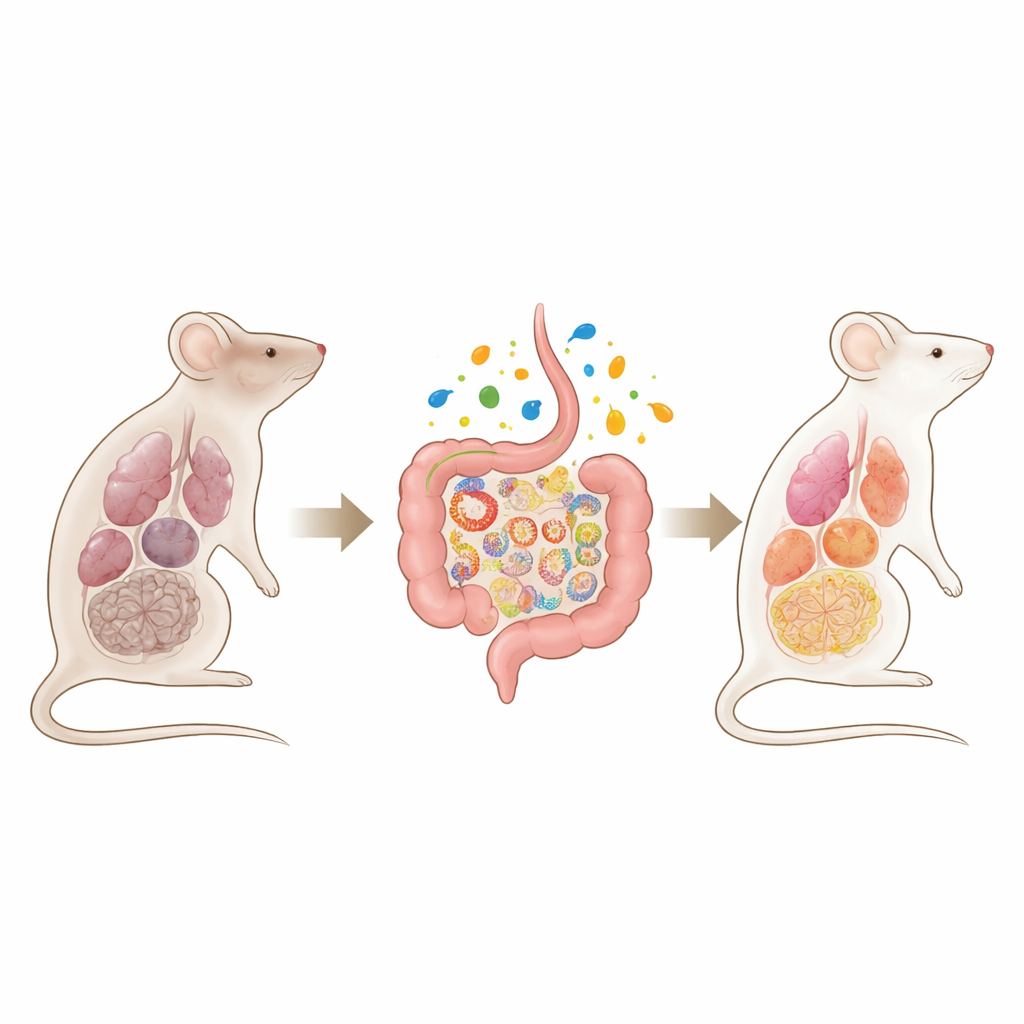
Wanneer celenergiecentrales stukgaan
De onderzoekers maakten eerst een muismodel waarin een belangrijke mitochondriale regelaar, TFAM, in de volwassenheid door het hele lichaam kon worden uitgeschakeld. Zodra deze moleculaire "bewaker" van mitochondriaal DNA werd verwijderd, ontwikkelden de dieren snel een syndroom dat op versnelde veroudering leek: verlies van vet en spiermassa, zwakke grijpkracht, slechte bloedsuikerregeling, longfibrose, afwijkingen aan hart en bloedvaten, nierfalen, bloedarmoede en tekenen van hersendegeneratie zoals bewegingsproblemen en verminderd nestgedrag. Veel organen toonden ontsteking en moleculaire merkers van cellulaire senescentie, en de muizen stierven voortijdig, wat aangeeft dat wijdverspreid mitochondriaal falen op zichzelf multiorgaanstoring kan veroorzaken.
Een lekkende darm en een verstoorde microbioomgemeenschap
Aangezien mitochondriën cruciaal zijn voor de gezondheid van darmcellen, onderzochten de onderzoekers de darmen van de dieren. Ze vonden kortere darmslijmvormingen, minder delende cellen en een dunnere beschermende slijmlaag ondanks normale aantallen slijmproducerende gobletcellen. Meer van deze cellen zaten "vast" met vastgehouden slijm in plaats van het los te laten. Genen die helpen de ruimtes tussen cellen af te dichten en antimicrobiële verdedigingen produceren, waren minder actief, en de darm werd permeabeler: een fluorescerende tracer lekte in het bloed en een bloedmarker voor bacteriële producten steeg sterk. Tegelijkertijd verschoof de samenstelling van de darmmicrobiota. Microben die gewoonlijk gedijen op voedingsrijke koolhydraten en gezondheidsbevorderende korte-keten vetzuren produceren, namen af, terwijl andere groepen toenamen. Chemische analyse bevestigde dat de niveaus van alle belangrijke korte-keten vetzuren in feces, en meerdere in bloed, duidelijk waren verlaagd.
Eenzelfde patroon in een ander mitochondriaal ziektmodel
Om te onderzoeken of deze darmverstoring uniek was voor één genetische ingreep, bestudeerden de wetenschappers een tweede muizenstam die met het ouder worden willekeurige mutaties in mitochondriaal DNA accumuleert en voortijdige multimorbiditeit ontwikkelt. Ook deze dieren hadden een lekker darmslijmvlies, verminderde expressie van junction- en antimicrobiële genen en een eenvoudigere, uit balans geraakte gemeenschap van darmmicroben. In het bijzonder waren bacteriën die gespecialiseerd zijn in de productie van butyraat uitgeput, en waren de fecale butyraatniveaus selectief lager, terwijl andere korte-keten vetzuren relatief gespaard bleven. Dit wees erop dat het verlies van butyraat-producerende partners een gemeenschappelijk kenmerk is van mitochondriale achteruitgang.
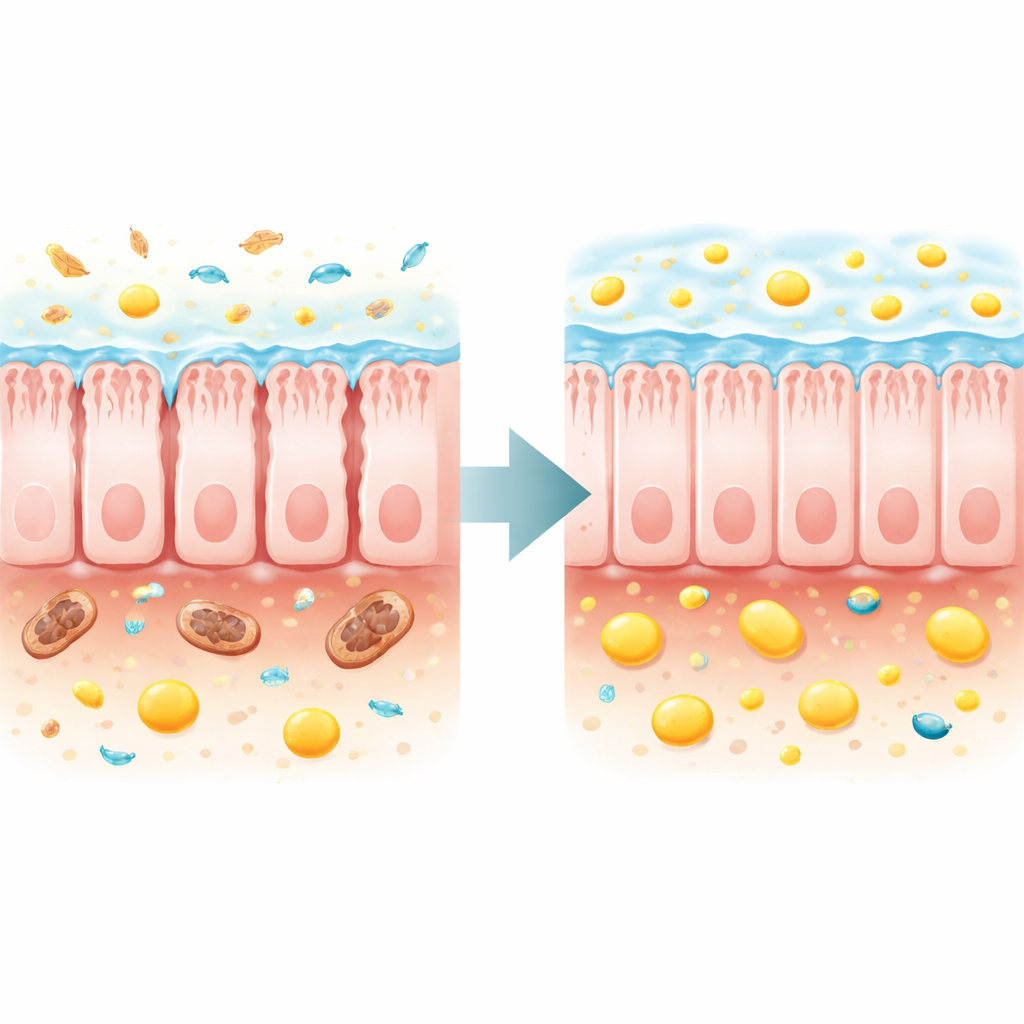
Het vervangen van verloren microbieel hulp en herbouwen van de barrière
De auteurs vroegen zich vervolgens af of het herstellen van het darmecosysteem of het direct aanvullen van butyraat de algehele gezondheid zou kunnen verbeteren. Het overbrengen van fecale microben van gezonde donoren naar de TFAM-deficiënte muizen vertraagde het gewichtsverlies bescheiden, verbeterde spierkracht en constipatie, verhoogde fecaal butyraat en aanverwante vetzuren, en verlengde de maximale levensduur met ongeveer 70% vergeleken met muizen die ziek microbiota ontvingen. Een gerichtere benadering gebruikte het voedingssupplement tributyrine, dat in de darm wordt omgezet in butyraat. Deze behandeling verhoogde fecaal butyraat, vertraagde het verval, versterkte spieren, normaliseerde nuchtere bloedsuiker en verminderde nierbeschadiging. Opmerkelijk verlengde het de mediane levensduur met ruwweg een kwart en de maximale levensduur met meer dan driekwart bij de zieke muizen.
Hoe een darmmolecuul met genen communiceert
Butyraat staat niet alleen bekend als brandstof voor darmcellen, maar ook als een chemisch signaal dat kan beïnvloeden welke genen aan of uit gaan. Bij de zieke muizen vonden de onderzoekers dat specifieke chemische tags op histon-eiwitten—kleine acylgroepen toegevoegd aan histon H3 op gedefinieerde posities—sterk verlaagd waren in darmsweefsel. Deze tags helpen het DNA rond genen die de darmbarrière behouden en omgaan met stress open te zetten. Het ontdoen van normale muizen van hun microbiota met antibiotica leidde tot een vergelijkbaar verlies van deze merkers, wat ze koppelt aan microbiele metabolieten. Het voeren van tributyrine aan de TFAM-deficiënte muizen herstelde deze histonmodificaties en verschuift de intestinale genactiviteit terug naar een gezonder patroon, inclusief genen die betrokken zijn bij cel-tot-cel verbindingen, het geraamte van het weefsel en reacties op oxiderende schade.
Een nieuwe manier om falende mitochondriën te ondersteunen
In eenvoudige bewoordingen suggereert deze studie dat wanneer mitochondriën falen, de darm lek wordt en zijn vriendelijke microben veranderen, waardoor het lichaam butyraat tekortkomt. Dat verlies verzwakt op zijn beurt de darmbarrière en verstoort genregulatie, wat systemische ziekte aanwakkert. Het herbouwen van de samenwerking tussen gastheer en microbiota—hetzij door het transplanteren van een gezondere microbieel gemeenschap, hetzij door het toedienen van een butyraat-afgevend supplement—kan veel symptomen verlichten en het leven verlengen bij muizen met ernstige mitochondriale dysfunctie. Hoewel veel werk nodig is voordat dergelijke strategieën op mensen kunnen worden toegepast, benadrukken de bevindingen de darm en haar microbieel chemie als veelbelovende nieuwe aangrijpingspunten voor de behandeling van aandoeningen die hun oorsprong vinden in gebroken cellulaire energiecentrales.
Bronvermelding: Gabandé-Rodríguez, E., Gómez de las Heras, M.M., Ramírez-Ruiz de Erenchun, P. et al. Butyrate extends health and lifespan in mice with mitochondrial deficiency. Nat Commun 17, 3909 (2026). https://doi.org/10.1038/s41467-026-70547-4
Trefwoorden: mitochondriale ziekte, darmmicrobioom, butyraat, intestinale barrière, korte-keten vetzuren