Clear Sky Science · pt
Butirato amplia saúde e longevidade em camundongos com deficiência mitocondrial
Por que o intestino importa para máquinas celulares em falha
Doenças mitocondriais são transtornos raros nos quais as pequenas “usinas” dentro de nossas células começam a falhar, provocando uma cascata de problemas em vários órgãos e frequentemente reduzindo a expectativa de vida. Os tratamentos atuais limitam‑se, em grande parte, ao manejo dos sintomas. Este estudo em camundongos revela um aliado inesperado que vive no intestino: certas bactérias que produzem um ácido graxo chamado butirato. O trabalho mostra que restaurar essa molécula de origem intestinal pode reforçar um intestino permeável, aliviar múltiplas doenças com características de envelhecimento e estender significativamente a longevidade em animais com defeitos mitocondriais severos.
Quando as usinas celulares entram em colapso
Os pesquisadores primeiro engenheiraram um camundongo no qual um regulador mitocondrial chave, TFAM, pode ser desligado em todo o corpo na vida adulta. Quando esse “guardião” molecular do DNA mitocondrial foi removido, os animais desenvolveram rapidamente uma síndrome que lembra envelhecimento acelerado: perda de gordura e músculo, preensão fraca, controle glicêmico ruim, fibrose pulmonar, anomalias do coração e vasos, insuficiência renal, anemia e sinais de degeneração cerebral incluindo problemas de movimento e comportamento de nidificação prejudicado. Muitos órgãos exibiram inflamação e marcadores moleculares de senescência celular, e os camundongos morreram prematuramente, indicando que a falha mitocondrial generalizada por si só pode conduzir a uma quebra multiorgânica.
Um intestino permeável e uma comunidade microbiana alterada
Porque as mitocôndrias são cruciais para a saúde das células intestinais, a equipe examinou os intestinos dos animais. Eles encontraram estruturas intestinais mais curtas, menos células em divisão e uma camada protetora de muco mais fina, apesar de números normais de células caliciformes produtoras de muco. Mais dessas células estavam “presas” retendo muco em vez de liberá‑lo. Genes que ajudam a selar os espaços entre as células e produzir defesas antimicrobianas foram rebaixados, e o intestino tornou‑se mais permeável: traçador fluorescente passou para o sangue, e um marcador sanguíneo de produtos bacterianos aumentou acentuadamente. Ao mesmo tempo, a composição das bactérias intestinais mudou. Microorganismos que normalmente prosperam com carboidratos dietéticos e produzem ácidos graxos de cadeia curta benéficos diminuíram, enquanto outros grupos se expandiram. A análise química confirmou que os níveis de todos os principais ácidos graxos de cadeia curta nas fezes, e vários no sangue, estavam marcadamente reduzidos.
Um padrão comum em outro modelo de doença mitocondrial
Para verificar se essa perturbação intestinal era exclusiva de um truque genético, os cientistas recorreram a uma segunda linhagem de camundongos que acumula mutações aleatórias no DNA mitocondrial conforme envelhece e desenvolve multimorbidades prematuras. Esses animais também apresentaram uma barreira intestinal mais permeável, expressão reduzida de genes de junção e antimicrobianos, e uma comunidade microbiana intestinal mais simples e desequilibrada. Em particular, bactérias especializadas na produção de butirato estavam esgotadas, e os níveis fecais de butirato eram seletivamente menores, enquanto outros ácidos graxos de cadeia curta foram relativamente poupados. Isso apontou a perda de parceiros produtores de butirato como uma característica compartilhada do declínio mitocondrial.
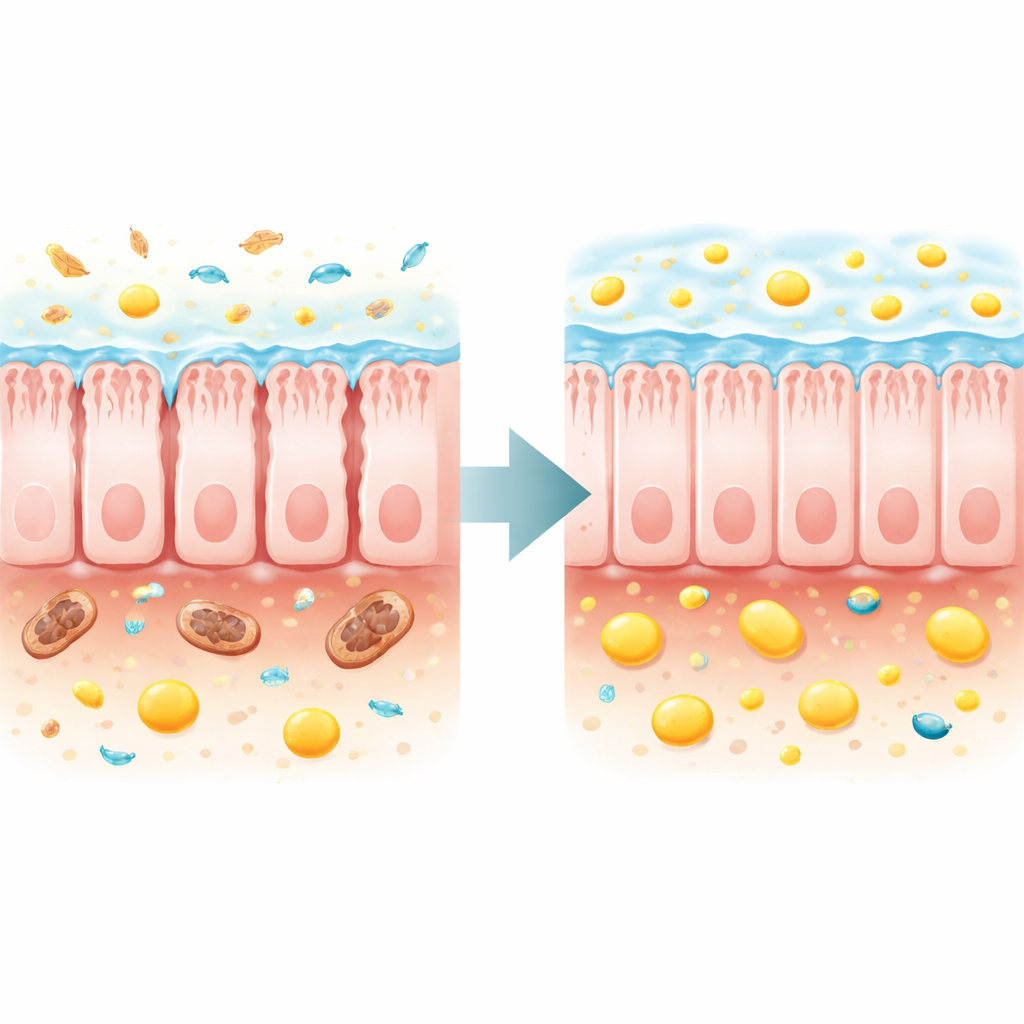
Substituindo a ajuda microbiana perdida e reconstruindo a barreira
Os autores então perguntaram se reparar o ecossistema intestinal ou restaurar diretamente o butirato poderia melhorar a saúde do corpo inteiro. A transferência de microrganismos fecais de doadores saudáveis para os camundongos deficientes em TFAM retardou modestamente a perda de peso, melhorou a força muscular e a constipação, aumentou o butirato fecal e ácidos graxos relacionados, e estendeu a longevidade máxima em cerca de 70% em comparação com camundongos que receberam microbiota doente. Uma abordagem mais direcionada usou um suplemento dietético, tributirina, que é convertido em butirato no intestino. Esse tratamento elevou o butirato fecal, retardou a perda de peso, fortaleceu os músculos, normalizou a glicemia de jejum e reduziu o dano renal. Notavelmente, estendeu a mediana de vida em aproximadamente um quarto e a longevidade máxima em mais de três quartos nos camundongos doentes.
Como uma molécula intestinal conversa com genes
Sabe‑se que o butirato é não só um combustível para células intestinais, mas também um sinal químico que pode influenciar quais genes são ligados ou desligados. Nos camundongos doentes, os pesquisadores encontraram que marcas químicas específicas em proteínas histonas—pequenos grupos acila adicionados à histona H3 em posições definidas—estavam muito reduzidas no tecido intestinal. Essas marcas ajudam a abrir o DNA ao redor de genes que preservam a barreira intestinal e lidam com o estresse. Depletar camundongos normais de sua microbiota com antibióticos produziu uma perda semelhante dessas marcas, ligando‑as a metabólitos microbianos. Alimentar os camundongos deficientes em TFAM com tributirina restaurou essas modificações de histonas e deslocou a atividade gênica intestinal de volta a um padrão mais saudável, incluindo genes envolvidos em junções entre células, na estrutura do tecido e nas respostas ao dano oxidativo.
Uma nova maneira de apoiar mitocôndrias em falha
De forma simples, este estudo sugere que quando as mitocôndrias falham, o intestino torna‑se permeável e seus micróbios amigos mudam, privando o corpo de butirato. Essa perda, por sua vez, enfraquece a barreira intestinal e perturba a regulação gênica, alimentando a doença sistêmica. Reconstruir a parceria entre hospedeiro e microbiota—seja transplantando uma comunidade microbiana mais saudável ou fornecendo um suplemento que libera butirato—pode aliviar muitos sintomas e estender a vida em camundongos com disfunção mitocondrial severa. Embora muito trabalho seja necessário antes que tais estratégias possam ser aplicadas em pessoas, os achados destacam o intestino e sua química microbiana como alavancas promissoras para tratar distúrbios enraizados em usinas celulares quebradas.
Citação: Gabandé-Rodríguez, E., Gómez de las Heras, M.M., Ramírez-Ruiz de Erenchun, P. et al. Butyrate extends health and lifespan in mice with mitochondrial deficiency. Nat Commun 17, 3909 (2026). https://doi.org/10.1038/s41467-026-70547-4
Palavras-chave: doença mitocondrial, microbioma intestinal, butirato, barreira intestinal, ácidos graxos de cadeia curta