Clear Sky Science · pl
Butyrate wydłuża zdrowie i długość życia myszy z niedoborem mitochondrialnym
Dlaczego jelita mają znaczenie dla zawodzących „silników” komórkowych
Choroby mitochondrialne to rzadkie zaburzenia, w których maleńkie „elektrownie” w komórkach zaczynają zawodzić, wywołując kaskadę problemów w wielu narządach i często skracając życie. Obecne terapie głównie łagodzą objawy. Badanie przeprowadzone na myszach odkrywa niespodziewanego sprzymierzeńca zamieszkującego jelito: niektóre bakterie produkujące kwas tłuszczowy zwany maślanem. Wyniki pokazują, że przywrócenie tej jelitowej cząsteczki może uszczelnić przeciekające jelito, złagodzić wiele chorób przypominających starzenie się i znacząco wydłużyć życie zwierząt z poważnymi defektami mitochondrialnymi.
Kiedy „elektrownie” komórek zawodzą
Naukowcy najpierw skonstruowali mysz, w której kluczowy regulator mitochondrialny, TFAM, można wyłączyć w całym organizmie w dorosłości. Gdy ten molekularny „strażnik” DNA mitochondrialnego został usunięty, zwierzęta szybko rozwinęły zespół przypominający przyspieszone starzenie: utratę tłuszczu i masy mięśniowej, osłabiony chwyt, zaburzenia kontroli glikemii, zwłóknienia płuc, nieprawidłowości serca i naczyń, niewydolność nerek, anemię oraz objawy degeneracji mózgu, w tym problemy z ruchem i zaburzenia zachowań budujących gniazdo. Wielu narządów dotyczyły stany zapalne i molekularne markery starzenia komórkowego, a myszy umierały przedwcześnie, co wskazuje, że szeroko rozpowszechnione uszkodzenie mitochondriów samo w sobie może prowadzić do wielonarządowego załamania.
Przeciekające jelito i zaburzona społeczność mikrobiologiczna
Ponieważ mitochondria są kluczowe dla zdrowia komórek jelitowych, zespół zbadał jelita zwierząt. Stwierdzono skrócone struktury jelitowe, mniej komórek dzielących się i cieńszą ochronną warstwę śluzu mimo prawidłowej liczby kubkowych komórek śluzowych. Więcej tych komórek było „uwięzionych”, zatrzymując śluz zamiast go wydzielać. Geny pomagające uszczelniać przestrzenie między komórkami i wytwarzać obronę antybakteryjną były wyciszone, a jelito stało się bardziej przepuszczalne: fluorescencyjny znacznik przeciekał do krwi, a we krwi gwałtownie wzrósł marker produktów bakteryjnych. Równocześnie zmienił się skład bakterii jelitowych. Mikrobi, które zwykle korzystają z węglowodanów diety i wytwarzają prozdrowotne krótkodługołańcuchowe kwasy tłuszczowe, zmniejszyły się, podczas gdy inne grupy się rozrosły. Analiza chemiczna potwierdziła, że poziomy wszystkich głównych krótkodługołańcuchowych kwasów tłuszczowych w kale oraz kilku we krwi były wyraźnie obniżone.
Wspólny wzorzec w innym modelu choroby mitochondrialnej
Aby sprawdzić, czy to zaburzenie jelit jest unikalne dla jednego triku genetycznego, naukowcy zwrócili się do drugiej linii myszy, która w miarę starzenia akumuluje losowe mutacje w DNA mitochondrialnym i rozwija przedwczesną multimorbidność. Te zwierzęta również miały bardziej przeciekającą barierę jelitową, obniżoną ekspresję genów połączeń międzykomórkowych i genów antybakteryjnych oraz prostszą, niezrównoważoną społeczność mikrobiologiczną jelit. W szczególności bakterie specjalizujące się w produkcji maślanu były zubożone, a poziomy maślanu w kale były selektywnie niższe, podczas gdy inne krótkodługołańcuchowe kwasy tłuszczowe były stosunkowo zachowane. To wskazywało, że utrata producentów maślanu jest wspólnym znakiem zaniku mitochondrialnego.
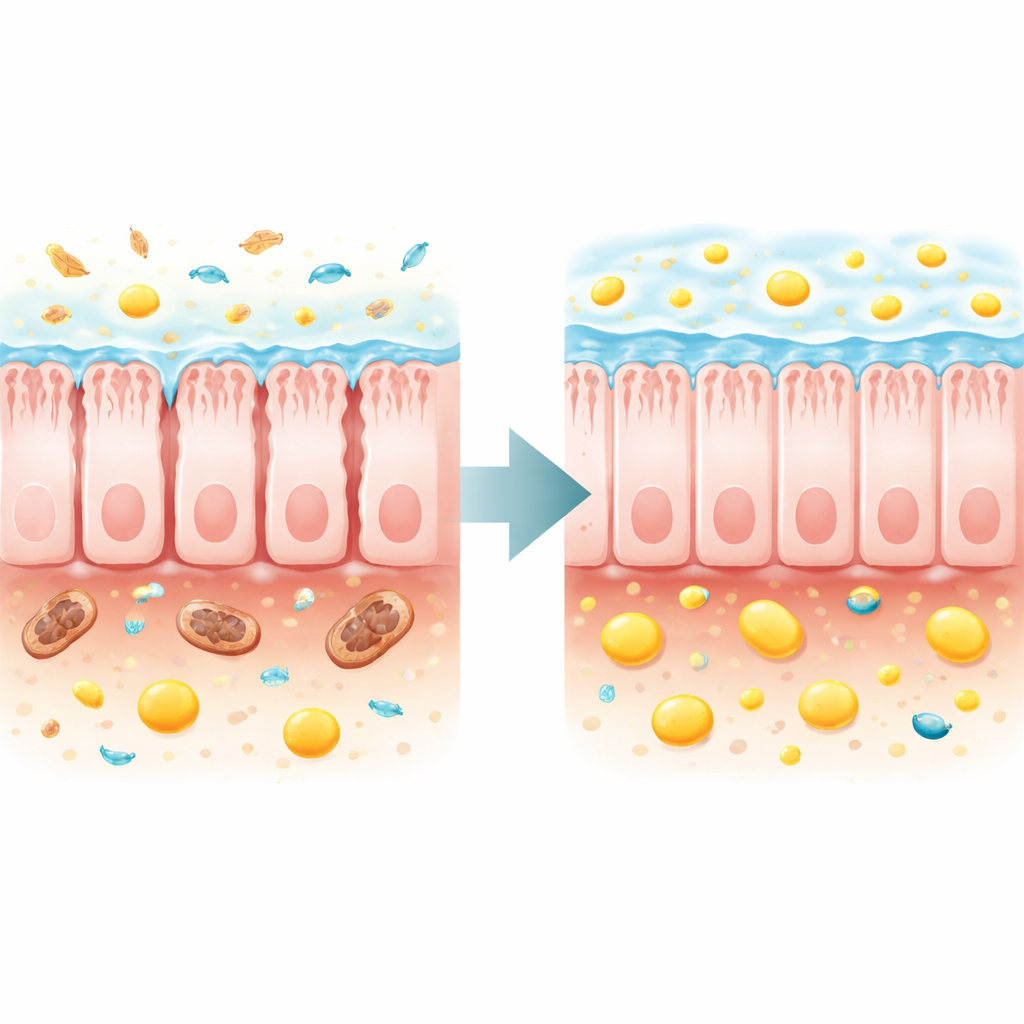
Odzyskiwanie utrzymanej pomocy mikrobiologicznej i odbudowa bariery
Autorzy zapytali następnie, czy naprawa ekosystemu jelitowego lub bezpośrednie przywrócenie maślanu może poprawić zdrowie całego organizmu. Przeszczep mikrobioty kałowej od zdrowych dawców do myszy pozbawionych TFAM łagodnie spowolnił utratę masy, poprawił siłę mięśni i zaparcia, podniósł poziomy maślanu i powiązanych kwasów tłuszczowych w kale oraz wydłużył maksymalną długość życia o około 70% w porównaniu z myszami, które otrzymały chorą mikrobiotę. Bardziej ukierunkowane podejście użyło suplementu diety, tributyryny, który w jelicie przekształca się w maślan. To leczenie zwiększyło maślan w kale, opóźniło wyniszczenie, wzmocniło mięśnie, znormalizowało poziom glukozy na czczo i zmniejszyło uszkodzenie nerek. Co godne uwagi, wydłużyło medianę przeżycia o mniej więcej jedną czwartą, a maksymalną długość życia chorujących myszy o ponad trzy czwarte.
Jak jelitowa cząsteczka komunikuje się z genami
Maślan jest znany nie tylko jako paliwo dla komórek jelitowych, lecz także jako sygnał chemiczny, który może wpływać na to, które geny są włączane lub wyłączane. U chorych myszy badacze stwierdzili, że specyficzne chemiczne znaczniki na białkach histonowych — małe grupy acylowe dodawane do histonu H3 w określonych pozycjach — były znacznie zmniejszone w tkance jelitowej. Te znaczniki pomagają otwierać DNA wokół genów, które utrzymują barierę jelitową i radzą sobie ze stresem. Odtworzenie mikrobioty w normalnych myszach za pomocą antybiotyków spowodowało podobną utratę tych znaków, łącząc je z metabolitami mikrobiologicznymi. Karmienie myszy pozbawionych TFAM tributyryną przywróciło te modyfikacje histonów i przesunęło aktywność genową w jelicie z powrotem w kierunku zdrowszego wzorca, w tym genów zaangażowanych w połączenia międzykomórkowe, rusztowanie tkanki i reakcje na uszkodzenia oksydacyjne.
Nowy sposób wsparcia zawodzących mitochondriów
Prosto ujmując, badanie sugeruje, że gdy mitochondria zawodzą, jelito staje się przeciekające, a jego przyjazne mikroby ulegają zmianie, pozbawiając organizm maślanu. Ta utrata z kolei osłabia barierę jelitową i zaburza regulację genów, napędzając chorobę ogólnoustrojową. Odbudowa partnerstwa między gospodarzem a mikrobiotą — przez przeszczep zdrowszej wspólnoty mikroorganizmów lub podanie suplementu uwalniającego maślan — może złagodzić wiele objawów i wydłużyć życie myszy z ciężką dysfunkcją mitochondrialną. Choć potrzeba jeszcze wiele pracy, zanim takie strategie będzie można zastosować u ludzi, wyniki podkreślają jelito i jego mikrobiologiczną chemię jako obiecujące dźwignie do leczenia zaburzeń związanych z uszkodzonymi „elektrowniami” komórkowymi.
Cytowanie: Gabandé-Rodríguez, E., Gómez de las Heras, M.M., Ramírez-Ruiz de Erenchun, P. et al. Butyrate extends health and lifespan in mice with mitochondrial deficiency. Nat Commun 17, 3909 (2026). https://doi.org/10.1038/s41467-026-70547-4
Słowa kluczowe: choroba mitochondrialna, mikrobiom jelitowy, maślan (butyrat), bariera jelitowa, krótkodługołańcuchowe kwasy tłuszczowe