Clear Sky Science · ar
البيوتيرات يطيل الصحة والعمر في الفئران ذات العجز الميتوكوندري
لماذا يهمّ الأمعاء في فشل محركات الخلايا
الأمراض الميتوكوندرية هي اضطرابات نادرة تتراجع فيها «محطات الطاقة» الصغيرة داخل خلايانا، مسببة سلسلة من المشاكل عبر عدة أعضاء وغالبًا ما تقصر العمر. العلاجات الحالية تقتصر في الغالب على إدارة الأعراض. تكشف هذه الدراسة على الفئران عن حليف غير متوقع يعيش في الأمعاء: بكتيريا معينة تُنتج حمضًا دهنيًا يسمى البيوتيرات. تُظهر النتائج أن استعادة هذه المادة المولدة في الأمعاء يمكن أن تدعم أمعاء متسربة، وتخفف من أمراض شبيهة بالشيخوخة، وتطيل إلى حد كبير عمر الحيوانات ذات العيوب الميتوكوندرية الشديدة.
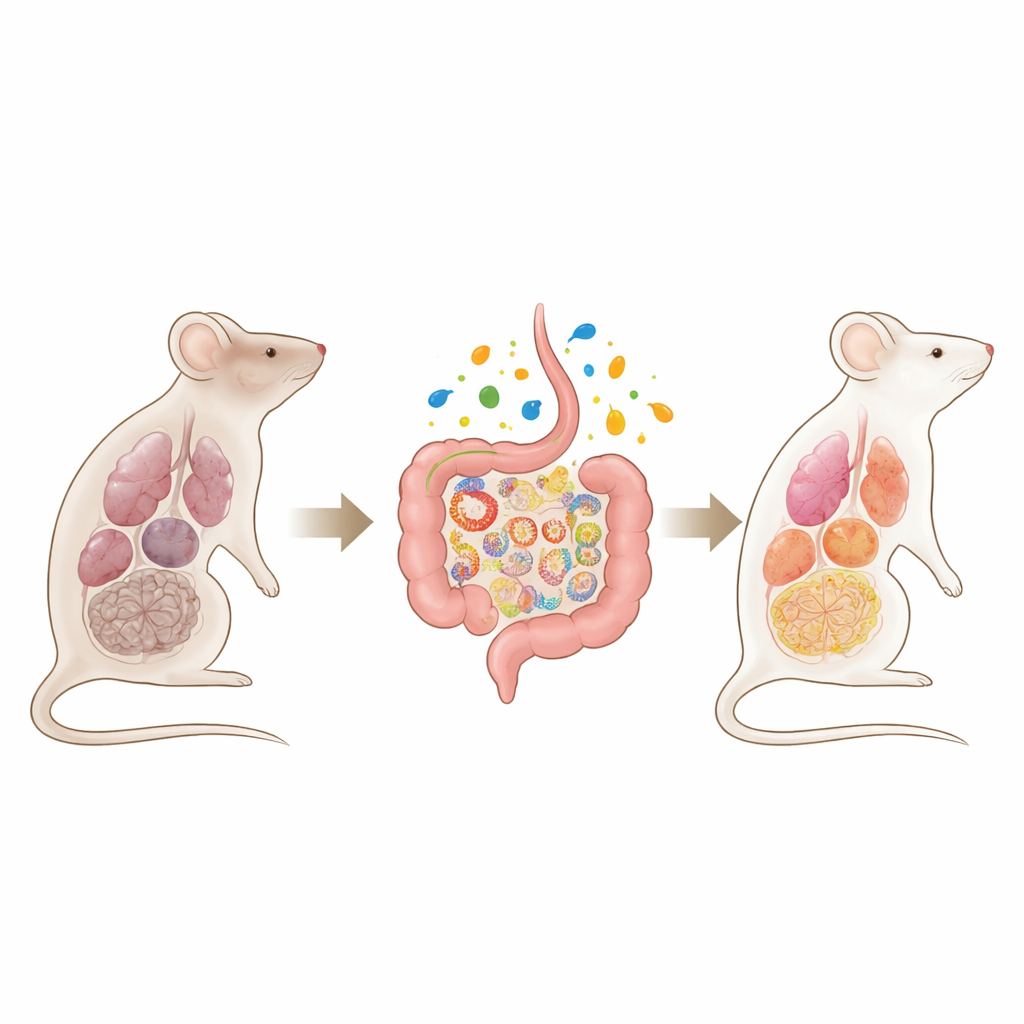
عندما تنهار محطات طاقة الخلايا
أولاً، مهندس الباحثون فأرًا يمكن إيقاف مدى تنظيم رئيسي للميتوكوندريا، TFAM، في جميع أنحاء الجسم في مرحلة البلوغ. بعد إزالة هذا «الحارس» الجزيئي لحمض الميتوكوندريا النووي، طورت الحيوانات بسرعة متلازمة تشبه الشيخوخة المسرّعة: فقدان الدهون والعضلات، ضعف القبضة، اضطراب في التحكم بمستويات السكر في الدم، تندّب الرئتين، شذوذات في القلب والأوعية، فشل كلوي، فقر دم، وعلامات لانحطاط الدماغ بما في ذلك مشاكل في الحركة واضطراب في بناء الأعشاش. أظهرت العديد من الأعضاء التهابًا وعلامات جزيئية للشيخوخة الخلوية، وماتت الفئران قبل أوانها، مما يدل على أن فشل الميتوكوندريا الواسع وحده يمكن أن يؤدي إلى تدهور متعدد الأعضاء.
أمعاء متسربة ومجتمع ميكروبي مضطرب
لأن الميتوكوندريا حاسمة لصحة خلايا الأمعاء، فحص الفريق أمعاء الحيوانات. وجدوا تراكيب معوية أقصر، وخلايا متقسمة أقل، وطبقة مخاطية واقية أنحف على الرغم من أعداد طبيعية من خلايا الكأس المفرزة للمخاط. وكان عدد أكبر من هذه الخلايا «عالقًا» محتفظًا بالمخاط بدل إفرازه. تم كبح التعبير عن الجينات التي تساعد على سد الفواصل بين الخلايا وإنتاج الدفاعات المضادة للميكروبات، وأصبحت الأمعاء أكثر منفاذية: تسرّب متتبِّع فلوري إلى الدم، وارتفع مؤشر في الدم لمنتجات بكتيرية بشكل حاد. في الوقت نفسه تغيّر تركيب بكتيريا الأمعاء؛ انخفضت الميكروبات التي تزدهر عادة على الكربوهيدرات الغذائية وتنتج أحماضًا دهنية قصيرة السلسلة المفيدة للصحة، بينما توسعت مجموعات أخرى. وأكد التحليل الكيميائي أن مستويات كل الأحماض الدهنية قصيرة السلسلة الرئيسية في البراز، وبعضها في الدم، تراجعت بشكل ملحوظ.
نمط شائع في نموذج ميتوكوندري آخر
للتأكد مما إذا كان هذا الاضطراب المعوي فريدًا لحيلة جينية واحدة، لجأ العلماء إلى سلالة فأرية ثانية تتراكم فيها طفرات عشوائية في حمض الميتوكوندريا النووي مع التقدّم في العمر وتطوّر مرض متعدد ومبكر. كانت هذه الحيوانات أيضًا ذات حاجز معوي أكثر تسربًا، وتعبير مخفض لجينات الوصلات والجينات المضادة للميكروبات، ومجتمع ميكروبي أبسط وغير متوازن في الأمعاء. على وجه الخصوص، نُقصت البكتيريا المتخصّصة في إنتاج البيوتيرات، وكانت مستويات البيوتيرات البرازية أقل بشكل انتقائي، بينما بقيت الأحماض الدهنية قصيرة السلسلة الأخرى محمية نسبيًا. أشارت هذه النتائج إلى أن فقدان الشركاء المنتجين للبيوتيرات يعد سمة مشتركة لتدهور الميتوكوندريا.
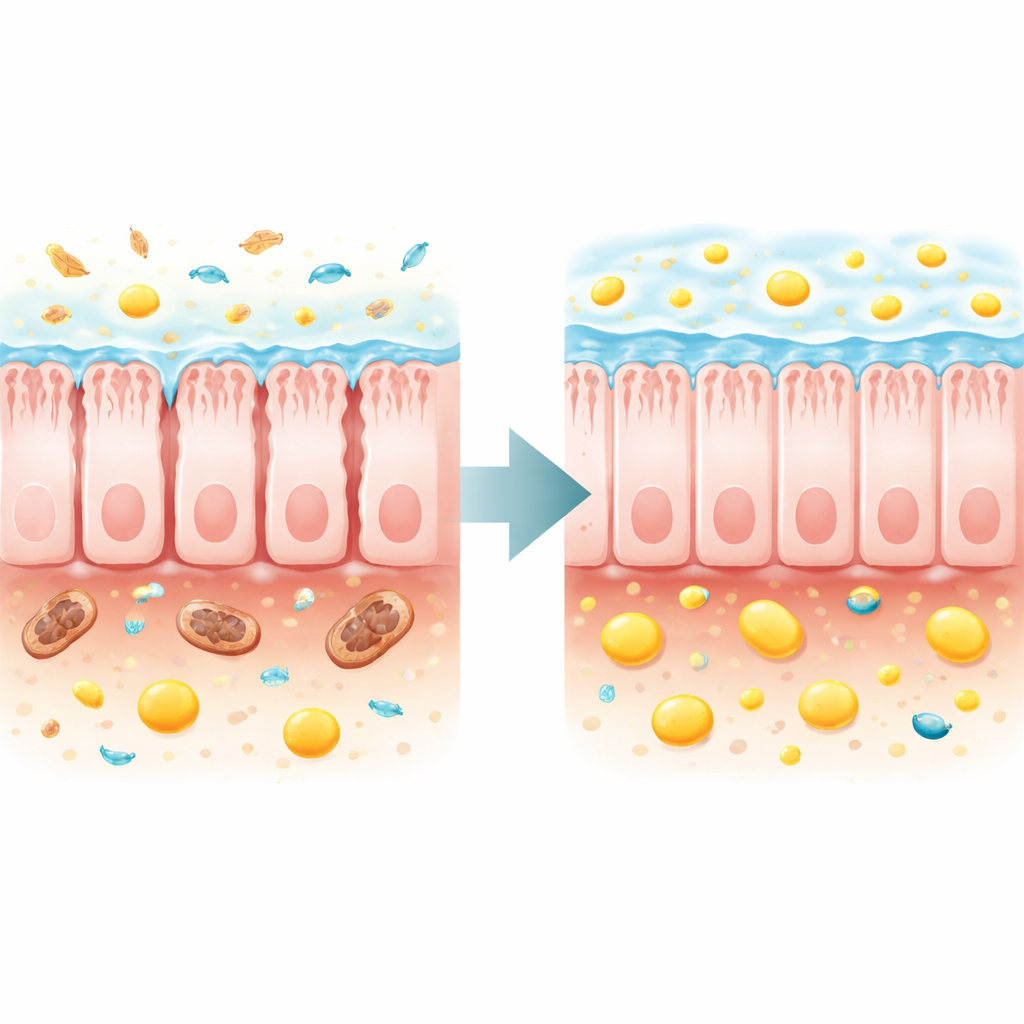
استبدال المساعدة الميكروبية المفقودة وإعادة بناء الحاجز
سأل المؤلفون بعد ذلك ما إذا كان إصلاح نظام الأمعاء البيئي أو استعادة البيوتيرات مباشرة يمكن أن يحسّن الصحة العامة. نقل ميكروبات برازية من متبرعين أصحاء إلى الفئران قليلة TFAM أبطأ بشكل متواضع فقدان الوزن، وحسّن قوة العضلات والإمساك، وزاد البيوتيرات البرازي والدهون المشتقة ذات الصلة، ووسع أقصى فترة حياة بنحو 70% مقارنة بالفئران التي تلقت ميكروبيوتا مريضة. نهج أكثر تركيزًا استخدم مكملاً غذائيًا، التريبيوتيرين، الذي يتحول إلى بيوترات في الأمعاء. عزز هذا العلاج البيوتيرات البرازي، وأخر الهزال، وقوّى العضلات، ونَوَّمَ سكر الدم أثناء الصيام إلى مستويات طبيعية، وقلّل من تلف الكلى. واللافت أنه مدد متوسط العمر بنحو ربع ومدى الحياة الأقصى بأكثر من ثلاثة أرباع في الفئران المريضة.
كيف يتواصل جزيء معوي مع الجينات
من المعروف أن البيوتيرات ليس فقط وقودًا لخلايا الأمعاء بل إشارة كيميائية يمكن أن تؤثر في تشغيل أو إيقاف جينات معينة. في الفئران المريضة، وجد الباحثون أن علامات كيميائية محددة على بروتينات الهيستون — مجموعات أسيليّة صغيرة مضافة إلى الهيستون H3 في مواقع معينة — انخفضت بشكل كبير في نسيج الأمعاء. تساعد هذه العلامات على فتح الحمض النووي حول الجينات التي تحافظ على حاجز الأمعاء وتتعامل مع الإجهاد. كما أدى استنزاف الميكروبيوتا في الفئران السليمة بالمضادات الحيوية إلى فقدان مماثل لهذه العلامات، رابطًا إياها بميثابوليتات الميكروبات. إطعام الفئران ناقصة TFAM بالتريبيوتيرين أعاد هذه التعديلات على الهيستونات وحوّل نشاط الجينات المعوي نحو نمط أكثر صحة، بما في ذلك جينات مشاركة في الوصلات بين الخلايا، والهيكل الداعم للأنسجة، والاستجابات للضرر التأكسدي.
طريقة جديدة لدعم الميتوكوندريا المتداعية
بعبارة مبسطة، تقترح هذه الدراسة أنه عندما تتعثر الميتوكوندريا، تصبح الأمعاء متسربة وتتغير ميكروباتها الصديقة، مما يحرم الجسم من البيوتيرات. وهذا الفقدان بدوره يُضعف حاجز الأمعاء ويشوش تنظيم الجينات، مما يغذي المرض الجهازي. إعادة بناء الشراكة بين المضيف والميكروبيوتا — إما عن طريق زراعة مجتمع ميكروبي أكثر صحة أو بتوفير مكمّل يطلق البيوتيرات — يمكن أن يخفف العديد من الأعراض ويطيل العمر في الفئران ذات الخلل الميتوكوندري الشديد. ومع أن هناك حاجة إلى مزيد من العمل قبل تطبيق مثل هذه الاستراتيجيات على البشر، تبرز النتائج الأمعاء وكيمياء الميكروبات فيها كمقابض واعدة جديدة لعلاج اضطرابات تنبع من محطات طاقة خلوية معطلة.
الاستشهاد: Gabandé-Rodríguez, E., Gómez de las Heras, M.M., Ramírez-Ruiz de Erenchun, P. et al. Butyrate extends health and lifespan in mice with mitochondrial deficiency. Nat Commun 17, 3909 (2026). https://doi.org/10.1038/s41467-026-70547-4
الكلمات المفتاحية: مرض ميتوكوندري, الميكروبيوم المعوي, البيوتيرات, الحاجز المعوي, الأحماض الدهنية قصيرة السلسلة