Clear Sky Science · fr
Le butyrate prolonge la santé et la durée de vie chez la souris atteinte d’un défaut mitochondrial
Pourquoi l’intestin compte pour des moteurs cellulaires défaillants
Les maladies mitochondriales sont des troubles rares dans lesquels les minuscules « centrales électriques » à l’intérieur de nos cellules commencent à tomber en panne, provoquant une cascade de problèmes dans de nombreux organes et raccourcissant souvent l’espérance de vie. Les traitements actuels se limitent essentiellement à la prise en charge des symptômes. Cette étude chez la souris met au jour un allié inattendu vivant dans l’intestin : certaines bactéries qui produisent un acide gras appelé butyrate. Les travaux montrent que restaurer cette molécule d’origine intestinale permet de colmater un intestin poreux, d’atténuer plusieurs maladies d’allure liée à l’âge et d’allonger significativement la durée de vie chez des animaux présentant de graves défauts mitochondriaux.
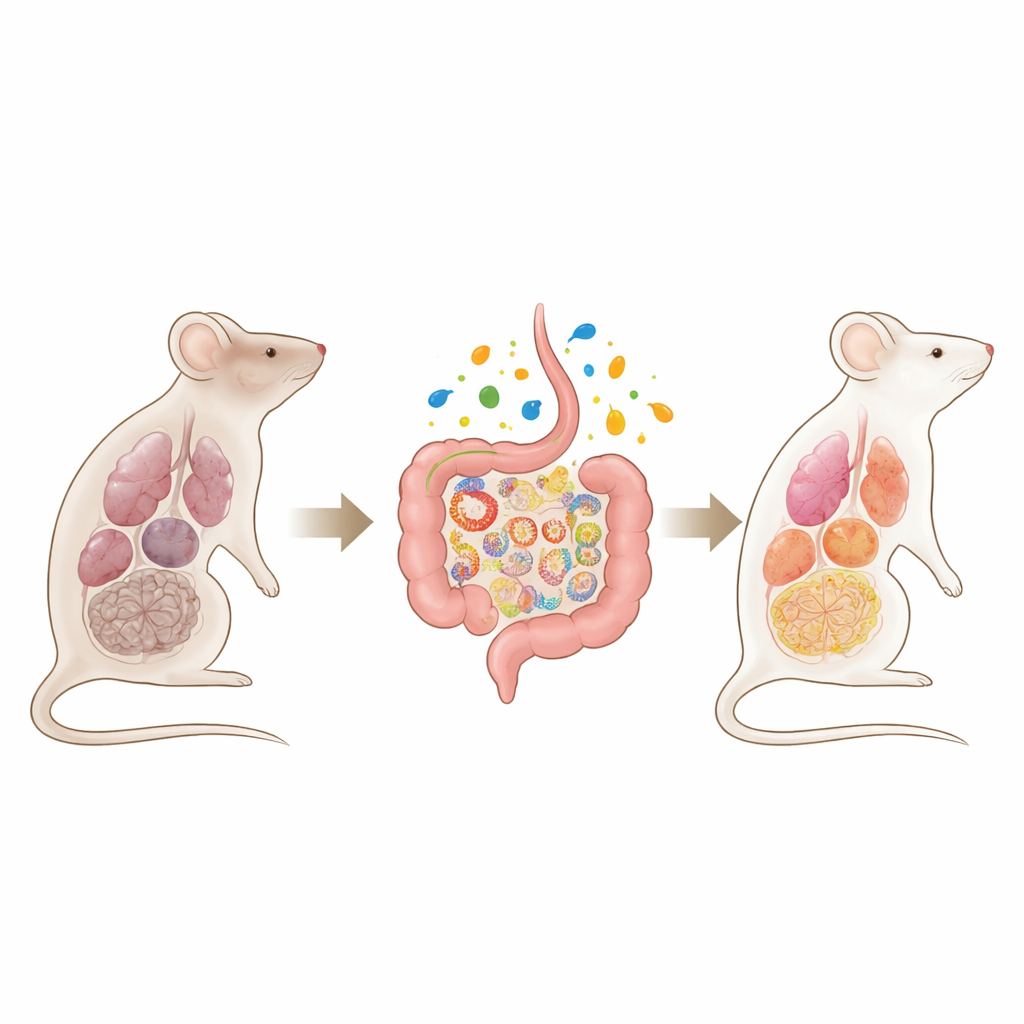
Quand les centrales cellulaires se détériorent
Les chercheurs ont d’abord conçu une souris dans laquelle un régulateur mitochondrial clé, TFAM, peut être éteint dans tout l’organisme à l’âge adulte. Une fois ce « gardien » moléculaire de l’ADN mitochondrial supprimé, les animaux ont rapidement développé un syndrome ressemblant à un vieillissement accéléré : perte de masse grasse et musculaire, préhension faible, mauvais contrôle de la glycémie, fibrose pulmonaire, anomalies cardiaques et vasculaires, insuffisance rénale, anémie et signes de dégénérescence cérébrale, y compris troubles moteurs et altération du comportement de nidification. De nombreux organes présentaient une inflammation et des marqueurs moléculaires de sénescence cellulaire, et les souris mouraient prématurément, ce qui indique qu’une défaillance mitochondriale généralisée peut à elle seule entraîner une dégradation multi‑organes.
Un intestin poreux et une communauté microbienne perturbée
Parce que les mitochondries sont cruciales pour la santé des cellules intestinales, l’équipe a examiné l’intestin des animaux. Ils ont observé des structures intestinales raccourcies, moins de cellules en division et une couche de mucus protectrice plus fine malgré un nombre normal de cellules caliciformes productrices de mucus. Un plus grand nombre de ces cellules restaient « collées » avec du mucus au lieu de le libérer. Les gènes qui aident à refermer les espaces entre les cellules et à produire des défenses antimicrobiennes étaient réprimés, et l’intestin devenait plus perméable : un traceur fluorescent fuyait dans le sang et un marqueur sanguin de produits bactériens augmentait nettement. Parallèlement, la composition des bactéries intestinales a changé. Les microbes qui habituellement prospèrent grâce aux glucides alimentaires et produisent des acides gras à chaîne courte bénéfiques ont diminué, tandis que d’autres groupes se sont étendus. L’analyse chimique a confirmé que les niveaux de tous les principaux acides gras à chaîne courte dans les fèces, et plusieurs dans le sang, étaient fortement réduits.
Un schéma commun dans un autre modèle de maladie mitochondriale
Pour vérifier si cette perturbation intestinale était spécifique à une astuce génétique, les scientifiques se sont tournés vers une seconde souche de souris qui accumule des mutations aléatoires de l’ADN mitochondrial en vieillissant et développe une multimorbidité prématurée. Ces animaux présentaient également une barrière intestinale plus perméable, une expression réduite des gènes de jonction et antimicrobiens, et une communauté microbienne intestinale plus simple et déséquilibrée. En particulier, les bactéries spécialisées dans la production de butyrate étaient appauvries, et les niveaux de butyrate fécal étaient sélectivement plus bas, tandis que d’autres acides gras à chaîne courte étaient relativement préservés. Cela indiquait que la perte de partenaires producteurs de butyrate est un signe commun du déclin mitochondrial.
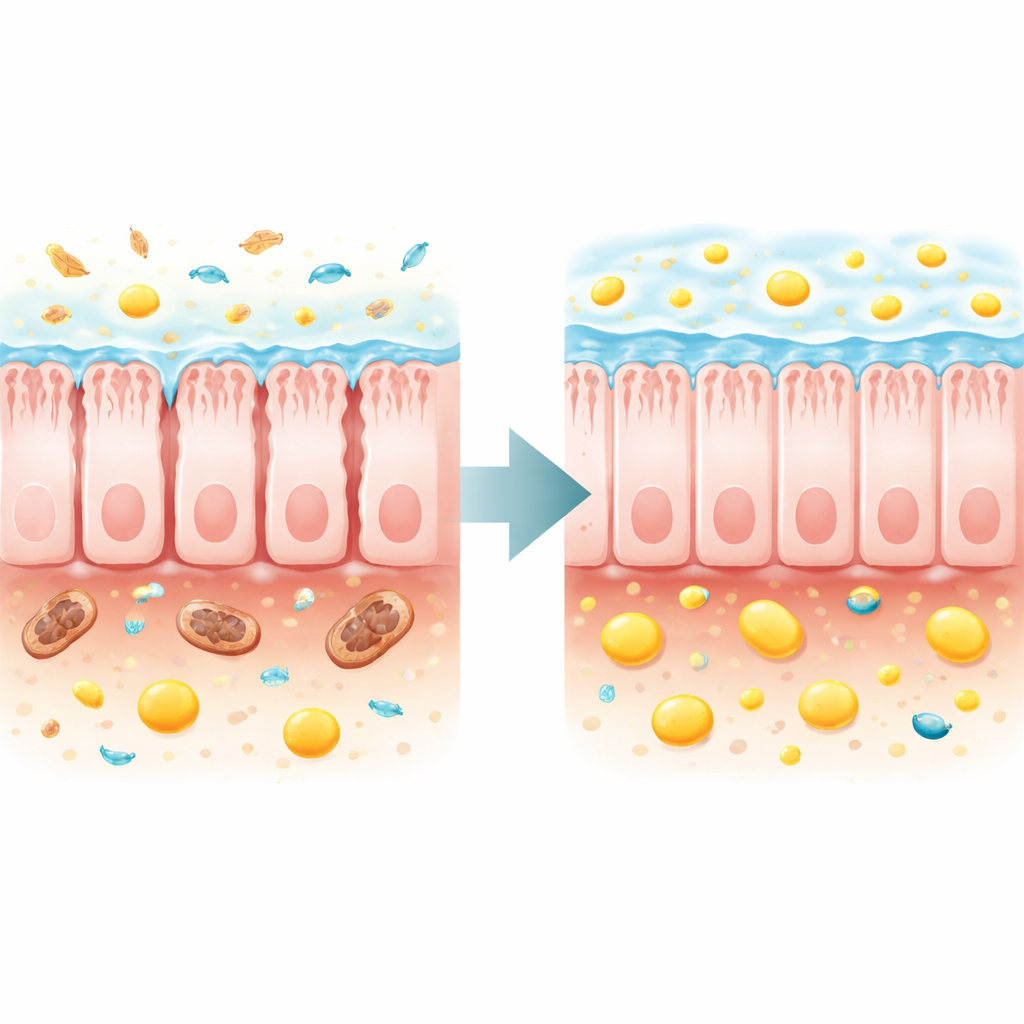
Remplacer l’aide microbienne perdue et reconstruire la barrière
Les auteurs se sont alors demandé si réparer l’écosystème intestinal ou restaurer directement le butyrate pouvait améliorer la santé globale. Le transfert de microbiote fécal de donneurs sains vers les souris déficientes en TFAM a modestement ralenti la perte de poids, amélioré la force musculaire et la constipation, augmenté le butyrate fécal et les acides gras voisins, et prolongé la durée de vie maximale d’environ 70 % comparé aux souris ayant reçu un microbiote malade. Une approche plus ciblée a utilisé un complément alimentaire, le tributyrine, qui est converti en butyrate dans l’intestin. Ce traitement a augmenté le butyrate fécal, retardé l’amaigrissement, renforcé les muscles, normalisé la glycémie à jeun et réduit les lésions rénales. Fait remarquable, il a prolongé la durée de vie médiane d’environ un quart et la durée de vie maximale de plus des trois quarts chez les souris malades.
Comment une molécule intestinale dialogue avec les gènes
Le butyrate est connu non seulement comme carburant pour les cellules intestinales, mais aussi comme signal chimique capable d’influencer l’activation ou la répression de gènes. Chez les souris malades, les chercheurs ont constaté que des marques chimiques spécifiques sur les protéines histones — de petits groupes acyles ajoutés à l’histone H3 à des positions définies — étaient fortement réduites dans le tissu intestinal. Ces marques aident à ouvrir l’ADN autour des gènes qui préservent la barrière intestinale et gèrent le stress. L’appauvrissement du microbiote chez des souris normales par des antibiotiques produisait une perte similaire de ces marques, les reliant aux métabolites microbien. L’alimentation des souris déficientes en TFAM avec de la tributyrine a rétabli ces modifications d’histones et réorienté l’activité génique intestinale vers un profil plus sain, y compris des gènes impliqués dans les jonctions intercellulaires, l’ossature du tissu et les réponses aux dommages oxydatifs.
Une nouvelle manière de soutenir des mitochondries défaillantes
En termes simples, cette étude suggère que lorsque les mitochondries faiblissent, l’intestin devient poreux et ses microbes amis changent, privant l’organisme de butyrate. Cette perte, à son tour, affaiblit la barrière intestinale et perturbe la régulation génétique, alimentant une maladie systémique. Reconstruire le partenariat entre l’hôte et le microbiote — soit en transplantant une communauté microbienne plus saine, soit en apportant un supplément libérant du butyrate — peut atténuer de nombreux symptômes et prolonger la vie chez des souris souffrant d’une grave dysfonction mitochondriale. Bien que de nombreuses études soient nécessaires avant d’envisager ces stratégies chez l’homme, les résultats mettent en lumière l’intestin et sa chimie microbienne comme de nouveaux leviers prometteurs pour traiter des troubles issus de centrales cellulaires défaillantes.
Citation: Gabandé-Rodríguez, E., Gómez de las Heras, M.M., Ramírez-Ruiz de Erenchun, P. et al. Butyrate extends health and lifespan in mice with mitochondrial deficiency. Nat Commun 17, 3909 (2026). https://doi.org/10.1038/s41467-026-70547-4
Mots-clés: maladie mitochondriale, microbiote intestinal, butyrate, barrière intestinale, acides gras à chaîne courte