Clear Sky Science · zh
DPEP2 通过改变巨噬细胞代谢抑制脓毒症中的过度炎症反应
为何要平息机体的过度反应
脓毒症是一种危及生命的状态,机体免疫系统在试图对抗感染时失控,开始损伤自身器官。尽管有抗生素和现代重症监护,许多人仍然死亡,因为这种失控的炎症难以在不削弱关键防御的情况下被控制。本研究发现了前线免疫细胞中的一种天然“刹车”分子,并展示了通过基因疗法增强其功能如何在不损害抗菌能力的前提下减轻有害炎症。
位于抗感染细胞内的隐形刹车
研究人员聚焦于单核细胞和巨噬细胞——在血液中循环并巡逻各器官、在微生物入侵时发出警报的免疫细胞。通过对脓毒症早期患者血液进行先进的单细胞和整体 RNA 测序,他们逐细胞绘制了基因活动图谱。一个名为 DPEP2 的基因脱颖而出:在健康的单核细胞和巨噬细胞中强烈表达,但在脓毒症患者中持续下降。较低的 DPEP2 水平与更严重的器官功能衰竭评分、血中炎症分子水平升高和更高的死亡风险密切相关。存活患者的 DPEP2 阳性单核细胞数量比未存活者多,这表明该分子有助于遏制免疫系统最危险的冲动。
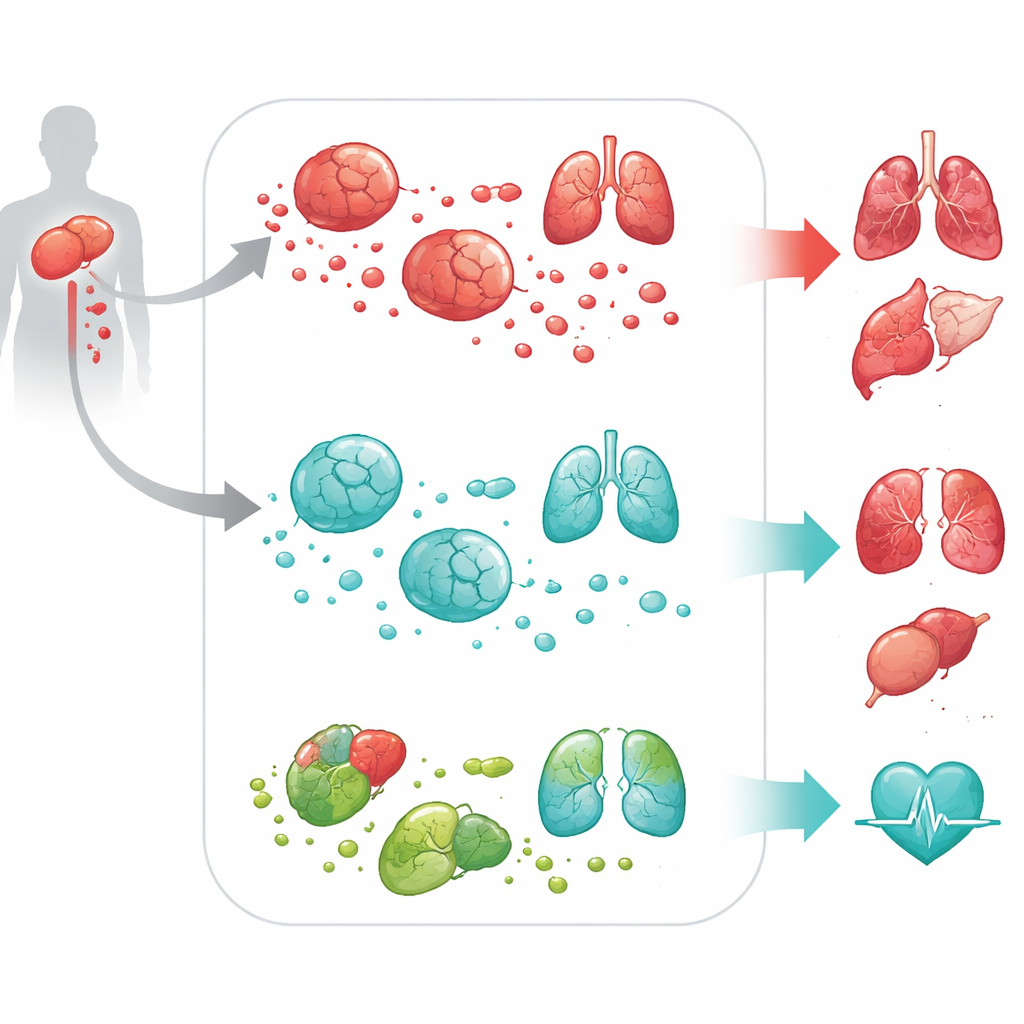
从基因信号到全身损伤
为检验 DPEP2 是旁观者还是积极的保护因子,团队转向细胞与动物模型。在体外培养的鼠类和人源巨噬细胞中,关闭 DPEP2 会导致这些细胞在受细菌成分刺激时分泌更多炎症细胞因子。在采用标准手术诱导的脓毒症小鼠模型中,缺失 DPEP2 的动物——无论是全身缺失还是特异性在巨噬细胞中缺失——情况都明显更差。它们血液中炎症分子水平更高,肺、肝、肾、心和脑损伤更严重,死亡率显著上升。这些实验表明 DPEP2 不只是疾病严重性的标记,而是真正对抗失控炎症的有效防御因子。
一种脂类加工酶如何平息炎症
DPEP2 通过重塑巨噬细胞处理某些作为强效局部激素的脂类分子的方式发挥作用。具体而言,它有助于将一种名为白三烯 D4 的化合物分解为炎症性较弱的产物,失去 DPEP2 会导致白三烯 D4 堆积。该堆积反过来促使细胞内更多脂类前体朝向合成前列腺素 E2(另一种强烈的炎症驱动因子)的方向流动。这些脂质共同作用在细胞内的一个重要开关 NF-κB 上,NF-κB 控制着许多炎症细胞因子的基因。当 DPEP2 缺失或含量偏低时,这个以脂类为基础的信号网络失去制约,激活 NF-κB,使巨噬细胞向体内大量释放有害的炎性因子。
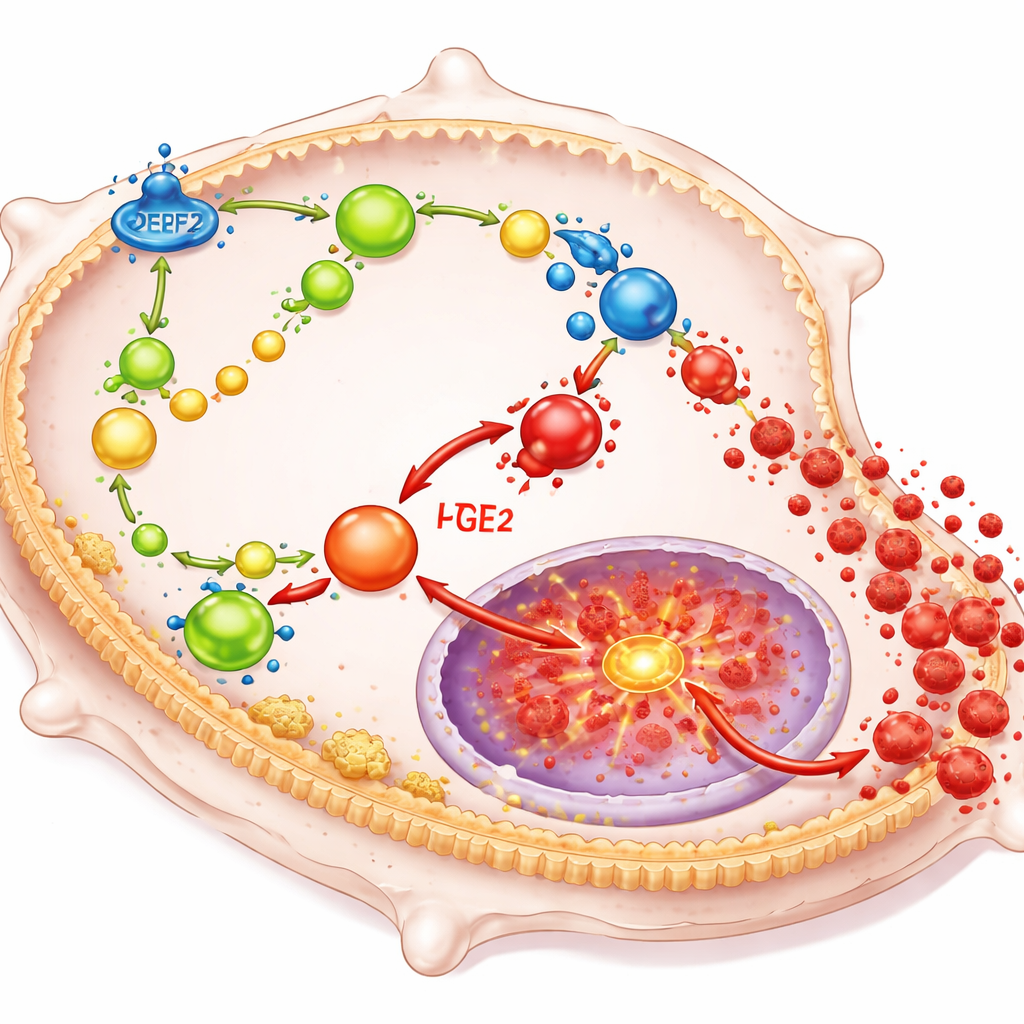
用 mRNA 重写免疫细胞
有了这一机制性的认识,科学家们探讨恢复 DPEP2 是否能帮助挽救脓毒症动物。他们设计了脂质纳米颗粒——类似于 mRNA 疫苗中使用的微小脂质囊泡——将 Dpep2 mRNA 特异性递送到单核细胞和巨噬细胞。静脉注射后,这些颗粒在靶细胞中短暂提高了 DPEP2 水平。在接受 Dpep2 载荷纳米颗粒治疗的脓毒症小鼠中,炎症标志物下降,肺和其它器官损伤减轻,存活率较对照动物提高。重要的是,该治疗在短期内无明显毒性,并在约一天半后消退,这与脓毒症死亡最常发生的关键早期时间窗相吻合。
对未来脓毒症护理的意义
这项工作揭示了 DPEP2 作为一种关键的天然保护机制,防止抗感染细胞将机体推向致命的自体损伤。研究显示血液中单核细胞的 DPEP2 水平反映疾病严重性,提示它可能作为识别高风险患者的有用血液生物标志物。更为引人注目的是,Dpep2 mRNA—纳米颗粒疗法在小鼠中的成功指向了一类新的精确治疗策略:与其广泛抑制免疫,不如在未来通过微调免疫细胞内特定的代谢开关来冷却脓毒症中的炎症风暴,同时保留机体的防御能力。
引用: Luo, W., Xu, W., Yin, Q. et al. DPEP2 suppresses hyperinflammation via metabolic reprogramming of macrophages in sepsis. Nat Commun 17, 3710 (2026). https://doi.org/10.1038/s41467-026-70466-4
关键词: 脓毒症, 巨噬细胞, 免疫代谢, 脂质介质, mRNA 治疗