Clear Sky Science · pt
DPEP2 suprime a hiperinflação via reprogramação metabólica de macrófagos na sepse
Por que acalmar a reação exagerada do corpo importa
A sepse é uma condição com risco de vida na qual o sistema imunológico, ao tentar combater uma infecção, entra em hiperatividade e começa a danificar os próprios órgãos. Apesar dos antibióticos e dos cuidados intensivos modernos, muitas pessoas ainda morrem porque essa inflação descontrolada é difícil de conter sem comprometer defesas vitais. Este estudo revela uma molécula "freio" natural em células imunológicas de linha de frente e mostra como potencializá-la com uma terapia genética pode silenciar a inflamação prejudicial ao mesmo tempo em que preserva a capacidade de combater micróbios.
Um freio oculto dentro das células que combatem infecções
Os pesquisadores concentraram-se em monócitos e macrófagos, células imunes que circulam no sangue e patrulham os órgãos, dando o alarme quando micróbios invadem. Utilizando técnicas avançadas de sequenciamento de RNA em células únicas e em massa em sangue de pacientes na fase inicial da sepse, mapearam a atividade gênica célula a célula. Um gene, chamado DPEP2, destacou-se: era fortemente ativo em monócitos e macrófagos saudáveis, mas consistentemente reduzido em pacientes com sepse. Níveis mais baixos de DPEP2 estavam fortemente associados a piores escores de falência orgânica, níveis mais altos de moléculas inflamatórias no sangue e maior risco de morte. Pacientes que sobreviveram apresentavam mais monócitos positivos para DPEP2 do que aqueles que não sobreviveram, sugerindo que essa molécula ajuda a conter os impulsos mais perigosos do sistema imunológico.
Do sinal gênico ao dano em todo o corpo
Para testar se DPEP2 era meramente um espectador ou um protetor ativo, a equipe recorreu a modelos celulares e animais. Em macrófagos de camundongo e humanos cultivados em laboratório, silenciar DPEP2 fez com que essas células produzissem muito mais citocinas inflamatórias quando estimuladas com componentes bacterianos. Em camundongos submetidos a um modelo padrão de sepse baseado em cirurgia, animais sem DPEP2 – tanto de forma sistêmica quanto especificamente nos macrófagos – evoluíram muito pior. Eles apresentaram níveis mais altos de moléculas inflamatórias na corrente sanguínea, lesões mais graves no pulmão, fígado, rim, coração e cérebro, e taxas de mortalidade significativamente maiores. Esses experimentos mostraram que DPEP2 não é apenas um marcador de gravidade da doença, mas um defensor ativo contra a inflamação avassaladora.
Como uma enzima de processamento de lipídios controla o fogo
DPEP2 atua remodelando a forma como os macrófagos processam certos lipídios que funcionam como potentes hormônios locais. Em particular, ele ajuda a degradar um composto chamado leucotrieno D4 em um produto menos inflamatório, e sua ausência causa acúmulo de leucotrieno D4. Esse acúmulo, por sua vez, direciona mais blocos de construção lipídicos da célula para a produção de prostaglandina E2, outro potente indutor de inflamação. Juntos, esses lipídios alimentam um grande interruptor intracelular conhecido como NF-κB, que controla genes de muitas citocinas inflamatórias. Quando DPEP2 está ausente ou em níveis baixos, essa rede de sinais lipídicos fica descontrolada, ativando o NF-κB e fazendo com que os macrófagos inundem o organismo com fatores inflamatórios danosos.
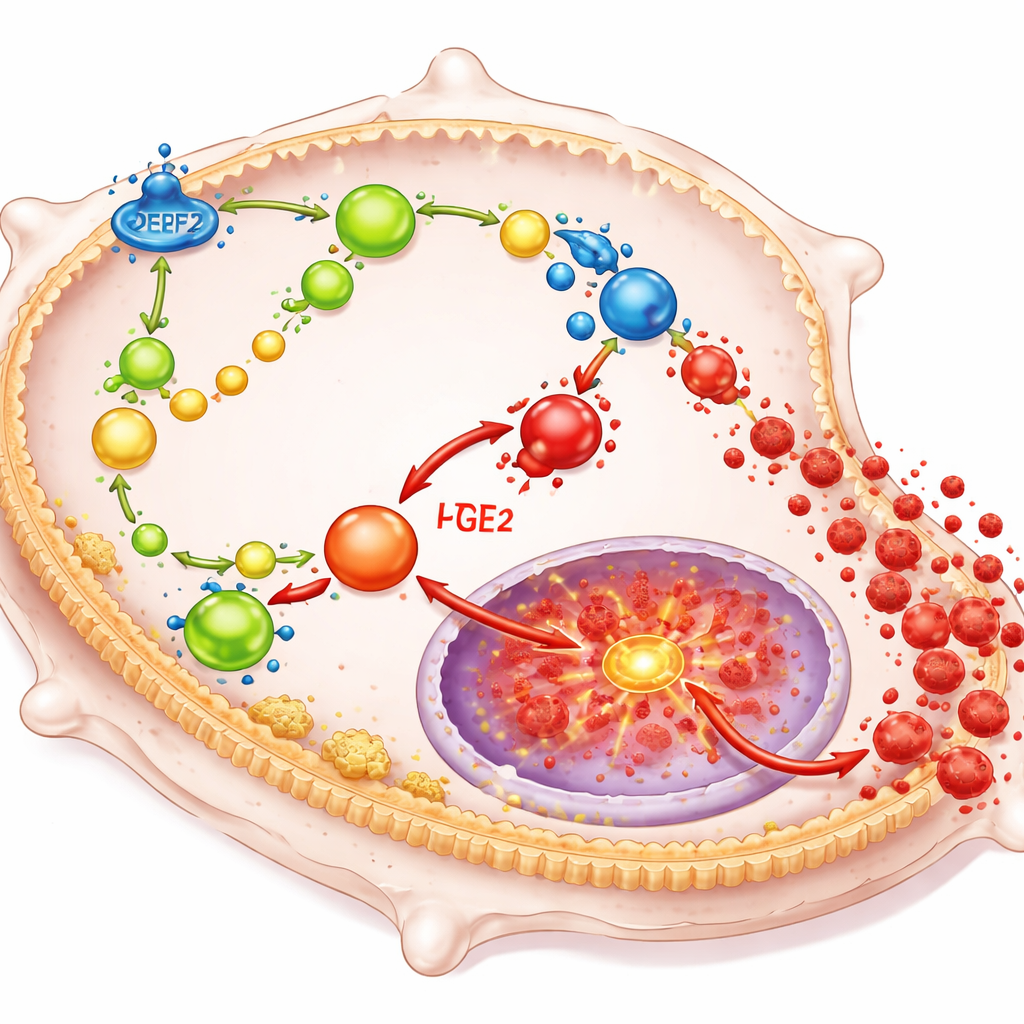
Reescrevendo células imunes com mRNA
Munidos dessa compreensão mecânica, os cientistas perguntaram se restaurar DPEP2 poderia ajudar a resgatar animais da sepse. Eles projetaram nanopartículas lipídicas — minúsculas bolhas de gordura semelhantes às usadas em vacinas de mRNA — para entregar mRNA de Dpep2 especificamente a monócitos e macrófagos. Após injeção intravenosa, essas partículas elevaram brevemente os níveis de DPEP2 nas células-alvo. Em camundongos sépticos tratados com as nanopartículas carregadas com Dpep2, os marcadores de inflamação diminuíram, os danos pulmonares e orgânicos se atenuaram e a sobrevida melhorou em comparação com animais de controle. Importante, o tratamento funcionou sem toxicidade óbvia e teve efeito transitório (cerca de um dia e meio), alinhando-se com a janela inicial crítica em que as mortes por sepse ocorrem com mais frequência.
O que isso significa para o futuro do tratamento da sepse
Este trabalho revela DPEP2 como uma salvaguarda natural crucial que impede que células que combatem infecções levem o corpo ao auto-dano letal. Ao mostrar que os níveis de DPEP2 em monócitos sanguíneos refletem a gravidade da doença, o estudo sugere que ele poderia servir como um biomarcador útil para sinalizar pacientes de maior risco. Ainda mais impressionante, o sucesso da terapia com mRNA-Dpep2 em nanopartículas em camundongos aponta para uma nova classe de tratamentos de precisão: em vez de suprimir amplamente a imunidade, os clínicos poderão, no futuro, ajustar interruptores metabólicos específicos dentro das células imunes para acalmar a tempestade inflamatória na sepse enquanto preservam a defesa do hospedeiro.
Citação: Luo, W., Xu, W., Yin, Q. et al. DPEP2 suppresses hyperinflammation via metabolic reprogramming of macrophages in sepsis. Nat Commun 17, 3710 (2026). https://doi.org/10.1038/s41467-026-70466-4
Palavras-chave: sepse, macrófagos, imunometabolismo, mediadores lipídicos, terapia por mRNA