Clear Sky Science · fr
DPEP2 supprime l’hyperinflammation via le reprogrammation métabolique des macrophages dans la septicémie
Pourquoi calmer la réaction excessive de l’organisme est important
La septicémie est une affection potentiellement mortelle dans laquelle le système immunitaire, tentant de lutter contre une infection, se met en surrégime et commence à endommager les propres organes de l’organisme. Malgré les antibiotiques et les soins intensifs modernes, de nombreuses personnes meurent encore car cette inflammation incontrôlée est difficile à maîtriser sans compromettre les défenses vitales. Cette étude met au jour une molécule « frein » naturelle dans les cellules immunitaires de première ligne et montre comment la renforcer par une thérapie génique pourrait apaiser l’inflammation nocive tout en préservant la capacité à combattre les agents infectieux.
Un frein caché dans les cellules qui combattent l’infection
Les chercheurs se sont concentrés sur les monocytes et les macrophages, des cellules immunitaires qui circulent dans le sang et patrouillent les organes, déclenchant l’alerte lorsque des microbes envahissent. En utilisant des techniques de séquençage ARN unicellulaire et en masse de pointe sur le sang de patients au stade précoce de la septicémie, ils ont cartographié l’activité génique cellule par cellule. Un gène, appelé DPEP2, s’est démarqué : il était fortement actif dans les monocytes et macrophages sains mais systématiquement réduit chez les patients septicémiques. Des niveaux plus faibles de DPEP2 étaient étroitement corrélés à des scores d’insuffisance d’organe plus élevés, à des taux sanguins accrus de molécules inflammatoires et à un risque de décès plus important. Les patients survivants avaient plus de monocytes positifs pour DPEP2 que ceux qui n’ont pas survécu, ce qui suggère que cette molécule aide à contenir les impulsions les plus dangereuses du système immunitaire.
Du signal génique aux dommages à l’échelle du corps
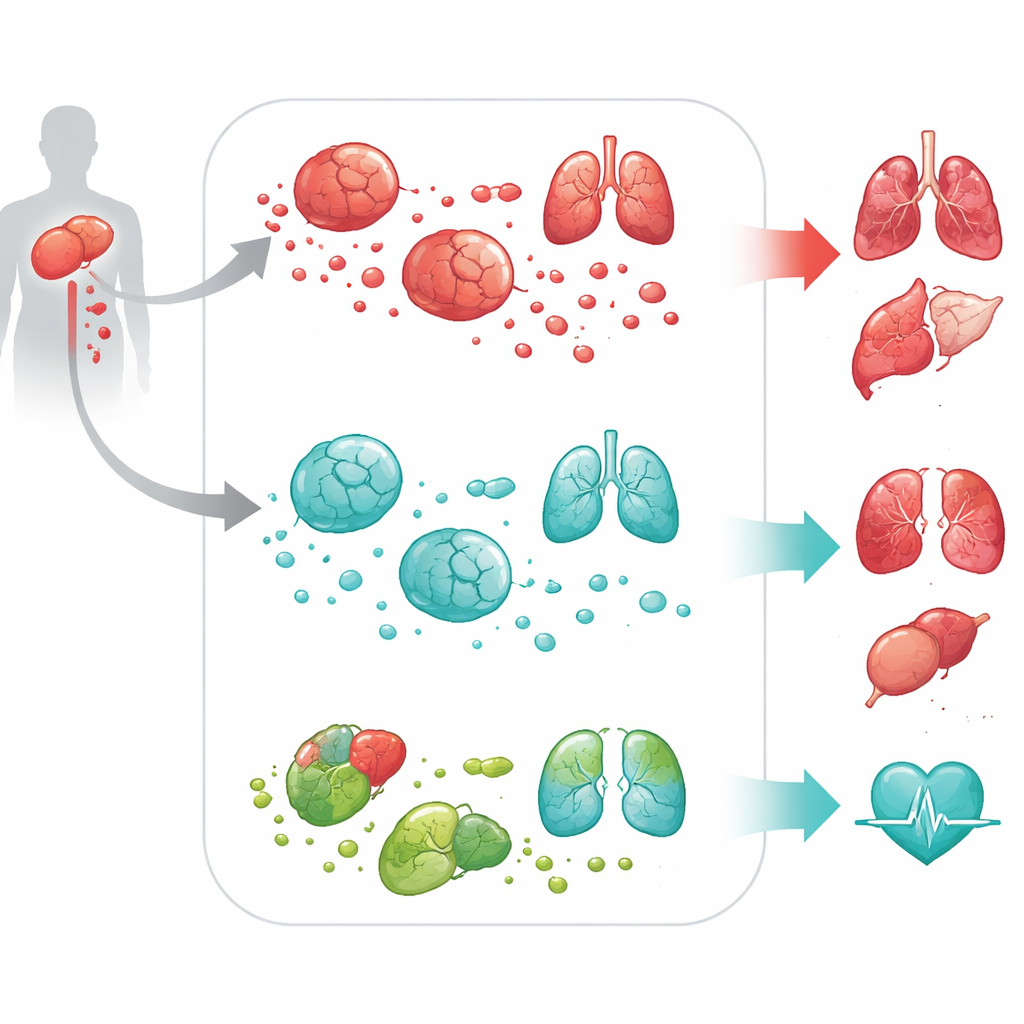
Pour tester si DPEP2 était simplement un marqueur ou un protecteur actif, l’équipe est passée à des modèles cellulaires et animaux. Dans des macrophages de souris et d’humain cultivés en laboratoire, l’inactivation de DPEP2 a amené ces cellules à libérer beaucoup plus de cytokines inflammatoires lorsqu’elles étaient stimulées par des composants bactériens. Dans un modèle standard de septicémie par chirurgie chez la souris, les animaux dépourvus de DPEP2 – soit dans tout l’organisme, soit spécifiquement dans les macrophages – se sont beaucoup plus mal portés. Ils présentaient des taux plus élevés de molécules inflammatoires dans le sang, des lésions plus sévères des poumons, du foie, des reins, du cœur et du cerveau, et des taux de mortalité significativement supérieurs. Ces expériences ont montré que DPEP2 n’est pas seulement un indicateur de gravité mais un défenseur actif contre l’inflammation incontrôlée.
Comment une enzyme de métabolisme lipidique étouffe le feu
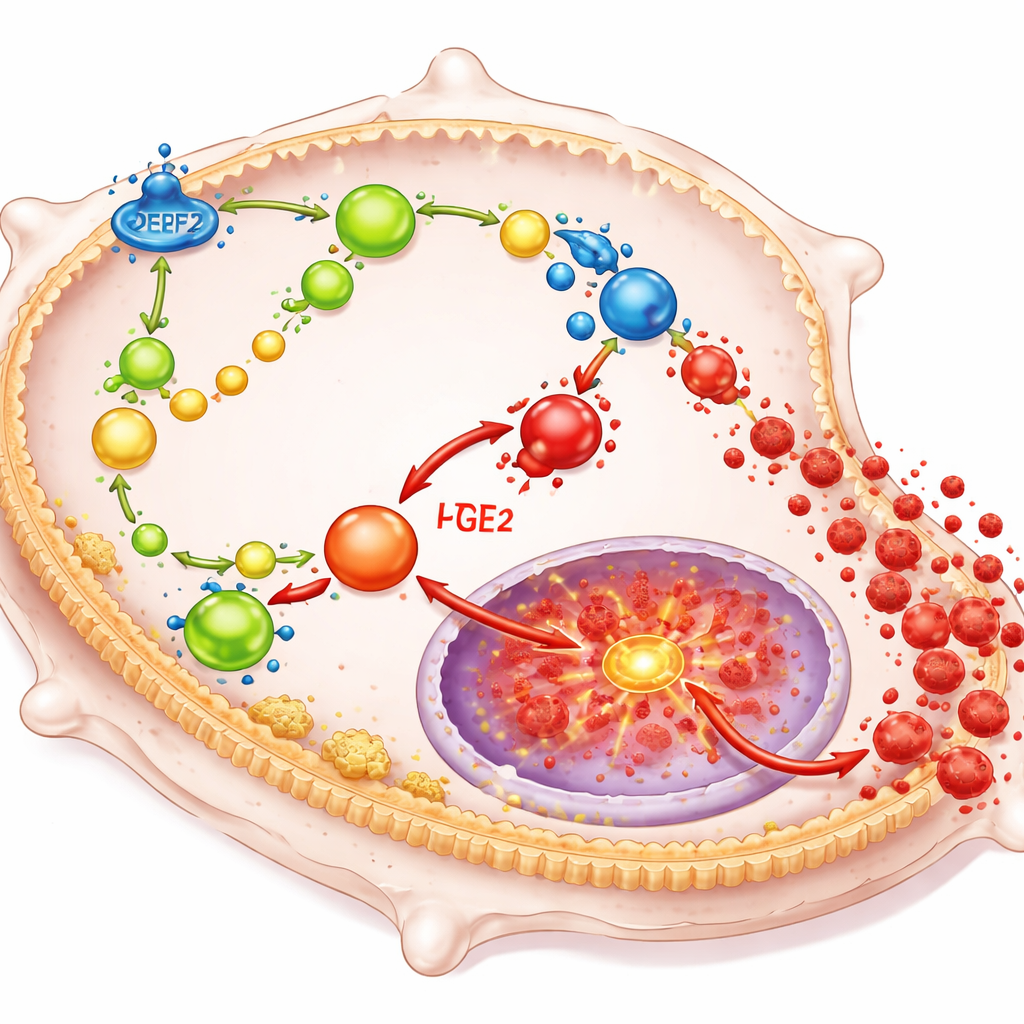
DPEP2 agit en remodelant la façon dont les macrophages traitent certains lipides qui font office d’hormones locales puissantes. En particulier, il aide à dégrader un composé appelé leucotriène D4 en un produit moins inflammatoire, et sa perte provoque une accumulation de leucotriène D4. Cette accumulation, à son tour, oriente davantage les précurseurs lipidiques de la cellule vers la production de prostaglandine E2, un autre puissant moteur de l’inflammation. Ensemble, ces lipides alimentent un interrupteur majeur à l’intérieur de la cellule connu sous le nom de NF-κB, qui contrôle les gènes de nombreuses cytokines inflammatoires. Lorsque DPEP2 est absent ou bas, ce réseau de signaux lipidiques tourne sans frein, activant NF-κB et poussant les macrophages à inonder l’organisme de facteurs inflammatoires dommageables.
Réécrire les cellules immunitaires avec de l’ARNm
Fortes de cet éclairage mécanique, les équipes ont testé si restaurer DPEP2 pouvait aider à sauver des animaux de la septicémie. Ils ont conçu des nanoparticules lipidiques — de minuscules bulles de graisse semblables à celles utilisées dans les vaccins à ARNm — pour délivrer l’ARNm de Dpep2 spécifiquement aux monocytes et macrophages. Après injection intraveineuse, ces particules ont brièvement augmenté les niveaux de DPEP2 dans les cellules cibles. Chez les souris septiques traitées par les nanoparticules chargées en Dpep2, les marqueurs d’inflammation ont diminué, les lésions pulmonaires et organiques se sont atténuées et la survie s’est améliorée par rapport aux animaux témoins. Fait important, le traitement a fonctionné sans toxicité évidente et son effet s’est estompé au bout d’environ un jour et demi, en phase avec la fenêtre précoce critique où surviennent le plus souvent les décès liés à la septicémie.
Ce que cela signifie pour la prise en charge future de la septicémie
Ce travail révèle DPEP2 comme une garde-fou naturelle cruciale qui empêche les cellules combattant l’infection de faire basculer l’organisme vers une auto-destruction létale. En montrant que les niveaux de DPEP2 dans les monocytes sanguins reflètent la gravité de la maladie, l’étude suggère qu’il pourrait servir de biomarqueur sanguin utile pour repérer les patients à risque le plus élevé. Plus remarquable encore, le succès de la thérapie par nanoparticules-ARNm Dpep2 chez la souris ouvre la voie à une nouvelle classe de traitements de précision : au lieu de supprimer l’immunité de manière large, les cliniciens pourraient un jour ajuster finement des interrupteurs métaboliques spécifiques à l’intérieur des cellules immunitaires pour calmer la tempête inflammatoire lors de la septicémie tout en préservant la défense de l’hôte.
Citation: Luo, W., Xu, W., Yin, Q. et al. DPEP2 suppresses hyperinflammation via metabolic reprogramming of macrophages in sepsis. Nat Commun 17, 3710 (2026). https://doi.org/10.1038/s41467-026-70466-4
Mots-clés: septicémie, macrophages, immunométabolisme, médiateurs lipidiques, thérapie par ARNm