Clear Sky Science · nl
DPEP2 onderdrukt hyperontsteking via metabole herprogrammering van macrofagen bij sepsis
Waarom het kalmeren van de overdreven reactie van het lichaam belangrijk is
Sepsis is een levensbedreigende aandoening waarbij het immuunsysteem van het lichaam, in een poging een infectie te bestrijden, in overdrive raakt en de eigen organen gaat beschadigen. Ondanks antibiotica en moderne intensivistische zorg overlijden nog steeds veel mensen omdat deze ontketende ontsteking moeilijk te beheersen is zonder essentiële afweerreacties uit te schakelen. Deze studie onthult een natuurlijk "remmolecuul" in de voorhoede van immuuncellen en toont aan hoe het versterken daarvan met een gen-gebaseerde therapie schadelijke ontsteking kan dempen terwijl het vermogen om ziekteverwekkers te bestrijden behouden blijft.
Een verborgen rem in infectiebestrijdende cellen
De onderzoekers richtten zich op monocyten en macrofagen, immuuncellen die in het bloed circuleren en organen bewaken en alarm slaan wanneer microben binnendringen. Met geavanceerde single-cell en bulk RNA-sequencing van bloed uit de vroege fase van sepsis brachten ze genactiviteit per cel in kaart. Eén gen, DPEP2 genaamd, bleek op te vallen: het was sterk actief in gezonde monocyten en macrofagen maar consequent verlaagd bij patiënten met sepsis. Lagere DPEP2-niveaus waren nauw verbonden met slechtere orgaanfalingsscores, hogere concentraties ontstekingsmoleculen in het bloed en een hoger sterfterisico. Patiënten die overleefden hadden meer DPEP2-positieve monocyten dan zij die overleden, wat suggereert dat dit molecuul helpt de gevaarlijkste impulsen van het immuunsysteem te beteugelen.
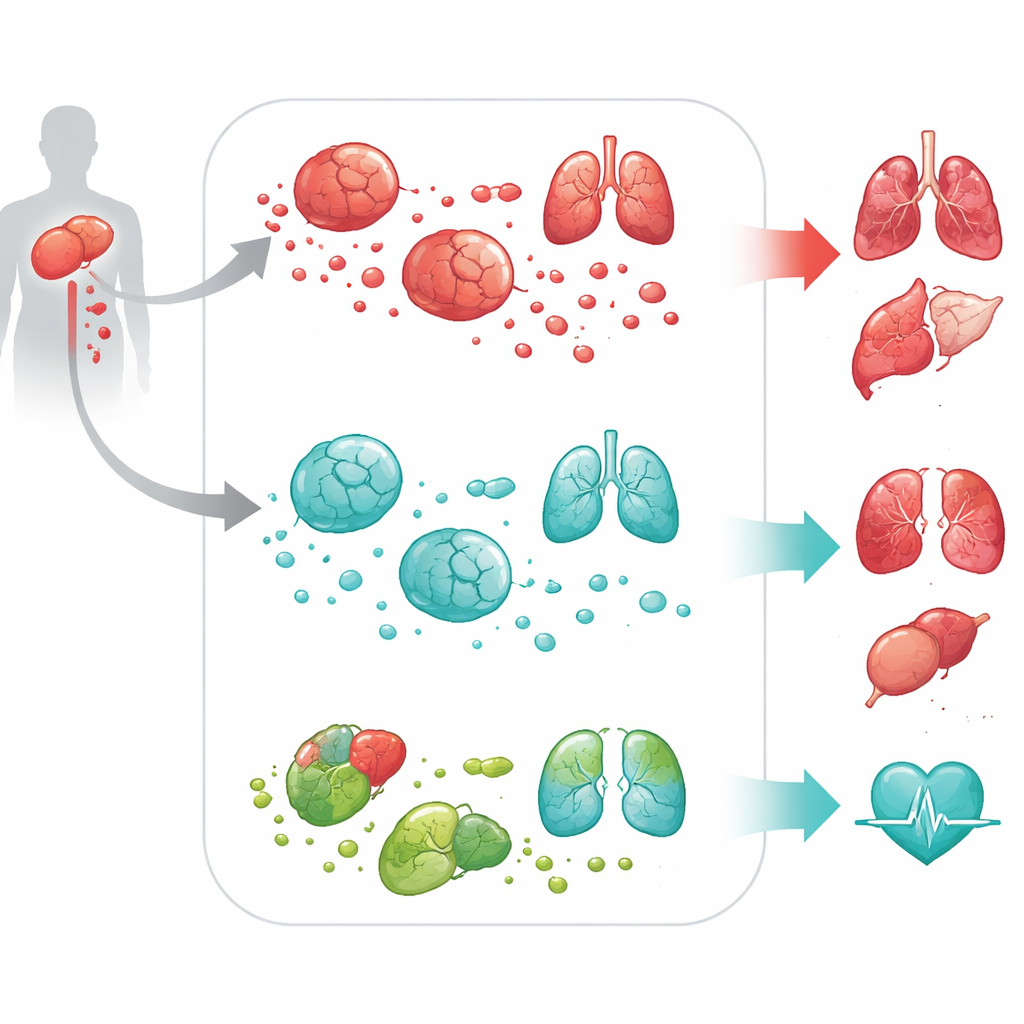
Van gen-signaal naar schade in het hele lichaam
Om te testen of DPEP2 slechts een bijstander of een actieve beschermer was, wendde het team zich tot cel- en diermodellen. In in vitro gekweekte muis- en humane macrofagen leidde het uitschakelen van DPEP2 ertoe dat deze cellen veel meer ontstekingscytokinen afscheidden wanneer ze werden gestimuleerd met bacteriële componenten. In muizen die werden onderworpen aan een standaard, chirurgisch gebaseerde sepsismodel, deden dieren zonder DPEP2 — zowel algemeen als specifiek in macrofagen — het veel slechter. Ze hadden hogere niveaus van ontstekingsmoleculen in de bloedbaan, ernstigere schade aan longen, lever, nieren, hart en hersenen, en aanzienlijk hogere sterftecijfers. Deze experimenten toonden aan dat DPEP2 niet alleen een merker van ziekteernst is, maar een actieve verdediger tegen overweldigende ontsteking.
Hoe een vetverwerkend enzym het vuur tempert
DPEP2 werkt door te veranderen hoe macrofagen bepaalde vetmoleculen verwerken die dienstdoen als krachtige lokale hormonen. In het bijzonder helpt het de afbraak van een verbinding genaamd leukotrieen D4 naar een minder ontstekingsbevorderend product, en het verlies hiervan veroorzaakt ophoping van leukotrieen D4. Die ophoping duwt op haar beurt meer van de vetbouwstenen van de cel richting de aanmaak van prostaglandine E2, een andere sterke ontstekingsdriver. Deze lipiden voeden samen een belangrijke schakel binnen de cel, bekend als NF-κB, die genen reguleert voor veel ontstekingscytokinen. Wanneer DPEP2 ontbreekt of laag is, loopt dit netwerk van vetgebaseerde signalen ongehinderd door, activeert NF-κB en doet macrofagen het lichaam overspoelen met schadelijke ontstekingsfactoren.
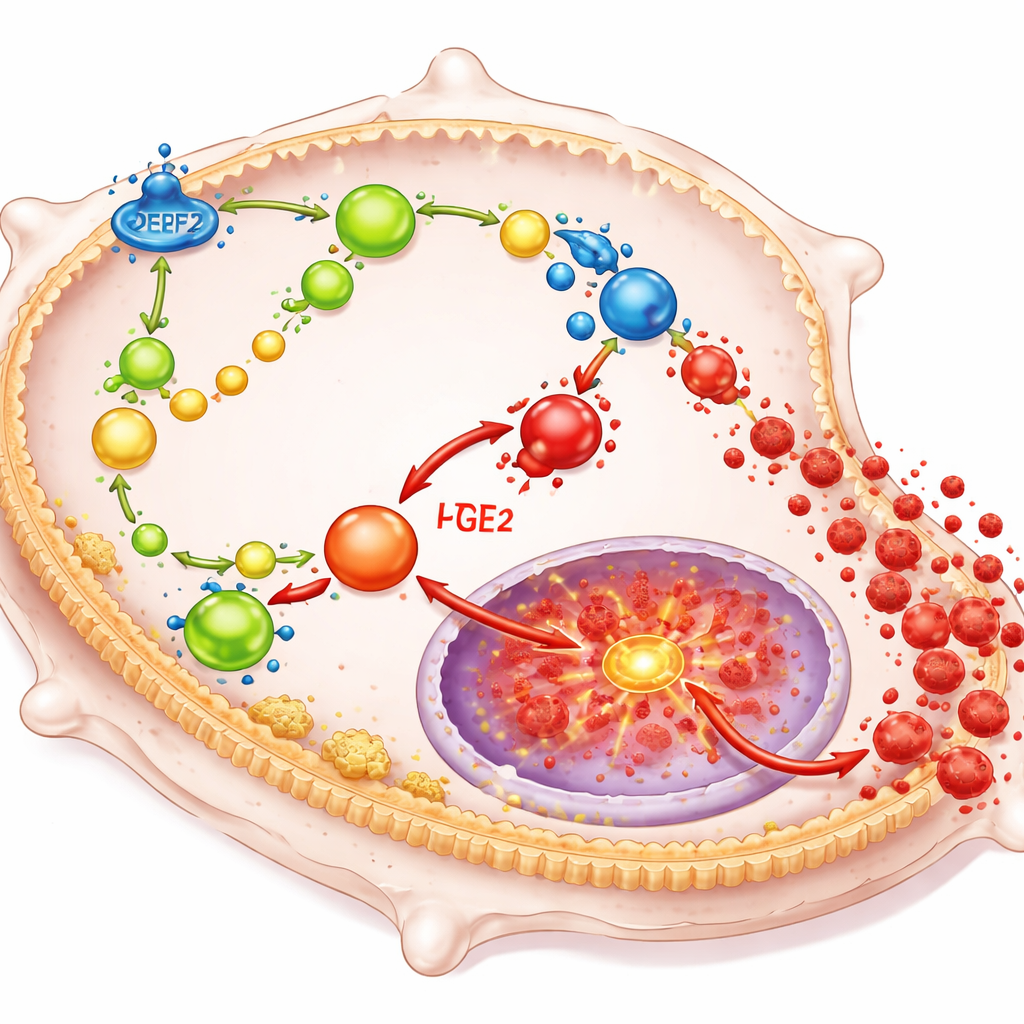
Immunocellen herschrijven met mRNA
Gewapend met dit mechanistische inzicht vroegen de wetenschappers zich af of het herstellen van DPEP2 dieren uit sepsis zou kunnen redden. Ze ontwierpen lipide-nanodeeltjes — kleine vetbellen vergelijkbaar met die gebruikt in mRNA-vaccins — om Dpep2-mRNA specifiek in monocyten en macrofagen af te leveren. Na intraveneuze injectie verhoogden deze deeltjes kortstondig DPEP2-niveaus in de doelcellen. In septische muizen die werden behandeld met de Dpep2-beladen nanodeeltjes daalden ontstekingsmarkers, verminderde long- en orgaanschade en verbeterde de overleving vergeleken met controledieren. Belangrijk is dat de behandeling zonder duidelijke toxiciteit werkte en na ongeveer een anderhalve dag afnam, wat overeenkomt met het kritieke vroege venster waarin sepsissterfte het vaakst voorkomt.
Wat dit betekent voor toekomstige sepsiszorg
Dit werk onthult DPEP2 als een cruciale natuurlijke beveiliging die voorkomt dat infectiebestrijdende cellen het lichaam in dodelijke zelfbeschadiging duwen. Doordat wordt aangetoond dat DPEP2-niveaus in bloedmonocyten de ziekteernst weerspiegelen, suggereert de studie dat het als een nuttige bloedbiomarker kan dienen om patiënten met het hoogste risico te signaleren. Nog opvallender is dat het succes van de Dpep2-mRNA–nanodeeltje therapie in muizen wijst op een nieuwe klasse van precisiebehandelingen: in plaats van de immuniteit breed te onderdrukken, zouden clinici op termijn specifieke metabole schakelaars binnen immuuncellen kunnen bijstellen om de inflammatoire storm bij sepsis te koelen en tegelijk de gastheerverdediging te behouden.
Bronvermelding: Luo, W., Xu, W., Yin, Q. et al. DPEP2 suppresses hyperinflammation via metabolic reprogramming of macrophages in sepsis. Nat Commun 17, 3710 (2026). https://doi.org/10.1038/s41467-026-70466-4
Trefwoorden: sepsis, macrofagen, immunometabolisme, lipidemediaatoren, mRNA-therapie