Clear Sky Science · he
DPEP2 מדכא דלקת יתר באמצעות תכנות מטבולי מחדש של מאקרופגים בספסיס
מדוע חשוב להרגיע תגובת יתר של הגוף
ספסיס הוא מצב מסכן חיים שבו מערכת החיסון של הגוף, בניסיון להילחם בזיהום, נכנסת למצב של פעילות יתר ומתחילה לפגוע בעצמם האיברים. למרות אנטיביוטיקה וטיפול נמרץ מודרני, רבים עדיין מתים כי הדלקת המתגברת קשה לשליטה מבלי לכבות גם מנגנוני הגנה חיוניים. מחקר זה חושף מולקולת "בלם" טבעית בתאי חיסון קו-החזית ומראה כיצד חיזוקה באמצעות טיפול מבוסס גן עשוי להשקיט דלקת מזיקה תוך שמירה על היכולת להילחם במיקרובים.
בלם מוסתר בתוך תאי הלחימה בזיהום
החוקרים התמקדו במונוציטים ובמאקרופגים, תאי חיסון שנעים במחזור הדם וסורקים איברים, ומפעילים אזעקה כשהמיקרובים חודרים. באמצעות ריצוף RNA חד-תאי וריצוף עוצמה כולל על דם של מטופלים בשלב המוקדם של ספסיס הם מיפו פעילות גנים תאי אחר תא. גן אחד, בשם DPEP2, בלט: הוא היה פעיל בעוצמה במונוציטים ובמאקרופגים בריאים אך נמצא מופחת בעקביות בחולים עם ספסיס. רמות נמוכות של DPEP2 נקשרו בחוזקה לציוני כשל איברים גרועים יותר, לרמות גבוהות של מולקולות דלקתיות בדם ולסיכון תמותה גבוה יותר. חולים ששרדו הציגו יותר מונוציטים חיוביים ל-DPEP2 בהשוואה לאלה שלא שרדו, מה שמרמז שהמולקולה מסייעת לרסן את הדחפים המסוכנים ביותר של מערכת החיסון.
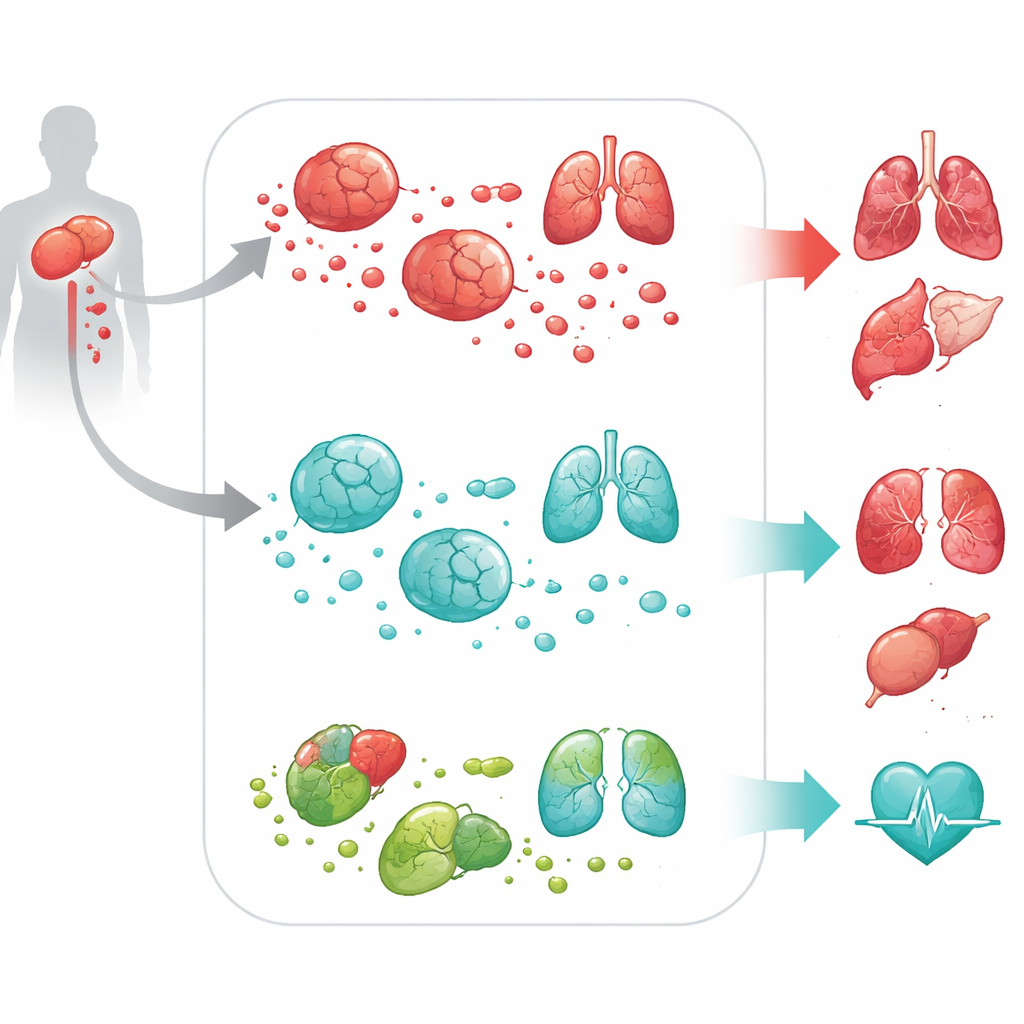
מאותות גנטיים לנזק לכל הגוף
כדי לבדוק האם DPEP2 הוא רק צופה מהצד או שומר פעיל, הצוות פנה למודלים תאים ובעלי חיים. במאקרופגים של עכבר ושל אדם המגודלים במעבדה, כיבוי DPEP2 גרם לתאים אלה להפריש הרבה יותר ציטוקינים דלקתיים כאשר הועלו בגירוי עם רכיבי חיידקים. בעכברים שנחשפו למודל ספסיס סטנדרטי בגישה ניתוחית, בעלי חיים חסרי DPEP2 – בין אם בכל הגוף ובין אם באופן ספציפי רק במאקרופגים – עברו מהלך קשה יותר בהרבה. היו להם רמות גבוהות יותר של מולקולות דלקת בזרם הדם, פגיעה חמורה יותר בריאות, בכבד, בכליות, בלב ובמוח, ושיעורי תמותה גבוהים משמעותית. ניסויים אלה הראו ש-DPEP2 אינו רק סימן לחומרת המחלה אלא מגן פעיל מפני דלקת משתוללת.
כיצד אנזים לעיבוד שומנים מרסן את הלהבה
DPEP2 פועל על ידי שינוי הדרך שבה מאקרופגים מעבדים מולקולות שומניות מסוימות שמשמשות כהורמונים מקומיים רבי עוצמה. באופן ספציפי, הוא מסייע בפירוק תרכובת בשם ליקוטריאן D4 לתוצר פחות דלקתי, והיעלמותו גורמת להצטברות של ליקוטריאן D4. הצטברות זו, בתורה, דוחפת עוד מרכיבי בניין שומניים של התא לייצור פרוסטגלנדין E2, דרייבר חזק נוסף של דלקת. יחד, שומנים אלה מזינים מתג מרכזי בתוך התא הידוע כ-NF-κB, שהוא שולט בגנים של ציטוקינים דלקתיים רבים. כאשר DPEP2 חסר או נמוך, רשת האותות מבוססת השומן הזו פועלת ללא מעצורים, מפעילה את NF-κB וגורמת למאקרופגים להציף את הגוף בגורמי דלקת מזיקים.
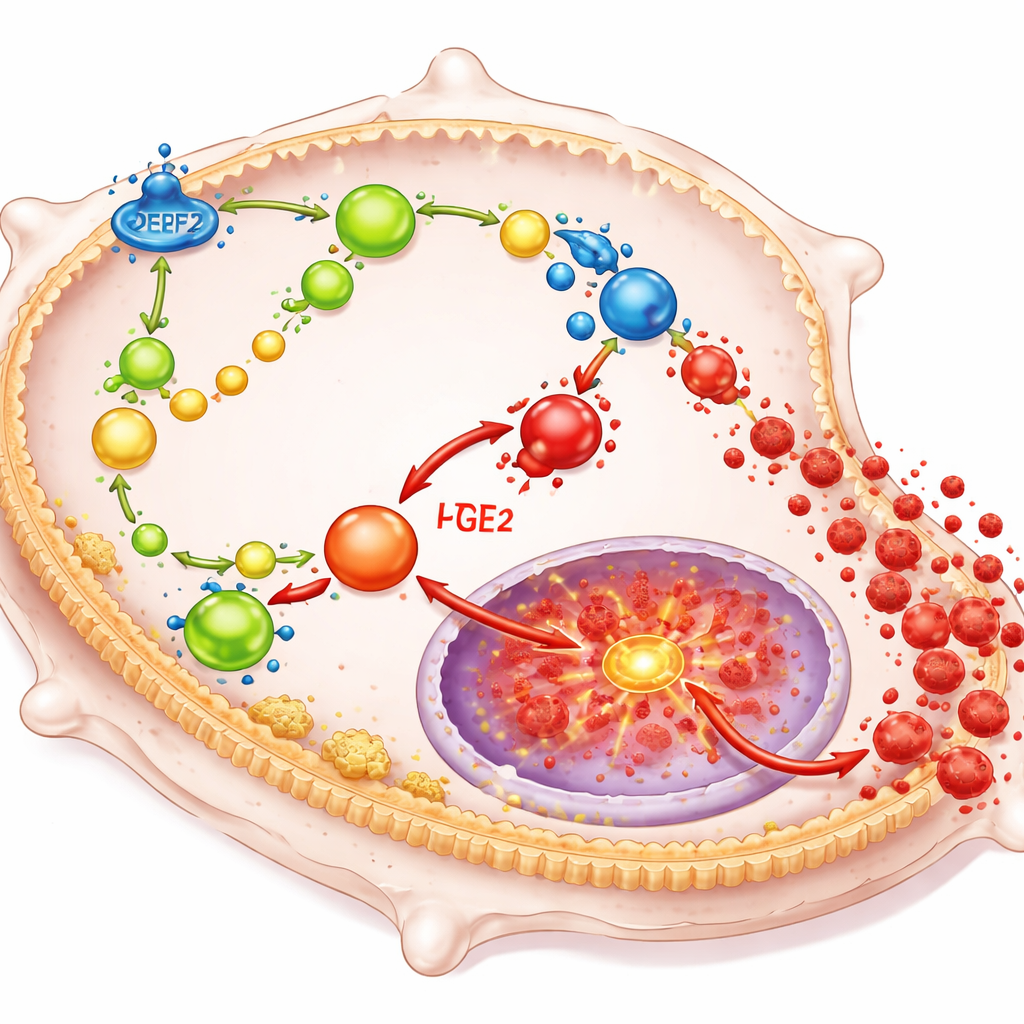
שכתוב תאי חיסון עם mRNA
מצוידים בתובנה מכניסטית זו, המדענים שאלו האם שיחזור DPEP2 יכול להציל בעלי חיים מספסיס. הם תכננו ננו-חלקיקי שומנים — בועיות שומן זעירות הדומות לאלו שבחיסוני mRNA — כדי להעביר mRNA של Dpep2 במיוחד למונוציטים ולמאקרופגים. לאחר הזרקה תוך-ורידית, חלקיקים אלה הגביהו זמנית את רמות DPEP2 בתאים המטרה. בעכברים ספטיים שטופלו בננו-חלקיקים טעוני Dpep2, סימני הדלקת ירדו, נזק לריאות ולאיברים הקל, וההישרדות השתפרה בהשוואה לבעלי חיים בקבוצת הביקורת. חשוב לציין, הטיפול עבד ללא רעילות ברורה ודעך לאחר כיממה וציוני חצי, בהתאם לחלון המוקדם הקריטי שבו בדרך כלל מתרחשות מקרי המוות מספסיס.
מה משמעות זאת לטיפול עתידי בספסיס
עבודה זו חושפת את DPEP2 כמנגנון טבעי מהותי שמונע מתאי ההגנה בזיהום לגלוש לפגיעה קטלנית עצמית של הגוף. על ידי הראייה שרמות DPEP2 במונוציטים בדם משקפות את חומרת המחלה, המחקר מציע שהוא עשוי לשמש כסמן דם שימושי לזיהוי מטופלים בסיכון הגבוה ביותר. וביותר מרשים, הצלחת טיפולי ה-mRNA–ננו-חלקיקים עם Dpep2 בעכברים מציינת כיתה חדשה של טיפולים ממוקדים: במקום לדכא את המערכת החיסונית באופן כולל, ייתכן שבעתיד הרופאים יוכלו לכוונן מתגים מטבוליים ספציפיים בתוך תאי החיסון כדי לקרר את סערת הדלקת בספסיס תוך שמירה על ההגנה של המאחסן.
ציטוט: Luo, W., Xu, W., Yin, Q. et al. DPEP2 suppresses hyperinflammation via metabolic reprogramming of macrophages in sepsis. Nat Commun 17, 3710 (2026). https://doi.org/10.1038/s41467-026-70466-4
מילות מפתח: ספסיס, מאקרופגים, אימונומטבוליזם, מתווכים שומניים, טיפול ב-mRNA