Clear Sky Science · pl
DPEP2 tłumi nadmierne zapalenie poprzez przeprogramowanie metaboliczne makrofagów w sepsie
Dlaczego ważne jest utemperowanie nadreakcji organizmu
Sepsa to stan zagrażający życiu, w którym układ odpornościowy, próbując zwalczyć infekcję, wpada w nadmierną aktywność i zaczyna uszkadzać własne narządy. Pomimo antybiotyków i współczesnej intensywnej opieki medycznej wielu pacjentów nadal umiera, ponieważ ta wymykająca się spod kontroli zapalna reakcja jest trudna do opanowania bez jednoczesnego wyłączenia istotnych mechanizmów obronnych. Badanie to odkrywa naturalną „hamulec” w komórkach pierwszej linii obrony i pokazuje, jak zwiększenie jego działania za pomocą terapii genowej może uciszyć szkodliwe zapalenie, zachowując jednocześnie zdolność do zwalczania drobnoustrojów.
Ukryty hamulec w komórkach walczących z infekcją
Naukowcy skupili się na monocytach i makrofagach, komórkach układu odpornościowego krążących we krwi i patrolujących narządy, które uruchamiają alarm, gdy pojawią się mikroby. Wykorzystując nowoczesne techniki jednorodnościowe i analizy RNA z próbek krwi pacjentów we wczesnej fazie sepsy, zmapowali aktywność genów komórka po komórce. Jeden gen o nazwie DPEP2 wyróżniał się: był silnie aktywny w zdrowych monocytach i makrofagach, ale konsekwentnie obniżony u pacjentów z sepsą. Niższe poziomy DPEP2 ściśle korelowały z gorszymi wynikami w skali niewydolności narządów, wyższymi stężeniami cząsteczek zapalnych we krwi oraz większym ryzykiem zgonu. Pacjenci, którzy przeżyli, mieli więcej monocytów pozytywnych pod względem DPEP2 niż ci, którzy zmarli, co sugeruje, że ta cząsteczka pomaga powstrzymywać najgroźniejsze impulsy układu odpornościowego.
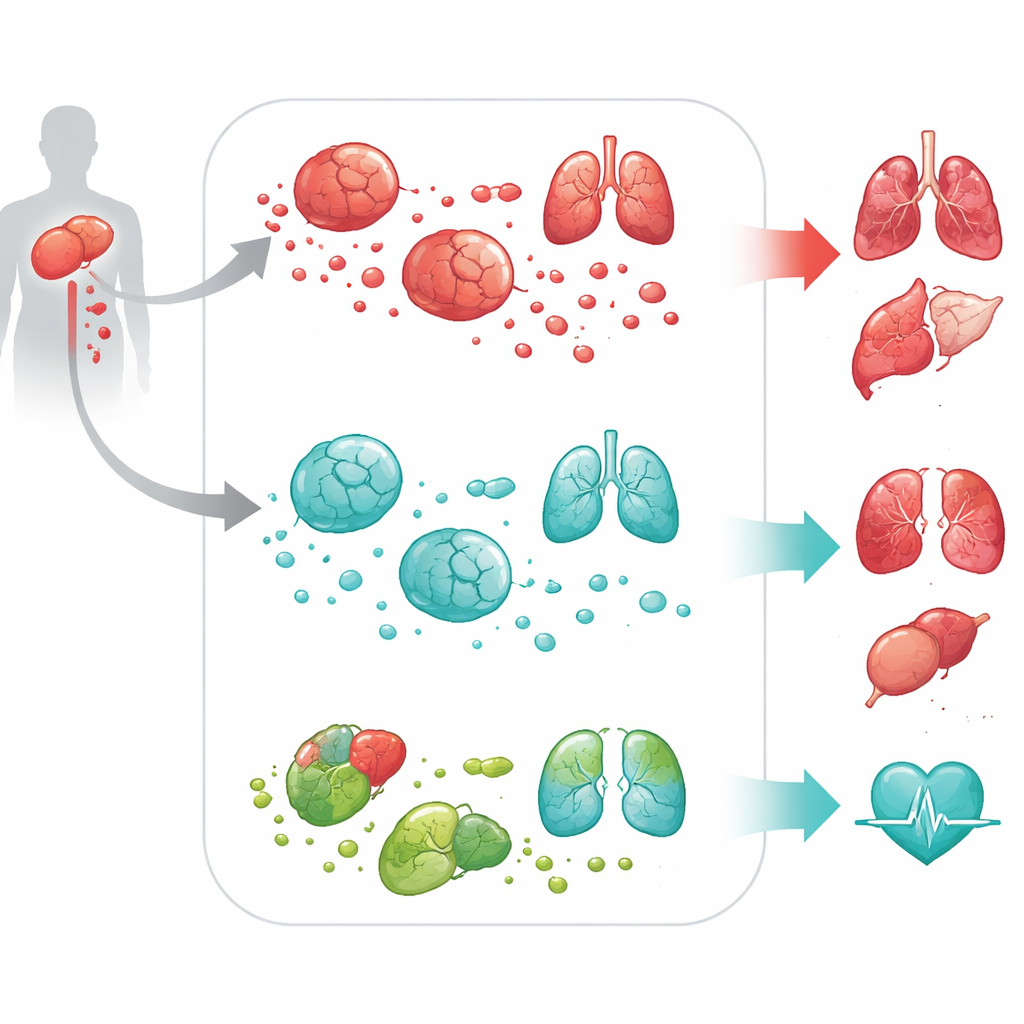
Od sygnału genowego do uszkodzeń całego organizmu
Aby sprawdzić, czy DPEP2 jest tylko obserwatorem, czy aktywnym obrońcą, zespół sięgnął po modele komórkowe i zwierzęce. W makrofagach mysich i ludzkich hodowanych w laboratorium wyłączenie DPEP2 spowodowało, że komórki te wydzielały znacznie więcej cytokin zapalnych po stymulacji składnikami bakteryjnymi. W modelu sepsy u myszy opartym na standardowym zabiegu chirurgicznym zwierzęta pozbawione DPEP2 — zarówno globalnie, jak i specyficznie w makrofagach — radziły sobie znacznie gorzej. Miały wyższe stężenia czynników zapalnych we krwi, cięższe uszkodzenia płuc, wątroby, nerek, serca i mózgu oraz istotnie wyższe wskaźniki śmiertelności. Te eksperymenty wykazały, że DPEP2 nie jest tylko markerem ciężkości choroby, lecz aktywną tarczą przeciwko wymykającemu się spod kontroli zapaleniu.
Jak enzym przetwarzający tłuszcze gasi ogień
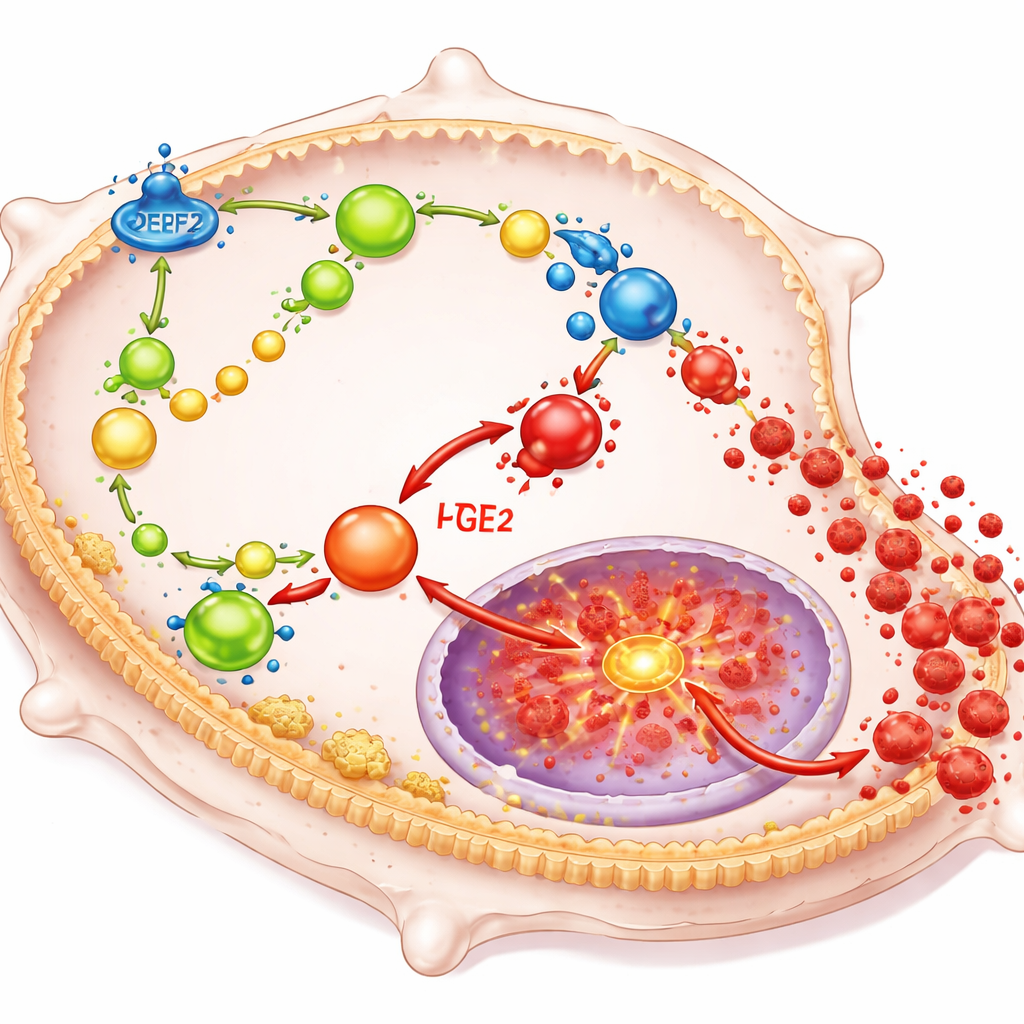
DPEP2 działa, przekształcając sposób, w jaki makrofagi metabolizują pewne cząsteczki tłuszczowe pełniące rolę silnych lokalnych hormonów. W szczególności pomaga rozkładać związek zwany leukotrienem D4 do mniej zapalnego produktu, a jego utrata prowadzi do nagromadzenia leukotrienu D4. To nagromadzenie z kolei przesuwa więcej lipidowych elementów budulcowych komórki w kierunku syntezy prostaglandyny E2, kolejnego silnego czynnika prozapalnego. Te lipidy razem aktywują kluczowy włącznik wewnątrzkomórkowy znany jako NF-κB, który kontroluje geny kodujące wiele cytokin zapalnych. Gdy DPEP2 jest nieobecny lub jego poziom jest niski, ta sieć sygnałów lipidowych pracuje bez hamulca, nadmiernie aktywując NF-κB i powodując, że makrofagi zalewają organizm szkodliwymi czynnikami zapalnymi.
Przepisanie komórek odpornościowych za pomocą mRNA
Wyposażeni w to mechanistyczne zrozumienie, naukowcy sprawdzili, czy przywrócenie DPEP2 może pomóc uratować zwierzęta przed sepsą. Zaprojektowali nanocząsteczki lipidowe — maleńkie pęcherzyki tłuszczowe podobne do tych używanych w szczepionkach mRNA — aby dostarczyć mRNA Dpep2 specyficznie do monocytów i makrofagów. Po dożylnym podaniu cząsteczki te krótkotrwale zwiększały poziomy DPEP2 w komórkach docelowych. U myszy z sepsą traktowanych nanocząsteczkami zawierającymi Dpep2 spadły markery zapalenia, zmniejszyły się uszkodzenia płuc i innych narządów, a przeżywalność poprawiła się w porównaniu z kontrolnymi zwierzętami. Co ważne, leczenie działało bez widocznej toksyczności i ustępowało po około półtorej dobie, co pokrywa się z krytycznym wczesnym oknem, gdy najczęściej występują zgony z powodu sepsy.
Co to oznacza dla przyszłej opieki nad sepsą
Praca ta ujawnia DPEP2 jako istotne naturalne zabezpieczenie, które powstrzymuje komórki walczące z infekcją przed doprowadzeniem organizmu do śmiertelnego samozniszczenia. Pokazując, że poziomy DPEP2 w monocytach krwi odzwierciedlają ciężkość choroby, badanie sugeruje, że może on służyć jako użyteczny marker krwi do wyłapywania pacjentów o najwyższym ryzyku. Jeszcze bardziej uderzające jest to, że powodzenie terapii mRNA z Dpep2 w nanocząsteczkach u myszy wskazuje na nową klasę precyzyjnych terapii: zamiast szeroko tłumić odporność, klinicyści mogliby w przyszłości precyzyjnie modulować konkretne przełączniki metaboliczne w komórkach odpornościowych, aby ostudzić burzę zapalną w sepsie, zachowując jednocześnie obronę gospodarza.
Cytowanie: Luo, W., Xu, W., Yin, Q. et al. DPEP2 suppresses hyperinflammation via metabolic reprogramming of macrophages in sepsis. Nat Commun 17, 3710 (2026). https://doi.org/10.1038/s41467-026-70466-4
Słowa kluczowe: sepsa, makrofagi, immunometabolizm, mediatory lipidowe, terapia mRNA