Clear Sky Science · es
DPEP2 suprime la hiperinflamación mediante la reprogramación metabólica de macrófagos en la sepsis
Por qué es importante calmar la sobrerreacción del cuerpo
La sepsis es una condición potencialmente mortal en la que el sistema inmunitario, al intentar combatir una infección, se desboca y comienza a dañar los propios órganos. A pesar de los antibióticos y los cuidados intensivos modernos, muchas personas siguen falleciendo porque esta inflamación descontrolada es difícil de controlar sin paralizar defensas vitales. Este estudio descubre una molécula “freno” natural en las células inmunitarias de primera línea y muestra cómo potenciarla con una terapia basada en genes podría silenciar la inflamación dañina al tiempo que preserva la capacidad de combatir los gérmenes.
Un freno oculto dentro de las células que combaten la infección
Los investigadores se centraron en monocitos y macrófagos, células inmunitarias que circulan en la sangre y vigilan los órganos, dando la alarma cuando invaden microbios. Empleando avanzadas técnicas de secuenciación de ARN unicelular y en masa en sangre de pacientes en la fase temprana de la sepsis, mapearon la actividad génica célula por célula. Un gen, llamado DPEP2, destacó: estaba fuertemente activo en monocitos y macrófagos sanos, pero consistentemente reducido en pacientes con sepsis. Los niveles bajos de DPEP2 se asociaron estrechamente con peores puntuaciones de fallo orgánico, niveles más altos de moléculas inflamatorias en sangre y un mayor riesgo de muerte. Los pacientes que sobrevivieron tenían más monocitos positivos para DPEP2 que los que no, lo que sugiere que esta molécula ayuda a contener los impulsos más peligrosos del sistema inmunitario.
Del indicador génico al daño sistémico
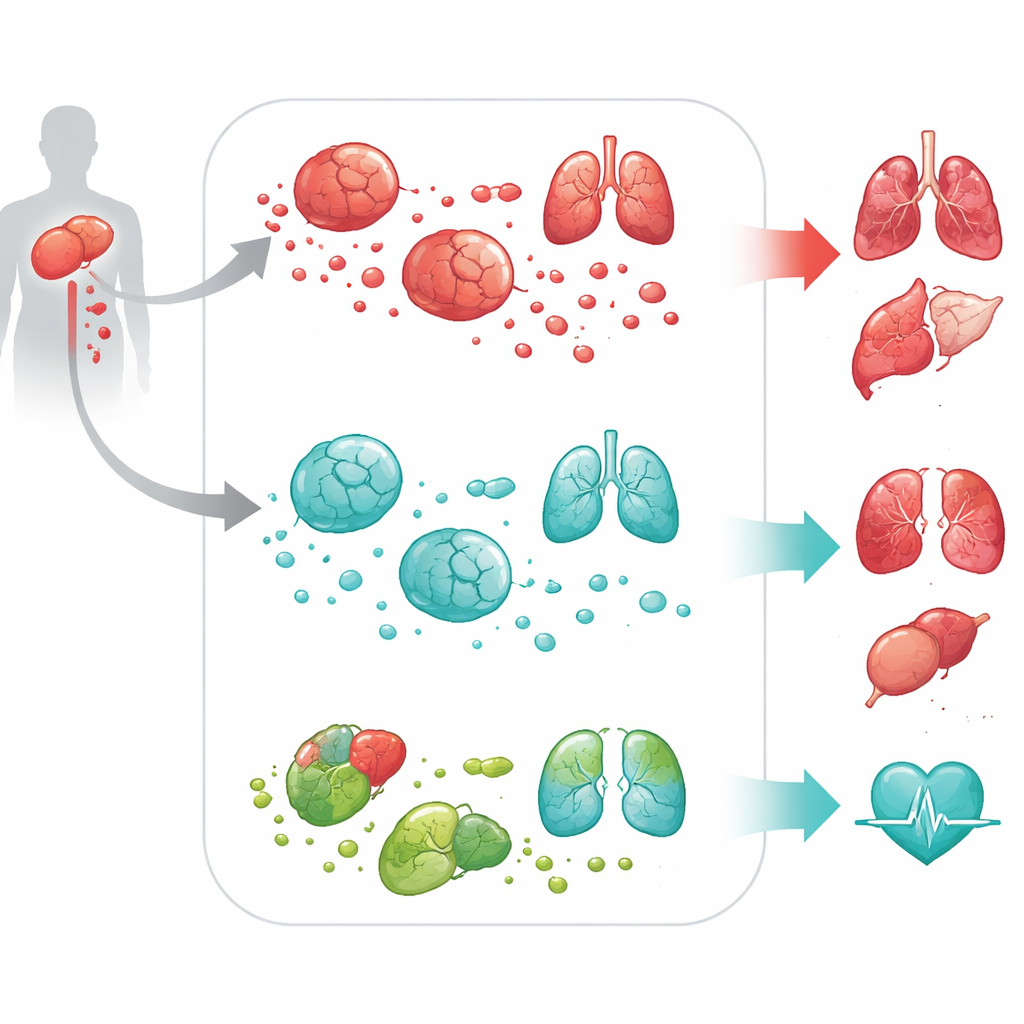
Para comprobar si DPEP2 era meramente un espectador o un protector activo, el equipo recurrió a modelos celulares y animales. En macrófagos de ratón y humanos cultivados en el laboratorio, desactivar DPEP2 hizo que estas células secretaran muchas más citocinas inflamatorias cuando se las estimuló con componentes bacterianos. En ratones sometidos a un modelo estándar de sepsis inducida por cirugía, los animales sin DPEP2 —ya sea de forma global o específicamente en macrófagos— empeoraron notablemente. Presentaron niveles más altos de moléculas inflamatorias en el torrente sanguíneo, lesiones más graves en pulmones, hígado, riñón, corazón y cerebro, y tasas de mortalidad significativamente mayores. Estos experimentos demostraron que DPEP2 no es solo un marcador de la gravedad de la enfermedad, sino un defensor activo contra la inflamación abrumadora.
Cómo una enzima que procesa grasas apaga el fuego
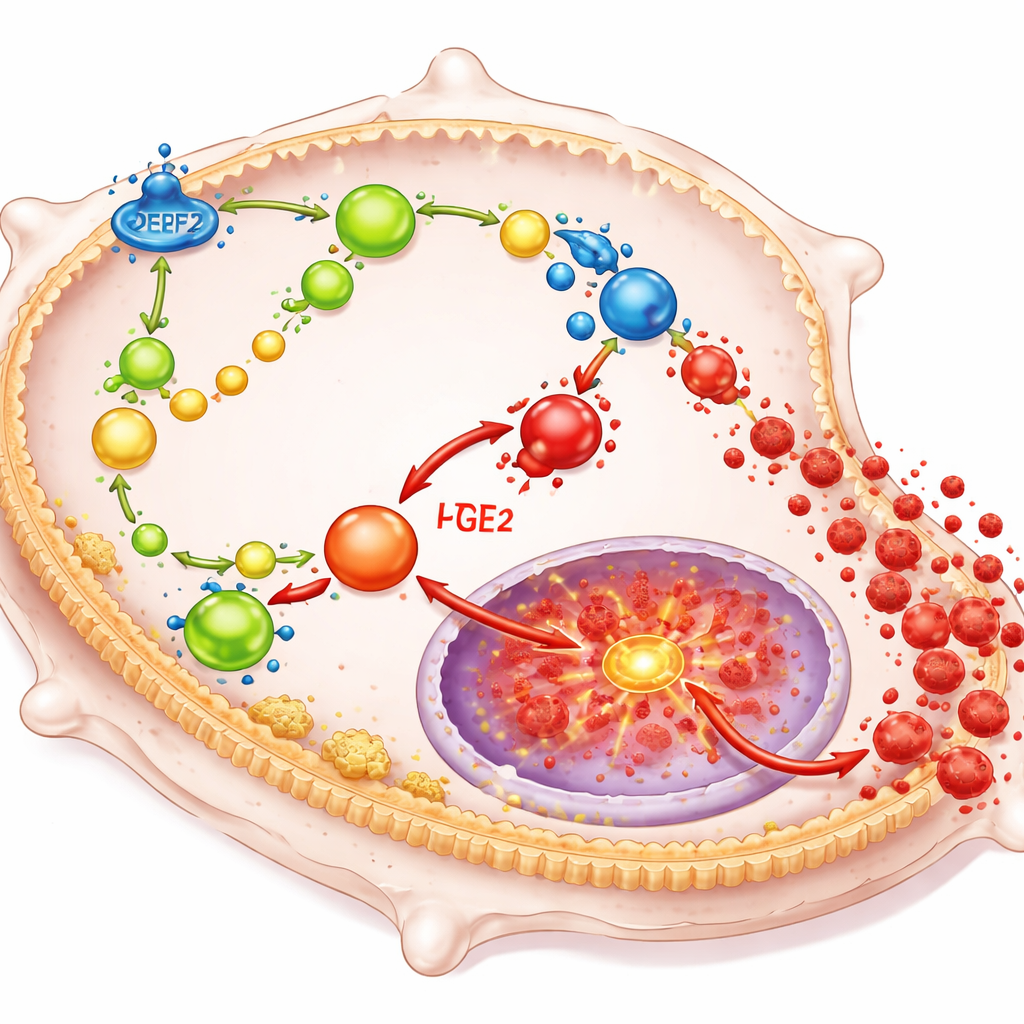
DPEP2 actúa reconfigurando la forma en que los macrófagos manejan ciertos lípidos que funcionan como potentes hormonas locales. En particular, ayuda a descomponer un compuesto llamado leucotrieno D4 en un producto menos inflamatorio, y su pérdida provoca la acumulación de leucotrieno D4. Esa acumulación, a su vez, empuja a que más bloques lipídicos de la célula se dirijan a la síntesis de prostaglandina E2, otro potente impulsor de la inflamación. En conjunto, estos lípidos alimentan un conmutador intracelular clave conocido como NF-κB, que controla genes de muchas citocinas inflamatorias. Cuando DPEP2 falta o está bajo, esta red de señales basadas en lípidos queda fuera de control, activando NF-κB y provocando que los macrófagos inunden el organismo con factores inflamatorios dañinos.
Reescribiendo células inmunes con ARNm
Armados con esta visión mecanística, los científicos se preguntaron si restaurar DPEP2 podría ayudar a rescatar animales con sepsis. Diseñaron nanopartículas lipídicas —minúsculas burbujas grasas similares a las utilizadas en vacunas de ARNm— para entregar ARNm de Dpep2 específicamente a monocitos y macrófagos. Tras la inyección intravenosa, estas partículas aumentaron brevemente los niveles de DPEP2 en las células objetivo. En ratones sépticos tratados con las nanopartículas cargadas con Dpep2, los marcadores de inflamación descendieron, el daño pulmonar y orgánico se atenuó y la supervivencia mejoró en comparación con animales control. Es importante que el tratamiento funcionó sin toxicidad evidente y se desvaneció después de aproximadamente día y medio, coincidiendo con la ventana temprana crítica en la que ocurren la mayoría de las muertes por sepsis.
Qué significa esto para la atención futura de la sepsis
Este trabajo revela a DPEP2 como una salvaguardia natural crucial que impide que las células que combaten la infección empujen al cuerpo hacia un daño autoinfligido letal. Al mostrar que los niveles de DPEP2 en monocitos sanguíneos reflejan la gravedad de la enfermedad, el estudio sugiere que podría servir como un biomarcador útil en sangre para identificar a los pacientes con mayor riesgo. Aun más llamativo, el éxito de la terapia con ARNm-Dpep2 en nanopartículas en ratones apunta a una nueva clase de tratamientos de precisión: en lugar de suprimir la inmunidad de forma general, los clínicos podrían algún día afinar interruptores metabólicos específicos dentro de las células inmunitarias para enfriar la tormenta inflamatoria en la sepsis conservando la defensa del huésped.
Cita: Luo, W., Xu, W., Yin, Q. et al. DPEP2 suppresses hyperinflammation via metabolic reprogramming of macrophages in sepsis. Nat Commun 17, 3710 (2026). https://doi.org/10.1038/s41467-026-70466-4
Palabras clave: sepsis, macrófagos, inmunometabolismo, mediadores lipídicos, terapia con ARNm