Clear Sky Science · it
DPEP2 sopprime l’iperinfiammazione tramite la riprogrammazione metabolica dei macrofagi nella sepsi
Perché è importante placare la reazione eccessiva dell’organismo
La sepsi è una condizione potenzialmente letale in cui il sistema immunitario, nel tentativo di combattere un’infezione, entra in iperattivazione e inizia a danneggiare gli stessi organi dell’organismo. Nonostante antibiotici e cure intensive moderne, molte persone muoiono ancora perché questa infiammazione incontrollata è difficile da gestire senza spegnere difese vitali. Questo studio scopre una molecola “freno” naturale nelle cellule immunitarie di prima linea e mostra come potenziarla con una terapia a base di geni possa attenuare l’infiammazione nociva preservando al contempo la capacità di combattere i microrganismi.
Un freno nascosto nelle cellule che combattono le infezioni
I ricercatori si sono concentrati su monociti e macrofagi, cellule immunitarie che circolano nel sangue e pattugliano gli organi, lanciando l’allarme quando i microbi invadono. Utilizzando tecnologie d’avanguardia di sequenziamento dell’RNA a singola cellula e in blocco su campioni di sangue di pazienti nella fase iniziale della sepsi, hanno mappato l’attività genica cellula per cellula. Un gene, chiamato DPEP2, è emerso con evidenza: era fortemente attivo nei monociti e macrofagi sani ma costantemente ridotto nei pazienti con sepsi. Livelli più bassi di DPEP2 erano strettamente associati a punteggi di insufficienza d’organo peggiori, a livelli più alti di molecole infiammatorie nel sangue e a un rischio di morte più elevato. I pazienti sopravvissuti avevano più monociti positivi per DPEP2 rispetto a quelli deceduti, suggerendo che questa molecola aiuta a contenere gli impulsi più pericolosi del sistema immunitario.
Dal segnale genico al danno sistemico
Per verificare se DPEP2 fosse solo un marcatore o un protettore attivo, il team ha usato modelli cellulari e animali. In macrofagi murini e umani coltivati in laboratorio, l’inattivazione di DPEP2 ha indotto queste cellule a secernere molte più citochine infiammatorie quando stimolate con componenti batteriche. In topi sottoposti a un modello chirurgico standard di sepsi, gli animali privi di DPEP2 – sia globalmente sia specificamente nei macrofagi – hanno avuto esiti molto peggiori. Presentavano livelli più alti di molecole infiammatorie nel circolo, danni più severi a polmoni, fegato, reni, cuore e cervello, e tassi di mortalità significativamente maggiori. Questi esperimenti dimostrano che DPEP2 non è solo un indicatore della gravità della malattia, ma un difensore attivo contro l’infiammazione travolgente.
Come un enzima del metabolismo lipidico doma l’incendio
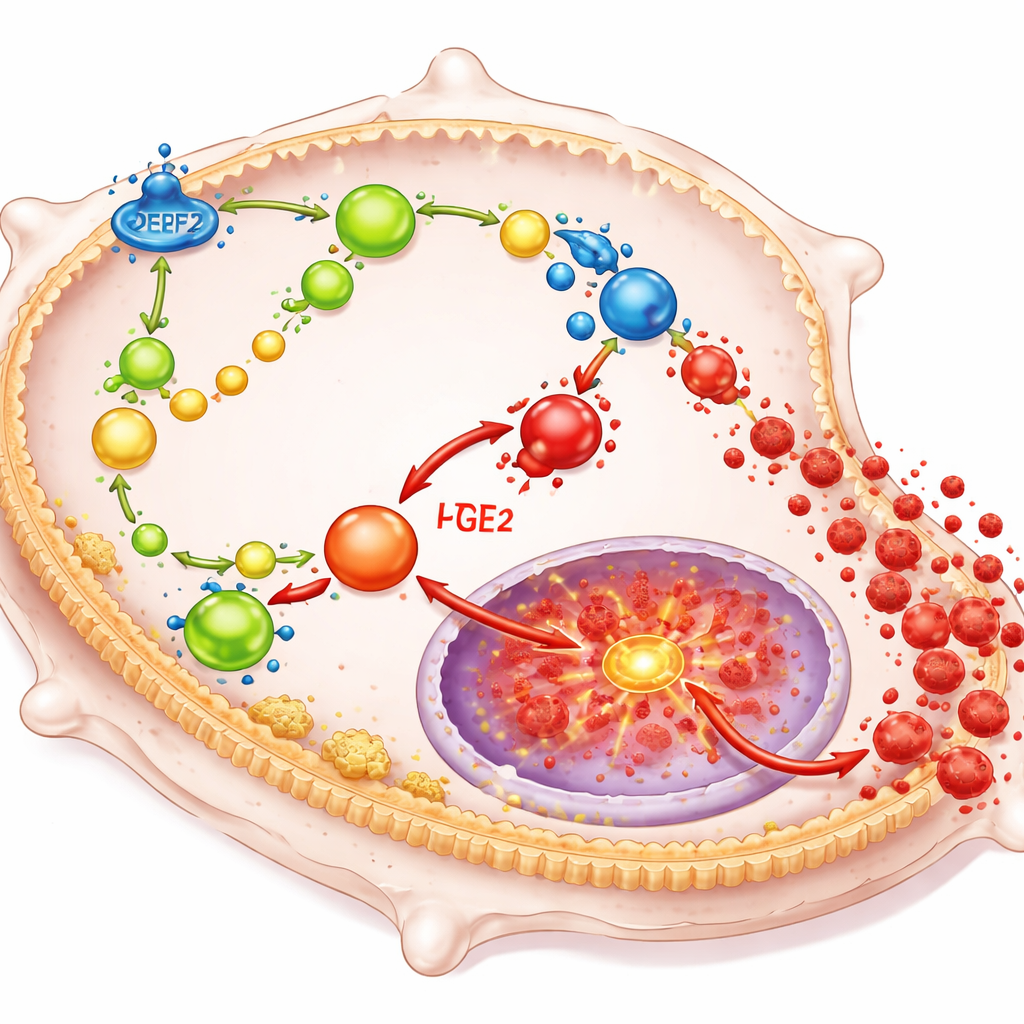
DPEP2 agisce rimodellando il modo in cui i macrofagi gestiscono specifiche molecole lipidiche che funzionano come potenti ormoni locali. In particolare, contribuisce alla degradazione di un composto chiamato leucotriene D4 in un prodotto meno infiammatorio, e la sua perdita causa l’accumulo di leucotriene D4. Questo accumulo, a sua volta, spinge più precursori lipidici della cellula verso la sintesi di prostaglandina E2, un altro forte promotore dell’infiammazione. Insieme, questi lipidi convergono su un interruttore molecolare chiave all’interno della cellula noto come NF-κB, che regola i geni di molte citochine infiammatorie. Quando DPEP2 manca o è basso, questa rete di segnali lipidici funziona senza freni, attivando NF-κB e inducendo i macrofagi a invadere l’organismo con fattori infiammatori dannosi.
Riprogrammare le cellule immunitarie con mRNA
Armati di questa intuizione meccanicistica, gli scienziati hanno chiesto se il ripristino di DPEP2 potesse aiutare a salvare gli animali dalla sepsi. Hanno progettato nanoparticelle lipidiche — piccole bolle di grasso simili a quelle usate nei vaccini a mRNA — per veicolare l’mRNA di Dpep2 specificamente in monociti e macrofagi. Dopo iniezione endovenosa, queste particelle hanno aumentato temporaneamente i livelli di DPEP2 nelle cellule bersaglio. Nei topi settici trattati con nanoparticelle cariche di Dpep2, i marcatori dell’infiammazione sono diminuiti, i danni polmonari e d’organo si sono attenuati e la sopravvivenza è migliorata rispetto agli animali di controllo. È importante che il trattamento abbia funzionato senza tossicità evidente e sia svanito in circa un giorno e mezzo, in linea con la finestra critica iniziale in cui avvengono la maggior parte dei decessi per sepsi.
Implicazioni per la cura futura della sepsi
Questo lavoro mette in luce DPEP2 come una salvaguardia naturale cruciale che impedisce alle cellule che combattono le infezioni di spingere l’organismo verso un’autodistruzione letale. Mostrando che i livelli di DPEP2 nei monociti circolanti riflettono la gravità della malattia, lo studio suggerisce che potrebbe servire come utile biomarcatore ematico per identificare i pazienti a più alto rischio. Ancora più significativo, il successo della terapia con nanoparticelle contenenti mRNA di Dpep2 nei topi indica una nuova classe di trattamenti di precisione: invece di sopprimere in modo indiscriminato l’immunità, i clinici potrebbero un giorno modulare selettivamente interruttori metabolici specifici nelle cellule immunitarie per attenuare la tempesta infiammatoria nella sepsi preservando la difesa dell’ospite.
Citazione: Luo, W., Xu, W., Yin, Q. et al. DPEP2 suppresses hyperinflammation via metabolic reprogramming of macrophages in sepsis. Nat Commun 17, 3710 (2026). https://doi.org/10.1038/s41467-026-70466-4
Parole chiave: sepsi, macrofagi, immunometabolismo, mediatori lipidici, terapia mRNA