Clear Sky Science · sv
DPEP2 dämpar hyperinflammation genom metabolisk omprogrammering av makrofager vid sepsis
Varför det är viktigt att lugna kroppens överreaktion
Sepsis är ett livshotande tillstånd där kroppens immunsystem, i försök att bekämpa en infektion, går in i övervarv och börjar skada egna organ. Trots antibiotika och modern intensivvård dör många fortfarande eftersom denna okontrollerade inflammation är svår att kontrollera utan att slå ut viktiga försvar. Denna studie avslöjar en naturlig ”broms”-molekyl i frontlinjens immunceller och visar hur förstärkning av den med en genbaserad terapi skulle kunna dämpa skadlig inflammation samtidigt som förmågan att bekämpa mikrober bevaras.
En dold broms i infektskyddande celler
Forskarlaget fokuserade på monocyter och makrofager, immunceller som cirkulerar i blodet och patrullerar organ, och som larmar när mikrober invaderar. Genom att använda avancerad single-cell- och bulk RNA-sekvensering på blod från patienter i det tidiga skedet av sepsis kartlade de genaktivitet cell för cell. En gen, kallad DPEP2, stack ut: den var starkt aktiv i friska monocyter och makrofager men konsekvent minskad hos patienter med sepsis. Lägre nivåer av DPEP2 var tätt kopplade till värre organsviktpoäng, högre nivåer av inflammatoriska molekyler i blodet och större risk för död. Patienter som överlevde hade fler DPEP2-positiva monocyter än de som inte gjorde det, vilket tyder på att denna molekyl hjälper till att begränsa immunsystemets farligaste impulser.
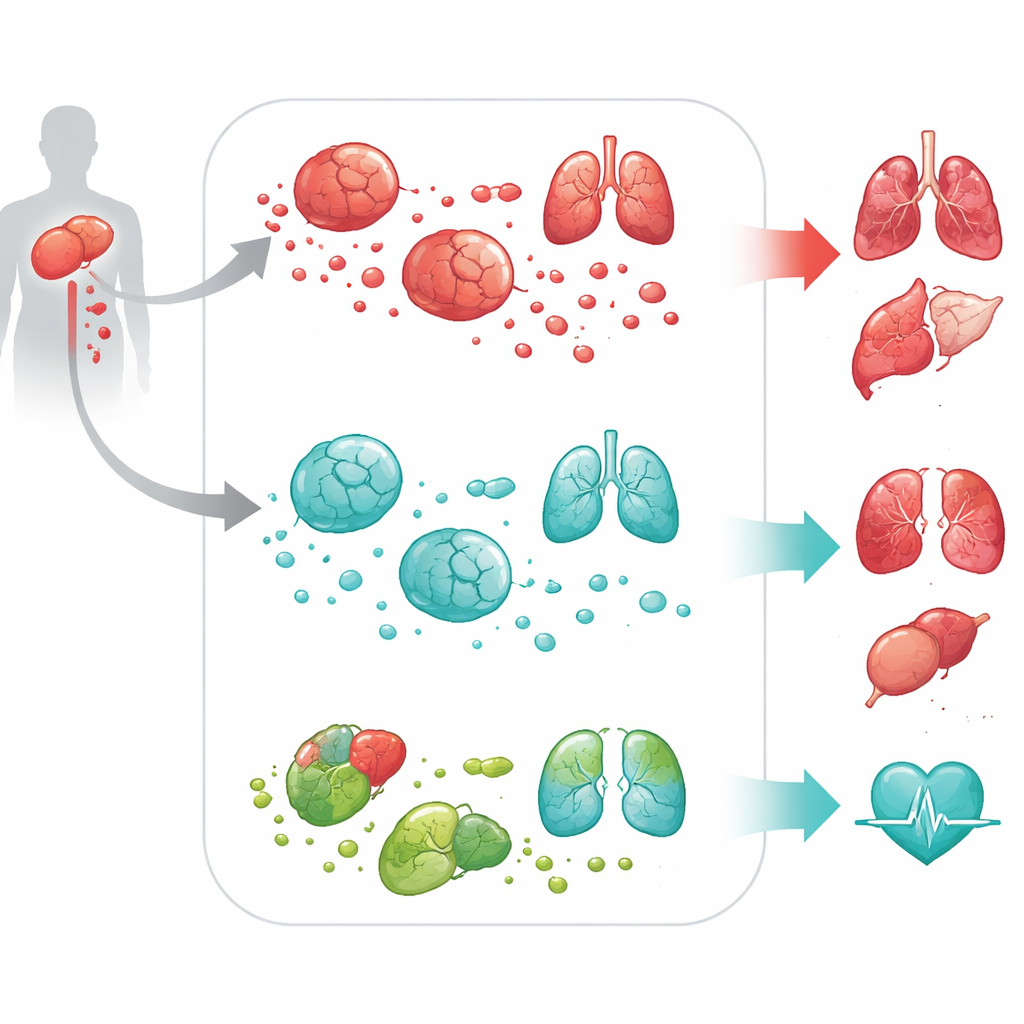
Från gensusignal till helkroppsskada
För att pröva om DPEP2 bara var en åskådare eller en aktiv beskyddare vände teamet sig till cell- och djurmodeller. I mus- och människomakrofager odlade i labbet ledde avstängning av DPEP2 till att dessa celler utsöndrade mycket mer inflammatoriska cytokiner när de stimulerades med bakteriella komponenter. I möss utsatta för en standardiserad, kirurgibaserad modell av sepsis klarade sig djur utan DPEP2 – antingen i hela kroppen eller specifikt i makrofager – mycket sämre. De hade högre nivåer av inflammatoriska molekyler i blodet, allvarligare skador på lungor, lever, njurar, hjärta och hjärna, och signifikant högre dödlighet. Dessa experiment visade att DPEP2 inte bara är en markör för sjukdomsgrad utan en aktiv försvarare mot överväldigande inflammation.
Hur ett fettbearbetande enzym dämpar elden
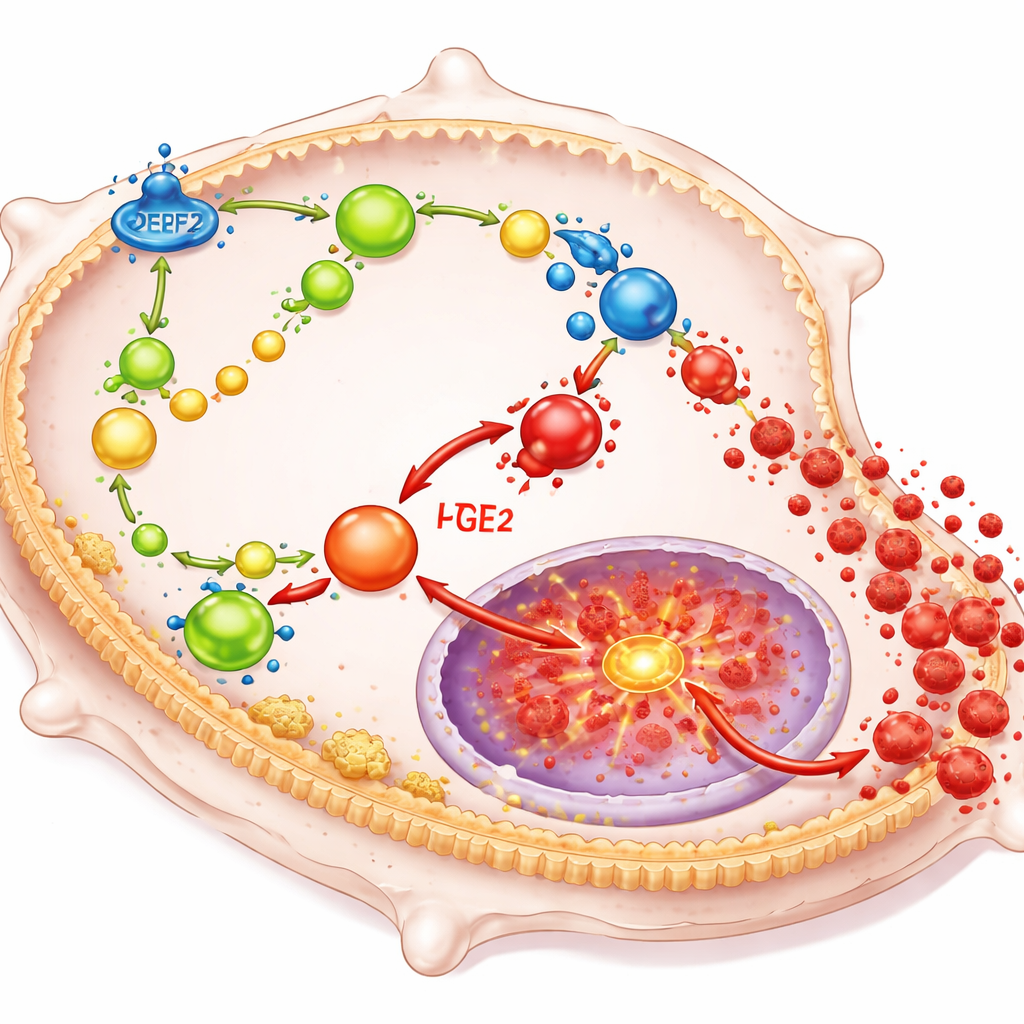
DPEP2 fungerar genom att omforma hur makrofager hanterar vissa fettsyrarelaterade molekyler som fungerar som kraftfulla lokala hormoner. Framför allt hjälper det till att bryta ner en förening kallad leukotrien D4 till en mindre inflammatorisk produkt, och förlust av DPEP2 leder till ansamling av leukotrien D4. Denna ansamling driver i sin tur fler av cellens fettbyggstenar mot bildandet av prostaglandin E2, en annan stark inflammationsdrivare. Tillsammans matar dessa lipider in i en central växling inne i cellen känd som NF-κB, som styr gener för många inflammatoriska cytokiner. När DPEP2 saknas eller är låg löper detta nätverk av fettbaserade signaler okontrollerat, aktiverar NF-κB och får makrofager att översvämma kroppen med skadliga inflammatoriska faktorer.
Omskrivning av immunceller med mRNA
Med denna mekanistiska insikt undrade forskarna om återställande av DPEP2 kunde hjälpa till att rädda djur från sepsis. De utformade lipidnanopartiklar—små fettbubblor liknande dem som används i mRNA-vacciner—för att leverera Dpep2-mRNA specifikt till monocyter och makrofager. Efter intravenös injektion ökade dessa partiklar kortvarigt DPEP2-nivåerna i målcellerna. I septiska möss behandlade med Dpep2-laddade nanopartiklar sjönk inflammationsmarkörer, lung- och organskador minskade, och överlevnaden förbättrades jämfört med kontrollgrupper. Viktigt är att behandlingen fungerade utan uppenbar toxicitet och avtog efter ungefär en och en halv dag, i linje med det kritiska tidiga fönster då sepsisdöd oftast inträffar.
Vad detta innebär för framtidens sepsisvård
Detta arbete avslöjar DPEP2 som en avgörande naturlig skyddsmekanism som hindrar infektskyddande celler från att vända kroppen mot dödligt självskadebeteende. Genom att visa att DPEP2-nivåer i blodmonocyter speglar sjukdomsgraden antyder studien att det kan fungera som en användbar blodbaserad biomarkör för att identifiera patienter med högst risk. Ännu mer slående är att framgången för Dpep2-mRNA–nanopartikelterapin i möss pekar mot en ny klass av precisionsbehandlingar: istället för att brett undertrycka immunitet kan kliniker en dag finjustera specifika metabola brytpunkter inne i immunceller för att dämpa den inflammatoriska stormen vid sepsis samtidigt som värdförsvaret bevaras.
Citering: Luo, W., Xu, W., Yin, Q. et al. DPEP2 suppresses hyperinflammation via metabolic reprogramming of macrophages in sepsis. Nat Commun 17, 3710 (2026). https://doi.org/10.1038/s41467-026-70466-4
Nyckelord: sepsis, makrofager, immunometabolism, lipidmediatorer, mRNA-terapi