Clear Sky Science · de
DPEP2 unterdrückt Hyperinflammation durch metabolische Umlenkung von Makrophagen bei Sepsis
Warum das Beruhigen der körpereigenen Überreaktion wichtig ist
Sepsis ist ein lebensbedrohlicher Zustand, bei dem das Immunsystem des Körpers im Versuch, eine Infektion zu bekämpfen, außer Kontrolle gerät und eigene Organe schädigt. Trotz Antibiotika und moderner Intensivmedizin sterben viele Menschen weiterhin, weil sich diese eskalierende Entzündung kaum beherrschen lässt, ohne zugleich lebenswichtige Abwehrmechanismen auszuschalten. Diese Studie entdeckt ein natürliches "Brems"-Molekül in den vordersten Reihen der Immunabwehr und zeigt, wie dessen Verstärkung mittels gentherapieähnlicher Ansätze schädliche Entzündungen dämpfen kann, ohne die Fähigkeit zur Bekämpfung von Krankheitserregern zu beeinträchtigen.
Eine verborgene Bremse in infektionabwehrenden Zellen
Die Forschenden konzentrierten sich auf Monozyten und Makrophagen, Immunzellen, die im Blut zirkulieren und Organe patrouillieren, um Alarm zu schlagen, wenn Mikroben eindringen. Mithilfe moderner Einzelzell- und Bulk-RNA-Sequenzierung von Blutproben aus der frühen Phase der Sepsis kartierten sie die Genaktivität Zelle für Zelle. Ein Gen, DPEP2 genannt, stach hervor: Es war in gesunden Monozyten und Makrophagen stark aktiv, in Sepsispatienten dagegen durchgängig vermindert. Geringere DPEP2-Werte standen in enger Beziehung zu schlechteren Organfunktionswerten, höheren Spiegeln entzündlicher Moleküle im Blut und einem höheren Sterberisiko. Überlebende hatten mehr DPEP2-positive Monozyten als Nicht-Überlebende, was darauf hindeutet, dass dieses Molekül hilft, die gefährlichsten Impulse des Immunsystems zu zügeln.
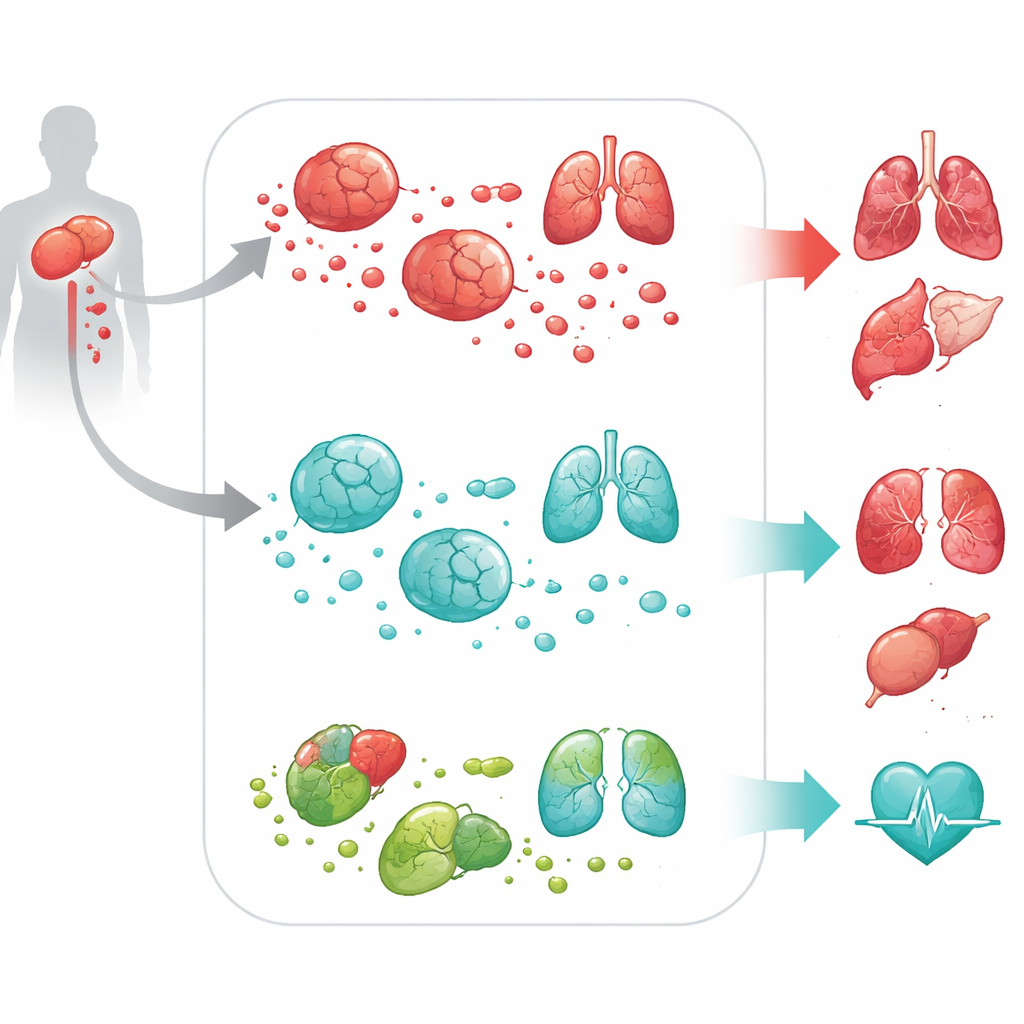
Vom Gen-Signal zum Schaden im ganzen Körper
Um zu prüfen, ob DPEP2 nur ein Begleiter oder ein aktiver Schutzfaktor ist, griff das Team auf Zell- und Tiermodelle zurück. In im Labor gezüchteten Maus- und Humanmakrophagen führte das Abschalten von DPEP2 dazu, dass diese Zellen nach Stimulation mit bakteriellen Komponenten deutlich mehr entzündliche Zytokine ausschütteten. In Mäusen, die einem etablierten operationsbasierten Sepsismodell unterzogen wurden, erlitten Tiere ohne DPEP2 – entweder systemisch oder spezifisch in Makrophagen – deutlich schlechtere Verläufe. Sie wiesen höhere Konzentrationen entzündlicher Moleküle im Blut, schwerere Verletzungen von Lunge, Leber, Niere, Herz und Gehirn sowie deutlich höhere Sterblichkeitsraten auf. Diese Experimente zeigten, dass DPEP2 nicht nur ein Marker für Krankheits-Schwere ist, sondern ein aktiver Verteidiger gegen überwältigende Entzündungen.
Wie ein fettabbauendes Enzym das Feuer zügelt
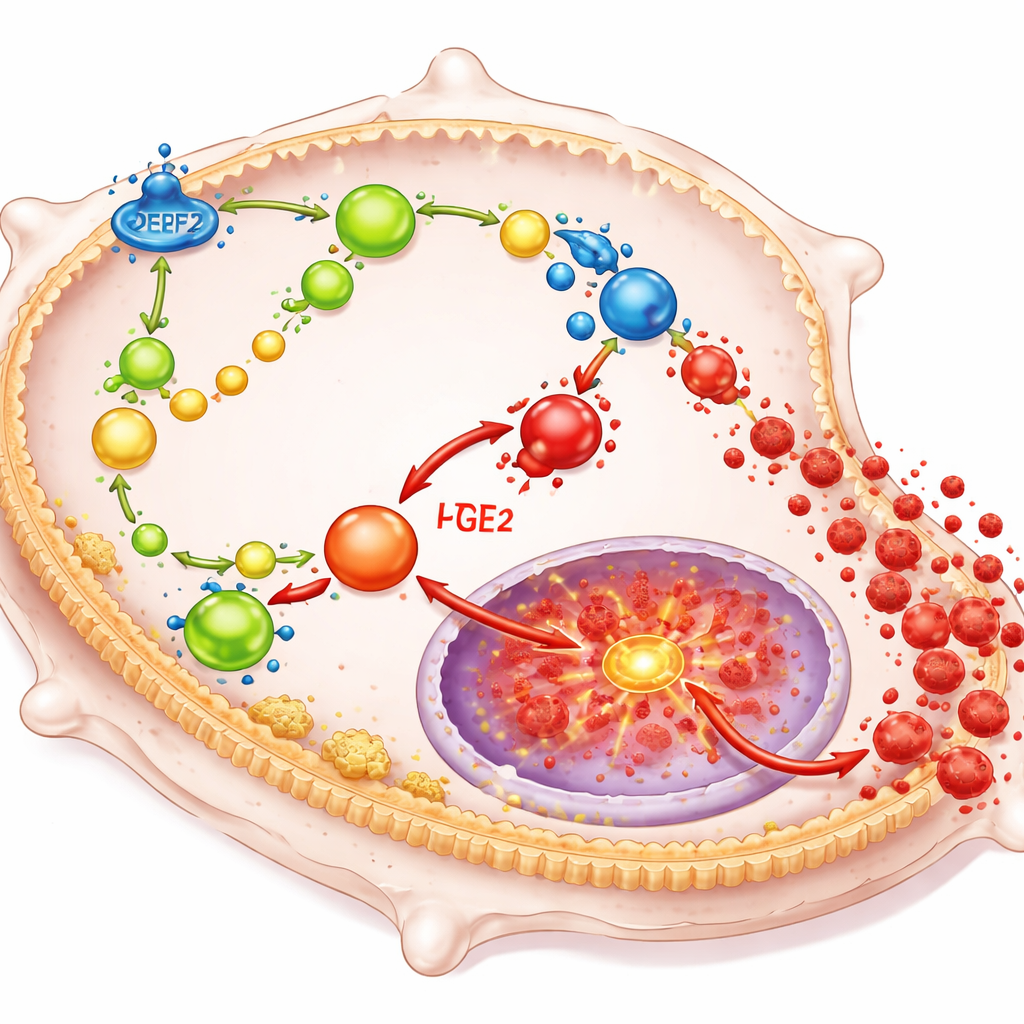
DPEP2 wirkt, indem es die Verarbeitung bestimmter Fettmoleküle in Makrophagen verändert, die als potente lokale Hormone fungieren. Insbesondere hilft es beim Abbau einer Verbindung namens Leukotrien D4 zu einem weniger entzündlichen Produkt; bleibt DPEP2 aus, häuft sich Leukotrien D4 an. Diese Anhäufung lenkt zudem mehr der fetten Bausteine der Zelle in Richtung Bildung von Prostaglandin E2, einem weiteren starken Entzündungsförderer. Zusammen wirken diese Lipide auf einen wichtigen Schaltpunkt in der Zelle, bekannt als NF-κB, der die Gene vieler entzündlicher Zytokine steuert. Fehlt DPEP2 oder ist es niedrig, läuft dieses Netzwerk aus fettbasierten Signalen ungebremst, aktiviert NF-κB und bringt Makrophagen dazu, den Körper mit schädlichen Entzündungsfaktoren zu überschwemmen.
Immunzellen mit mRNA umprogrammieren
Gestützt auf diese mechanistische Erkenntnis fragten die Wissenschaftler, ob die Wiederherstellung von DPEP2 Tieren in der Sepsis helfen könnte. Sie entwickelten Lipidnanopartikel – winzige Fettbläschen ähnlich denen in mRNA-Impfstoffen –, um Dpep2-mRNA gezielt in Monozyten und Makrophagen zu bringen. Nach intravenöser Injektion steigerten diese Partikel vorübergehend die DPEP2-Spiegel in den Zielzellen. Bei septischen Mäusen, die mit den Dpep2-beladenen Nanopartikeln behandelt wurden, sanken Entzündungsmarker, Lungen- und Organschäden besserten sich, und das Überleben verbesserte sich im Vergleich zu Kontrolltieren. Wichtig ist, dass die Behandlung ohne offensichtliche Toxizität wirkte und nach etwa eineinhalb Tagen abklang – passend zum frühen kritischen Zeitfenster, in dem Sepsis-Todesfälle am häufigsten auftreten.
Was das für die künftige Sepsisversorgung bedeutet
Diese Arbeit identifiziert DPEP2 als eine entscheidende natürliche Schutzvorrichtung, die Infektionsabwehrzellen davon abhält, den Körper in tödliche Selbstschäden zu stürzen. Indem gezeigt wird, dass DPEP2-Spiegel in Blutmonozyten die Krankheits-Schwere widerspiegeln, legt die Studie nahe, dass es als Blut-Biomarker Patienten mit besonders hohem Risiko markieren könnte. Noch beeindruckender deutet der Erfolg der Dpep2-mRNA–Nanopartikel-Therapie bei Mäusen auf eine neue Klasse präziser Behandlungen hin: Statt die Immunität breit zu unterdrücken, könnten Ärzte eines Tages gezielt spezifische metabolische Schalter in Immunzellen justieren, um den entzündlichen Sturm bei Sepsis zu dämpfen und gleichzeitig die Wirtsabwehr zu erhalten.
Zitation: Luo, W., Xu, W., Yin, Q. et al. DPEP2 suppresses hyperinflammation via metabolic reprogramming of macrophages in sepsis. Nat Commun 17, 3710 (2026). https://doi.org/10.1038/s41467-026-70466-4
Schlüsselwörter: Sepsis, Makrophagen, Immunmetabolismus, Lipidmediatoren, mRNA-Therapie